Diacetylperoxid
Diacetylperoxid ist eine chemische Verbindung aus der Gruppe der organischen Peroxide.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
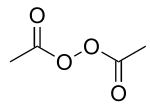 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Diacetylperoxid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C4H6O4 | |||||||||||||||
| Kurzbeschreibung |
farbloser Feststoff mit stechendem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 118,09 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
1,18 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
63 °C (28 hPa)[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Diacetylperoxid kann durch Reaktion von Natriumperoxid oder Wasserstoffperoxid mit Essigsäureanhydrid in einem Ester wie Dimethylphthalat gewonnen werden.[4]
Eigenschaften
Diacetylperoxid ist ein kristalliner explosiver farbloser Feststoff mit stechendem Geruch, der schwer löslich in Wasser ist. Wegen Detonationsgefahr wird der reine Stoff selten verwendet. Handelsüblich ist eine 25%ige Lösung in Dimethylphthalat. Bei Flüssigkeitstemperaturen unter −8 Grad bilden sich sehr stoß- und reibungsempfindliche Kristalle.[1] Bei der Zersetzung der Verbindung durch Licht oder Wärme entsteht Methylacetat.[5]
Verwendung
Diacetylperoxid wird als Polymerisationsstarter und für organische Synthesen verwendet.[2]
Einzelnachweise
- Eintrag zu Diacetylperoxid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 17. April 2017. (JavaScript erforderlich)
- Pradyot Patnaik: A Comprehensive Guide to the Hazardous Properties of Chemical Substances. John Wiley & Sons, 2007, ISBN 978-0-471-71458-3, S. 721 (eingeschränkte Vorschau in der Google-Buchsuche).
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- John G. Wallace: Hydrogen Peroxide in Organic Chemistry. Electrochemicals Department, Peroxygen Products Division, E.I. Du Pont de Nemours, 1962, OCLC 2098412, S. 82 (eingeschränkte Vorschau in der Google-Buchsuche).
- D. C. Nonhebel, J. C. Walton: Free-Radical Chemistry Structure and Mechanism. CUP Archive, 1974, ISBN 0-521-20149-7, S. 22 (eingeschränkte Vorschau in der Google-Buchsuche).