Di-tert-butylperoxid
Di-tert-butylperoxid ist eine chemische Verbindung aus der Gruppe der organischen Peroxide.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
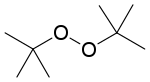 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Di-tert-butylperoxid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C8H18O2 | |||||||||||||||
| Kurzbeschreibung |
leichtentzündliche, flüchtige, farblose bis gelbliche Flüssigkeit mit etherischem Geruch[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 146,23 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig[1] | |||||||||||||||
| Dichte |
0,79 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt | ||||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex |
1,3891 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Gewinnung und Darstellung
Di-tert-butylperoxid kann durch Reaktion von tert-Butylhydroperoxid mit tert-Butylalkohol gewonnen werden.
Eigenschaften
Di-tert-butylperoxid ist eine leichtentzündliche, flüchtige, farblos bis gelbliche Flüssigkeit mit etherischem Geruch. Die Dämpfe von Di-tert-butylperoxid können mit Luft ein explosionsfähiges Gemisch (Flammpunkt 4 °C) bilden.[1]
Bei Erhitzung über 80 °C zersetzt sich die Verbindung.[1] Die Zersetzung verläuft mit einer Zersetzungswärme von −1211 kJ·kg−1 bzw. −177 kJ·mol−1 stark exotherm.[5] Dabei entstehen zunächst tert-Butoxyradikale, welche zu Aceton und Methylradikalen weiterreagieren können. Erfolgt diese Zersetzung in einer Lösung, so reagieren die entstehenden Methyl- und tert-Butoxyradikale mit dem Lösungsmittel, wobei sie diesem meist ein Wasserstoff-Atom entziehen (sog. radikalische Hydrogen-Abstraktion). Die resultierenden Lösungsmittelradikale können rekombinieren, wodurch sich entsprechende, substituierte Verbindungen erzeugen lassen (z. B. aus tertiären Aminen substituierte Ethylendiamine, aus primären und sekundären Alkoholen 1,2-Glycole).[6]
Verwendung
Di-tert-butylperoxid wird als Initiator für die Polymerisation von Olefinen und als Vernetzungsmittel für Silikonkautschuk verwendet.[1][2] Des Weiteren wird Di-tert-butylperoxid als Initiator für die Herstellung von sog. (Meth-)Acrylatharzen eingesetzt. Hierbei handelt es sich um einen Prozess der Lösungspolymerisation. Typische Anwendung solcher Bindemittel wären hochwertige Klarlacke im Automobilbereich.[7]
Risikobewertung
Di-tert-butylperoxid wurde 2013 von der EU gemäß der Verordnung (EG) Nr. 1907/2006 (REACH) im Rahmen der Stoffbewertung in den fortlaufenden Aktionsplan der Gemeinschaft (CoRAP) aufgenommen. Hierbei werden die Auswirkungen des Stoffs auf die menschliche Gesundheit bzw. die Umwelt neu bewertet und ggf. Folgemaßnahmen eingeleitet. Ursächlich für die Aufnahme von Di-tert-butylperoxid waren die Besorgnisse bezüglich der Einstufung als CMR-Stoff, Verbraucherverwendung, hoher (aggregierter) Tonnage und weit verbreiteter Verwendung. Die Neubewertung fand ab 2016 statt und wurde von den Niederlanden durchgeführt. Anschließend wurde ein Abschlussbericht veröffentlicht.[8][9]
Literatur
- Eduardo Lissi: Photolysis of Di-tert-butyl Peroxide in Solution. In: Canadian Journal of Chemistry. 52 (13), 1974, S. 2491–2492, doi:10.1139/v74-363.
Einzelnachweise
- Eintrag zu Di-tert-Butylperoxid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- Eintrag zu Di-tert-butylperoxid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 27. Januar 2017.
- Datenblatt tert-Butyl peroxide bei Sigma-Aldrich, abgerufen am 24. März 2011 (PDF).
- Eintrag zu Di-tert-butyl peroxide im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Yih-Shing Duh; Jin-Min Yo; Wen-Lian Lee; Chen-Shan Kao; Jing-Ming Hsu: Thermal decompositions of dialkyl peroxides studied by DSC. In: Journal of Thermal Analysis and Calorimetry, 2014, 118, S. 339–347; doi:10.1007/s10973-014-3998-6.
- K. Schwetlick, J. Jentzsch, R. Karl, D. Wolter: Reaktionen mit tert.-Butoxyradikalen. III. Dehydrodimerisierungen mit Di-tert.-butylperoxid. In: Journal für Praktische Chemie, 1964, 25 (1–2), S. 95–100; doi:10.1002/prac.19640250112.
- Ulrich Poth: Synthetische Bindemittel für Beschichtungssysteme. Vincentz Network, Hannover 2016, ISBN 978-3-86630-611-0.
- Europäische Chemikalienagentur (ECHA): Substance Evaluation Conclusion and Evaluation Report.
- Community rolling action plan (CoRAP) der Europäischen Chemikalienagentur (ECHA): Di-tert-butyl peroxide, abgerufen am 6. März 2022.

