Paramylon
Paramylon, Paramylum oder Curdlan ist ein Kohlenhydrat aus Glucose, das von manchen Algen und Bakterien gebildet wird. Es wurde erstmals 1850 von Johann Gottlieb basierend auf seinem wissenschaftlichen Austausch mit Ludwig Karl Schmarda benannt und beschrieben.[3]
| Strukturformel | |||
|---|---|---|---|
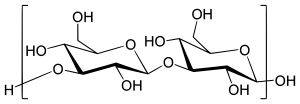 | |||
| Allgemeines | |||
| Name | Paramylon | ||
| Andere Namen |
| ||
| CAS-Nummer | 51052-65-4[1] | ||
| Monomer | D-Glucose | ||
| Summenformel der Wiederholeinheit | C6H10O5 | ||
| Molare Masse der Wiederholeinheit | 162,14 g·mol−1 | ||
| Art des Polymers |
β-D-(1→3)-Glucan | ||
| Eigenschaften | |||
| Aggregatzustand |
fest | ||
| Sicherheitshinweise | |||
| |||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||
Eigenschaften
Paramylon ist ein Homoglycan der Glucose mit glycosidischen Bindungen vom Typ β-(1,3), das unter anderem von Agrobacterium biobar, Euglena gracilis und Alcaligenes faecalis var. myxogenes gebildet wird. In manchen Arten kommen im Periplasma Paramylone mit zusätzlichen β-(1,6)-Bindungen vor.[4] Curdlan bzw. Paramylon wird von Bakterien als Teil der Glykokalyx oder als Speichergranula gebildet.
Paramylon bildet mit Wasser Hydrogele und nimmt in Wasser eine helikale Konformation an.[5] Es ist essbar und von der USFDA in den USA als Lebensmittelzusatzstoff zugelassen,[6] wo es als unverdauliches Verdickungsmittel verwendet wird.[7]
Agrobakterien
In Agrobakterien (sp. ATCC31749 und Agrobacterium tumefaciens) wurden vier an der Biosynthese beteiligte Gene beschrieben.[8] Ein Mangel an Stickstoffverbindungen führt zu einer verstärkten Biosynthese von Curdlan.[9]
Euglena

In Euglena wird Paramylon in den Pyrenoiden gebildet[10] und in stäbchenförmigen Partikeln im Zytosol gespeichert.[11] Paramylon ist ein bei Euglenophyceen und Kalkalgen (Haptophyta) vorkommender Reservestoff, der als Energiereserve genutzt wird.[12] Der Name leitet sich von Griechischen aus para (neben, bei) und mylos (Mühle) ab.[13] Paramylon besteht aus kettenförmig miteinander gebundenen D-Glucose-Molekülen, ist also ein Kohlenhydrat oder auch Polysaccharid. Während bei der Stärke der grünen Pflanzen und Rotalgen die Glucose α-1→4- und α-1→6-glycosidisch verknüpft ist, besteht das Paramylon der Euglenophyceen und der Kalkalgen aus β-1→3-glycosidisch verbundener Glucose.
In oben genannten Organismen wird der Speicherstoff im Cytoplasma in Form von Kügelchen deponiert, den sogenannten Paramylongranula.[13]
Verwendung und Wirkung
Wissenschaftliche Studien haben gezeigt, dass Paramylon einen positiven Einfluss auf den Blutzuckerspiegel, die Insulin-Regulation und den Cholesterinspiegel hat.[14] Eine weitere nachgewiesene Wirkung von Paramylon besteht darin, die Makrophagen-Aktivität anzuregen, auf diese Weise das Immunsystem zu stimulieren und so hemmende Effekte auf das Wachstum einiger Tumorarten zu haben.[15] Paramylon eignet sich auch als nachwachsender Rohstoff zur Herstellung von biologisch abbaubaren Kunststofffolien. Diese Folien sind in der Zellkulturtechnik, als Wundauflage und im Kosmetikbereich einsetzbar.[16] Als Lebensmittelzusatzstoff hat Curdlan die INS-Nummer 424.
Siehe auch
Literatur
- R. Zhang, K. J. Edgar: Properties, chemistry, and applications of the bioactive polysaccharide curdlan. In: Biomacromolecules. Band 15, Nummer 4, April 2014, S. 1079–1096, doi:10.1021/bm500038g. PMID 24552241.
- X. B. Zhan, C. C. Lin, H. T. Zhang: Recent advances in curdlan biosynthesis, biotechnological production, and applications. In: Applied Microbiology and Biotechnology. Band 93, Nummer 2, Januar 2012, S. 525–531, doi:10.1007/s00253-011-3740-2. PMID 22124723.
- E.J.F. Spicer, E.I. Goldenthal, T. Ikeda: A toxicological assessment of curdlan. In: Food and Chemical Toxicology. (1999), Band 37, S. 455–479, doi:10.1016/S0278-6915(99)00013-7.
Einzelnachweise
- Peter M. Collins: Dictionary of Carbohydrates. Chapman & Hall/CRC; 2. Auflage 2005; ISBN 0-8493-3829-8; S. 523.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- Professor J. Gottlieb: Ueber eine neue, mit Stärkmehl isomere Substanz. In: Annalen der Chemie und Pharmacie. Band 75, Nummer 1, 1850, S. 51–61, doi:10.1002/jlac.18500750105.
- M. McIntosh, B. A. Stone, V. A. Stanisich: Curdlan and other bacterial (1–>3)-beta-D-glucans. In: Applied Microbiology and Biotechnology. Band 68, Nummer 2, August 2005, S. 163–173, doi:10.1007/s00253-005-1959-5. PMID 15818477.
- B. C. Lehtovaara, F. X. Gu: Pharmacological, structural, and drug delivery properties and applications of 1,3-β-glucans. In: Journal of agricultural and food chemistry. Band 59, Nummer 13, Juli 2011, S. 6813–6828, doi:10.1021/jf200964u. PMID 21609131.
- USFDA Code of Federal Regulations Title 21: Sec. 172.809 Curdlan.
- Joint FAO/WHO Expert Committee on Food Additives (JECFA), Monograph für Curdlan, abgerufen am 15. April 2015.
- T. Karnezis, V. C. Epa, B. A. Stone, V. A. Stanisich: Topological characterization of an inner membrane (1–>3)-beta-D-glucan (curdlan) synthase from Agrobacterium sp. strain ATCC31749. In: Glycobiology. Band 13, Nummer 10, Oktober 2003, S. 693–706, doi:10.1093/glycob/cwg093. PMID 12851288.
- A. M. Ruffing, R. R. Chen: Transcriptome profiling of a curdlan-producing Agrobacterium reveals conserved regulatory mechanisms of exopolysaccharide biosynthesis. In: Microbial cell factories. Band 11, 2012, S. 17, doi:10.1186/1475-2859-11-17. PMID 22305302. PMC 3293034 (freier Volltext).
- R. Calvayrac, D. Laval-Martin, J. Briand, J. Farineau: Paramylon synthesis by Euglena gracilis photoheterotrophically grown under low O2 pressure : Description of a mitochloroplast complex. In: Planta. Band 153, Nummer 1, Oktober 1981, S. 6–13, doi:10.1007/BF00385311. PMID 24276700.
- A. K. Monfils, R. E. Triemer, E. F. Bellairs: „Characterization of paramylon morphological diversity in photosynthetic euglenoids (Euglenales, Euglenophyta)“. Phycologia (2011), Band 50, Heft 2, S. 156. doi:10.2216/09-112.1.
- Rüdiger Wehner, Walter Gehring, Alfred Kühn: Zoologie. Thieme, Stuttgart 24. Auflage 2007; ISBN 3-13-772724-3; S. 681.
- Cleveland P. Hickman, Larry S. Roberts, Allan Larson, Helen LAnson, David J. Eisenhour, Thomas Lazar (Übersetzer): Zoologie. Addison-Wesley Verlag München; 13. aktualisierte Auflage 2008; ISBN 978-3-8273-7265-9; S. 1287.
- BARSANTI L, VISMARA R, PASSARELLI V & GUALTIERI P (2001) Paramylon (β-1,3-glucan) content in wild type and WZSL mutant of Euglena gracilis. Effects of growth conditions. J Appl Phycol 13:59–65.
- QUESEDA LA DE LUSTIG ES, MARECHAL LR & BELOCOPITOW E (1976) Antitumor activity of paramylon on sarcoma-180 in mice. Gann 67:455–459.
- BÄUMER D (1998) Isolierung und partielle Charakterisierung der Paramylonsynthase aus Euglena gracilis (Euglenozoa). Dissertation Universität Bielefeld.