Carbonylbromid
Carbonylbromid (Bromphosgen) ist eine chemische Verbindung aus der Gruppe der Säurehalogenide. Sie ist das Dibromid der Kohlensäure.
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
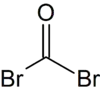 | ||||||||||
| Allgemeines | ||||||||||
| Name | Carbonylbromid | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | CBr2O | |||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit starkem Geruch[1] | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 187,81 g·mol−1 | |||||||||
| Aggregatzustand |
flüssig[1] | |||||||||
| Dichte |
2,5 g·cm−3[1] | |||||||||
| Siedepunkt |
65 °C[1] | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||
Gewinnung und Darstellung
Carbonylbromid wurde zuerst 1863 durch J. Schiel durch Reaktion von Kohlenmonoxid mit Bromdampf in Sonnenlicht synthetisiert.[3]
Es wird heute durch Reaktion von Tetrabromkohlenstoff mit Schwefelsäure bei 150–170 °C mit etwa 50 % Ausbeute gewonnen.[3]
Eigenschaften
Carbonylbromid ist eine farblose Flüssigkeit mit starkem Geruch, die an Luft raucht[1] und sich bei erhöhten Temperaturen (vor allem in Gegenwart von Verunreinigungen) oder Lichteinfluss zu Kohlenstoffmonoxid und elementarem Brom zersetzt.[3] Sie hydrolysiert in Wasser zu Bromwasserstoff und Kohlendioxid.[1]
Verwendung
Carbonylbromid wird zur Herstellung von Farbstoffen verwendet.[1]
Einzelnachweise
- Dale L. Perry: Handbook of Inorganic Compounds. CRC Press, 1995, ISBN 978-0-8493-8671-8, S. 101 (eingeschränkte Vorschau in der Google-Buchsuche).
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- T.A. Ryan, E.A. Seddon, K.R. Seddon, C. Ryan: Phosgene And Related Carbonyl Halides. Elsevier, 1996, ISBN 978-0-08-053880-8, S. 666–667 (eingeschränkte Vorschau in der Google-Buchsuche).