Bromsäure
Bromsäure ist eine chemische Verbindung der Elemente Brom, Sauerstoff und Wasserstoff mit der Formel HBrO3. Ihre Salze sind die Bromate.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
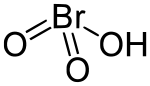 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Bromsäure | |||||||||||||||
| Andere Namen |
Brom(V)-säure | |||||||||||||||
| Summenformel | HBrO3 | |||||||||||||||
| Kurzbeschreibung |
nur als wässrige Lösung stabile farblose Flüssigkeit[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 128,91 g·mol−1 | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||
Gewinnung und Darstellung
Ihre Darstellung kann durch Umsetzung von Bariumbromat mit verdünnter Schwefelsäure erfolgen.[3] Hierbei fällt das schwerlösliche Bariumsulfat aus und die Bromsäure bleibt in Lösung.
Eigenschaften
Sie gehört zu den Halogensauerstoffsäuren und ist verwandt mit der Chlorsäure und der Iodsäure und wie diese pyramidal aufgebaut. Sie ist ein starkes Oxidationsmittel und wird deshalb für Redoxtitrationen eingesetzt. Weiterhin ist sie wichtig bei Belousov-Zhabotinsky-Reaktionen.
Bromsäure ist eine nicht sehr beständige Säure und kann nur in wässriger Lösung dargestellt werden. Ab einem Gehalt von 50 % tritt Zersetzung ein:[4]
Einzelnachweise
- Eintrag zu Bromsäure. In: Römpp Online. Georg Thieme Verlag, abgerufen am 29. September 2014.
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- G. Brauer (Hrsg.), Handbook of Preparative Inorganic Chemistry 2nd ed., vol. 1, Academic Press 1963, S. 315–6.
- Universität Kiel: Vorlesungsskript Brom und Bromverbindungen (Memento vom 29. September 2007 im Internet Archive; PDF; 85 kB)