Borsche-Koelsch-Cinnolinsynthese
Die Borsche-Koelsch-Cinnolinsynthese ist eine Namensreaktion in der organischen Chemie. Die Reaktion ist nach ihren Entdeckern, dem deutschen Chemiker Walther Borsche (1877–1959)[1] und dem US-amerikanischen Chemiker Charles Frederick Koelsch (1907–1999)[2], benannt und dient der Synthese von 4-Hydroxycinnolin und 4-Hydroxy-3-alkylcinnolin aus ortho-Aminoarylketonen.[3]
Übersichtsreaktion
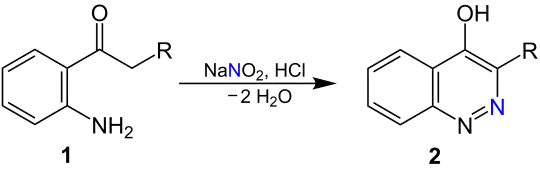
Ein ortho-Aminoarylketon 1 reagiert mit Natriumnitrit und Salzsäure unter Wasserabspaltung und Cyclisierung zu einem 4-Hydroxycinnolin 2. Alternativ kann Butylnitrit und Schwefelsäure verwendet werden.
Reaktionsmechanismus
Ein plausibler Ablauf der Reaktion ist folgender.[3] Im ersten Schritt findet eine Diazotierung mit dem aus Natriumnitrit und Salzsäure gebildeten Nitrosylkation statt. Das Enol-Tautomer 3 wird gebildet und es kommt unter Protonenabspaltung zur Cyclisierung, wodurch das Keto-Tautomer des 4-Hydroxycinnolins 4 entsteht. Das Endprodukt 5 ist das stabilere Enol-Tautomer.

Einzelnachweise
- Walther Borsche, Alfred Herbert: Synthesen mit 5-Nitro-2-brom-acetophenon. In: Justus Liebigs Annalen der Chemie. Band 546, Nr. 3, 1941, S. 293–303, doi:10.1002/jlac.19415460306.
- C. F. Koelsch: An Indole Synthesis from a m-Carboxyphenylhydrazone. In: The Journal of Organic Chemistry. Band 08, Nr. 4, 1943, S. 295–299, doi:10.1021/jo01192a001.
- Zerong Wang (Hrsg.): Comprehensive Organic Name Reactions and Reagents. John Wiley & Sons, Hoboken, New Jersey 2010, ISBN 978-0-470-63885-9, Borsche-Koelsch Cinnoline Synthesis, S. 474–477, doi:10.1002/9780470638859.conrr104.