Bisphosphonate
Bisphosphonate (auch Diphosphonate) sind chemische Verbindungen, die über zwei Phosphonat-Gruppen verfügen.

Verwendung
Bisphosphonate gehören einer Medikamentengruppe an, die seit den 1980er-Jahren für diagnostische und therapeutische Zwecke bei Knochen- und Calciumstoffwechselkrankheiten entwickelt wurde. Einige Verbindungen dieses Typs werden in Medikamenten zur Behandlung der Osteoporose verwendet. Sie sind in Deutschland zur Therapie der Osteoporose bei postmenopausalen Frauen, der Osteodystrophia deformans und der Tumor-assoziierten Hyperkalzämie zugelassen. Darüber hinaus finden sie Einsatz bei der Behandlung von Knochenmetastasen und Fibröser Dysplasie.[1]
In einer Studie aus dem Jahr 2009 wurde außerdem durch Hinzufügen von Zoledronat (eine Substanz aus der Gruppe der Bisphosphonate) zur endokrinen Therapie bei hormonsensiblem Brustkrebs eine längere rezidivfreie Überlebenszeit erzielt.[2]
Bisphosphonate dienen auch in Verbindung mit 99mTechnetium als Tracer in dem nuklearmedizinischen Untersuchungsverfahren Skelettszintigrafie. Dabei werden sie in einer sehr niedrigen, pharmakologisch nicht wirksamen Dosis angewendet.
Das Bisphosphonat Lexidronam wird in Verbindung mit dem überwiegenden Beta-Strahler 153Samarium zur palliativen analgetischen Therapie bei Knochenmetastasen eingesetzt (Radionuklidtherapie).
Wirkmechanismus
Bisphosphonate können Biomembranen zwar nur sehr schwer überwinden, die Osteoklasten nehmen Bisphosphonate aber im Rahmen des Abbaus von Knochensubstanz durch Phagozytose auf. Diese Aufnahme führt dazu, dass die Lebensdauer der Osteoklasten verkürzt wird. Dies wiederum bewirkt letztlich die therapeutisch erwünschte Verringerung des Knochenabbaus.
Bisphosphonate üben mehrere Effekte auf den Knochen aus: Durch Anlagerung an die Knochenoberfläche hemmen sie einerseits die Mineralisation der Knochensubstanz, andererseits hemmen sie den Knochenabbau durch Hemmung der Osteoklasten-Aktivität: Insbesondere die stickstoffreichen Bisphosphonate hemmen die Protonen-ATPase (direkt toxischer Effekt) und hemmen die Enzyme des Mevalonsäurestoffwechsels. Experimentell und klinisch belegt ist außerdem ihr direkter Einfluss auf das Monozyten-Makrophagen-System, indem sie die Rekrutierung und Fusionierung der Osteoklasten-Vorläufer torpedieren. Außerdem bewirken sie die Verkürzung der osteoklastären Lebensdauer durch Induktion der Apoptose, wahrscheinlich verbunden mit einer Verlängerung der osteoblastären Lebensdauer: Durch Hemmung der Farnesylpyrophosphat-Synthase können die Produkte dieses Enzyms, Farnesyl- und Geranylpyrophosphat kleine G-Proteine (u. a. Ras) nicht mehr in der Zellmembran verankern. Fehlen diese G-Proteine, haben an Zellrezeptoren gebundene Wachstumsfaktoren keine Auswirkung auf die Zelle mehr. Infolgedessen sterben die Osteoklasten im Rahmen der Apoptose ab.[3] Und schließlich bewirken sie die Hemmung von Prostacyclinen und anderen Cytokininen im Knochengewebe.[4]
Wirkstoffe

Die Bisphosphonate sind Ester und Salze der Methylendiphosphonsäure (Medronsäure). Sie sind Diphosphat-Analoga, in denen der Sauerstoff der P–O–P-Bindung durch Kohlenstoff ersetzt ist. Verbindungen dieses Typs zählen zu den Phosphonaten. Sie unterliegen im Körper keiner enzymatischen Hydrolyse. Bevor man ihre therapeutische Wirkung bei Osteoporose entdeckte, wurden Bisphosphonate unter anderem als Waschmittelzusätze verwendet. Durch Modifikationen der Molekülstruktur wurden ihre therapeutischen Eigenschaften schrittweise verbessert. So sind die neuesten Bisphosphonate 20000-mal potenter als Etidronat, das Bisphosphonat der ersten Generation. Sie unterscheiden sich in den Seitenketten und bilden demnach vier Gruppen:
- Bisphosphonat ohne Stickstoff: Etidronat, Clodronat, Tiludronat
- Aminobisphosphonate: Pamidronat, Alendronat
- am Stickstoff substituierte Aminobisphosphonate: Ibandronat
- Bisphosphonate mit einem basischen Heterocyclus: Risedronat, Zoledronat.
In Deutschland sind folgende Bisphosphonate zugelassen: Alendronat, Clodronat, Etidronat, Ibandronat, Pamidronat, Risedronat, Tiludronat und Zoledronat. Zur Skelettszintigrafie wird unter anderem Oxidronat (HDP) (nur in der Schweiz zugelassen) verwendet.
- In der Medizin verwendete Bisphosphonate
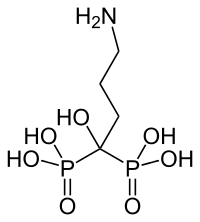 Alendronsäure zur Behandlung der Osteoporose
Alendronsäure zur Behandlung der Osteoporose Hydroxyethyliden-
Hydroxyethyliden-
Diphosphonat (HEDP, Etidronsäure) zur Skelettszintigrafie 2,3-Dicarboxypropan-
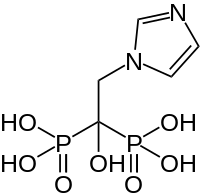
2,3-Dicarboxypropan-
1,1-Diphosphonat (DPD) zur Skelettszintigrafie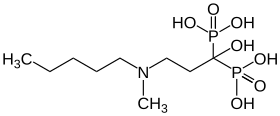

Pharmakokinetik
Bisphosphonate werden im Darm schlecht resorbiert und bilden mit Calcium unlösliche Komplexe. Die Resorptionsquote nach oraler Einnahme liegt zwischen 1 und 10 % der eingenommenen Dosis, teilweise ist sie noch geringer. Die Einnahmevorschriften müssen daher genau eingehalten werden. Bisphosphonate sollten morgens nüchtern mindestens 30 Minuten vor weiterer Nahrungsaufnahme oder anderen Medikamenten mit einem vollen Glas Leitungswasser eingenommen werden. Diese Vorschriften entfallen bei intravenöser Gabe durch Infusion oder Injektion.
Etwa 20–50 % der resorbierten Menge wird im Knochen gespeichert. Der Rest wird innerhalb von 24 Stunden mit dem Urin oder Stuhl ausgeschieden. Die Halbwertszeit der Bisphosphonate im Skelett beträgt viele Jahre, ähnlich wie bei Tetracyclinen oder Strontium.
Nebenwirkungen
Bei oraler Gabe treten bei zwei bis zehn Prozent der Patienten gastrointestinale Beschwerden wie Übelkeit, Bauchschmerzen, Erbrechen und Durchfall auf. Aufrechte Haltung während der Einnahme kann einen Rückfluss in die Speiseröhre (gastroösophagealer Reflux) und damit gastrointestinale Störungen vermeiden. Durch Komplexbildung mit Calciumionen im Darm können gelegentlich Hypokalzämien vorkommen. In Schwangerschaft und Stillzeit sind Bisphosphonate kontraindiziert.
In jüngster Zeit mehren sich Hinweise auf bisphosphonatassoziierte Knochennekrosen im Kieferbereich (BONJ, bisphosphonate-associated osteonecrosis of the jaw oder BRONJ, bisphosphonate-related osteonecrosis of the jaw), die klinisch sehr den Symptomen einer Osteoradionekrose ähneln und sehr therapieresistent sind. Ein relevantes Risiko für eine BP-assoziierte ONJ besteht, wenn aufgrund einer malignen Grunderkrankung Bisphosphonate intravenös in hohen Dosen und über einen längeren Zeitraum verabreicht werden. Das Committee for Medicinal Products for Human Use (CHMP) der EMA (European Medicines Agency, Europäische Arzneimittelagentur) hat mit einer Mitteilung vom 24. September 2009 diese unerwünschten Wirkungen aus den Daten des Eudravigilance-Vorhabens bestätigt und weitere Ursachenforschungen gefordert.[5] Aber auch bei alleiniger oraler Medikation sind mittlerweile Fälle von Kieferknochennekrosen bekannt, meist im Zusammenhang mit einer vorhergehenden Zahnextraktion. Die Bisphosphonate inhibieren endotheliale Zellen und stören damit die intraossäre Angiogenese des Knochens. Der geschädigte Knochen ist somit in seiner Fähigkeit, auf Infekte oder Traumata zu reagieren, eingeschränkt.
Bisphosphonat-assoziierte Kiefernekrosen wurden nach einer Latenzzeit von gut zehn Jahren nach Zulassung der ersten Bisphosphonate in den späten 1980er-Jahren als Syndrom beschrieben.[6] Diese Kiefernekrosen ähnelten den Phosphornekrosen des Kiefers, englisch phossy jaw, nach Vergiftungen durch weißen Phosphor, wie sie im 19. Jahrhundert aus der Streichholz-Industrie bekannt waren. Die klinische Diagnose der Bisphosphonat-assoziierten Kiefernekrose ist nur schwer zu stellen. Definitionsgemäß ergibt sie sich aus der Anamnese mit einer Vorbehandlung mit oralen oder intravenös verabreichten Bisphosphonaten. In einigen Studien hat der Gesichtsschädel eine bis zu 20-fach höhere knöcherne Umbauaktivität als das übrige Skelett, was die verstärkte Bisphosphonateinlagerung im Kieferknochen erklären könnte.[7] Eine Zahnsanierung vor der Behandlung und eine Verlängerung der Dosierungsintervalle könnten nach den Ergebnissen einer Beobachtungsstudie in JAMA Oncology das Risiko senken.[8]
In der Skelettszintigrafie verwendete Bisphosphonate haben aufgrund der extrem niedrigen Dosierung keine Nebenwirkungen. Lediglich bei fehlerhafter Injektion in das Gewebe neben der Vene kommt es zu einem sehr kurz anhaltenden brennenden Gefühl. Die Einschränkungen der Indikation nuklearmedizinischer Untersuchungen in Schwangerschaft und Stillzeit sowie die Strahlenexposition durch das Radionuklid sind zu beachten.
Laut der HORIZON-Studie trat bei Behandlung mit dem Bisphosphonat Zoledronsäure bei nicht wenigen Patientinnen (1,3 Prozent) auch schweres Vorhofflimmern auf, das bisher bei Bisphosphonaten nicht beobachtet worden war. Das Vorhofflimmern lag unter der für diese Altersgruppe zu erwartenden Rate und wurde in anderen Studien mit Zoledronsäure nicht beobachtet.[9]
Studien von 2011 zur Langzeitanwendung der Alendronsäure führten zu einem Hinweis im WHO Pharmaceuticals Newsletter in der Rubrik Safety of Medicines auf die Veröffentlichung des MHRA bezüglich möglicher atypischer Frakturen des Femurschafts (Corpus ossis femoris).[10] Atypische Frakturen des Femurs traten meist am proximalen Schaft auf und zeigen typische radiologische Merkmale. Sie können durch ein minimales Trauma ausgelöst werden, kommen jedoch auch ohne Trauma vor. Die Frakturen sind häufig bilateral und weisen eine schlechte Heilungstendenz auf.[11] Der Verdacht, dass Bisphosphonate langfristig den Knochenumbau stören und das Risiko für Frakturen deutlich erhöhen, wird durch eine neuere Studie erhärtet. Nach fünf Jahren Behandlung sei jedoch das Verhältnis von Nutzen zu Risiko immer noch günstig.[12] Aufgrund von epidemiologischen Hinweisen hat das CHMP bei der Europäischen Arzneimittelagentur EMA einen möglichen Zusammenhang von atypischen Femurfrakturen mit der Gabe von Bisphosphonaten auf Basis der vorhandenen Daten umfassend bewertet.[13]
Weitere mögliche Nebenwirkungen von Bisphosphonaten sind Verwirrtheit sowie optische, akustische und olfaktorische Halluzinationen.
Einzelnachweise
- R. Chapurlat: Current pharmacological treatment for fibrous dysplasia and perspectives for the future. In: Joint Bone Spine. Band 72, Nummer 3, 2005, S. 196–198, doi:10.1016/j.jbspin.2004.08.001.
- M. Gnant, B. Mlineritsch, W. Schippinger u. a.: Endocrine therapy plus zoledronic acid in premenopausal breast cancer. In: N Engl J Med. Band 360, Nummer 7, Februar 2009, S. 679–691, PMID 19213681.
- Heinz Lüllmann, Klaus Mohr, Lutz Hein: Pharmakologie und Toxikologie. Thieme, Stuttgart 2006, ISBN 978-3-13-368516-0, S. 262–264.
- R. Bartl, C. Bartl, R. Gradinger: Einsatz der Bisphosphonate in der Orthopädie und Unfallchirurgie. In: Der Orthopäde. Band 37, Nr. 6, Juni 2008, S. 595–614, doi:10.1007/s00132-008-1280-y.
- Bisphosphonates and osteonecrosis of the jaw. (PDF; 171 kB) EMA, 24. September 2009, abgerufen am 9. Juni 2017 (englisch).
- Robert E Marx: Pamidronate (Aredia) and zoledronate (Zometa) induced avascular necrosis of the jaws: a growing epidemic. In: Journal of Oral and Maxillofacial Surgery. Band 61, Nr. 9, September 2003, S. 1115–1117, doi:10.1016/S0278-2391(03)00720-1.
- Stefan Lachmann, Siegmar Reinert, Sebastian Hoefert: Thema mit großer Praxisrelevanz. Tübinger Bisphosphonat-Symposium. In: ZM. Band 102, Nr. 6A, 16. März 2012, S. 716–720 (online).
- Catherine H. Van Poznak, Joseph M. Unger u. a.: Association of Osteonecrosis of the Jaw With Zoledronic Acid Treatment for Bone Metastases in Patients With Cancer. In: JAMA Oncology., doi:10.1001/jamaoncol.2020.6353.
- Ergebnis der randomisierten HORIZON-Studie: Once-Yearly Zoledronic Acid for Treatment of Postmenopausal Osteoporosis. In: New England Journal of Medicine. Band 356, 2007, S. 1809–1822, doi:10.1056/NEJMoa067312. Hier zitiert nach: Deutsches Ärzteblatt. 3. Mai 2007 (online).
- Bisphosphonates: atypical femoral fractures. In: Drug Safety Update. Band 4, Nr. 11, Juni 2011 (online).
- E. Shane, D. Burr, P. R. Ebeling u. a.: Atypical subtrochanteric and diaphyseal femoral fractures: report of a task force of the American Society for Bone and Mineral Research. In: J Bone Miner Res. Band 25, Nr. 11, 2010, S. 2267–2294, doi:10.1002/jbmr.253.
- Laura Y. Park-Wyllie, Muhammad M. Mamdani, David N. Juurlink, et al.: Bisphosphonate Use and the Risk of Subtrochanteric or Femoral Shaft Fractures in Older Women. In: JAMA. Band 305, Nr. 8, Februar 2011, doi:10.1001/jama.2011.190.
- European Medicines Agency concludes class review of bisphosphonates and atypical fractures. EMA, 15. April 2011, abgerufen am 9. Juni 2017 (englisch).