Benzoesäurebenzylester
Benzoesäurebenzylester ist eine chemische Verbindung aus der Gruppe der Ester der Benzoesäure.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
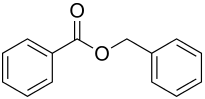 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Benzoesäurebenzylester | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C14H12O2 | |||||||||||||||||||||
| Kurzbeschreibung |
bei Temperaturen über 20 °C farblose Flüssigkeit mit schwach aromatischem Geruch; unter 20 °C Nadeln oder Blättchen[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 212,24 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||||||||
| Dichte |
1,12 g·cm−3[2] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
323 °C[2] | |||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||
Vorkommen

Benzoesäurebenzylester kommt natürlich in einigen Pflanzen (z. B. dem Perubalsam, Tolubalsam und der Rinde des Zimtbaumes) vor.[5]
Gewinnung und Darstellung
Benzoesäurebenzylester kann durch eine Kondensationsreaktion von Benzoesäure und Benzylalkohol gewonnen werden. Es kann auch durch eine Claisen-Tiščenko-Reaktion aus Benzaldehyd dargestellt werden.[6]
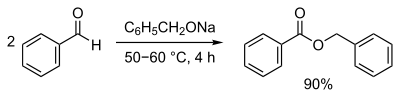
Eigenschaften
Benzoesäurebenzylester wird im Körper rasch zu Benzoesäure und Benzylalkohol hydrolysiert.[7] Es besitzt eine Viskosität von 10,9 mPa·s bei 25 °C.[8] Der Flammpunkt liegt bei 148 °C, die Zündtemperatur bei 480 °C.[2]
Verwendung
Benzoesäurebenzylester wird als Synthesechemikalie verwendet.[2] Es wird auch in der Medizin gegen Milben (z. B. bei Krätze), in der Parfum-, Kosmetik- und Lebensmittelindustrie zum Desinfizieren und Konservieren eingesetzt.[3] In der Parfümerie dient es als Lösungsmittel und Fixateur für Riechstoffe, in der Fototechnik als Campher-Ersatz in Celluloid und in der Chemie als Lösungsmittel (z. B. für Cellulosederivate). In der Lebensmittelindustrie dient es als Hilfsstoff und Zusatz zu Kaugummiaromen.[9]
Sicherheitshinweise
Benzylbenzoat hat lokale Reizwirkung auf Haut und Schleimhäute.[10]
Weblinks
- Vergleichsstudie der WHO zwischen Benzylbenzoat und Ivermectin bei Krätze (PDF; 546 kB, englisch)
Einzelnachweise
- Eintrag zu BENZYL BENZOATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 12. Mai 2020.
- Eintrag zu Benzylbenzoat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- Benzylbenzoat (Allum)
- Eintrag zu Benzyl benzoate im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- Eberhard Postel: Benzylbenzoat, ein Bestandteil des Perubalsams, in: Klinische Wochenschrift, Volume 22, Numbers 20–21 / Mai 1943, S. 362–364. doi:10.1007/BF01783698.
- Kamm, O.; Kamm, W. F.: Benzyl benzoate In: Organic Syntheses. 2, 1922, S. 5, doi:10.15227/orgsyn.002.0005; Coll. Vol. 1, 1941, S. 104 (PDF).
- Benzylbenzoat (embryotox) (Memento vom 26. November 2010 im Internet Archive).
- Datenblatt Benzoesäurebenzylester bei Merck, abgerufen am 14. März 2010.
- Benzoesäurebenzylester (Benzylbenzoat) FCC (Memento vom 7. November 2017 im Internet Archive).
- Eintrag zu Benzylbenzoat bei Vetpharm, abgerufen am 22. November 2011.

