Ascoviridae
Die Ascoviridae sind eine Familie von Viren mit der Typusgattung Ascovirus, die dem Phylum der Nucleocytoviricota (veraltet Nucleocytoplasmic large DNA viruses, NCLDV; frühere Vorschläge hatten auf Nucleocytoplasmaviricota bzw. – im Rang einer Ordnung – Megavirales gelautet) zugerechnet wird.[1] Es handelt sich um behüllte Viren mit einer doppelsträngigen, zirkulären DNA als Genom, die bislang ausschließlich bei Insekten der Ordnung Schmetterlinge (Lepidoptera) zu finden sind. Der Name der Familie leitet sich ab von griechisch ασκός ‚Schlauch, Säckchen‘, was auf die für die Ascoviren typische Abschnürung von virushaltigen Membranbläschen bei infizierten Zellen hindeutet. Die erste Virusspezies der Familie wurde 1983 entdeckt.[3]
| Ascoviridae | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

Schemazeichnung Ascovirus- | ||||||||||||||
| Systematik | ||||||||||||||
| ||||||||||||||
| Taxonomische Merkmale | ||||||||||||||
| ||||||||||||||
| Wissenschaftlicher Name | ||||||||||||||
| Ascoviridae | ||||||||||||||
| Links | ||||||||||||||
|
Mehrere Studien unterstützen seit dem Jahr 2000 die Annahme, dass die Ascoviridae sich aus den Iridoviridae entwickelt haben.[4][5][6][7][8]
Morphologie
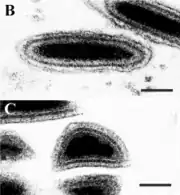
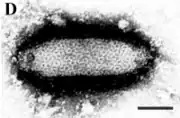
Die behüllten Virionen der Ascoviridae haben eine unregelmäßige, längliche, ovale Form mit einem Durchmesser von etwa 130 nm und einer Länge von 200–400 nm. Sie bestehen aus einer Virushülle mit einer netzartig geformten Oberfläche und einer inneren Partikelstruktur. Dieses innere Partikel wird von einem Kapsid mit komplexer Symmetrie und einer darum herumgelegten, inneren Lipidmembran gebildet. Diese zweite innere Membran erinnert an den Aufbau der Poxviridae, mit denen die Ascoviren aber sonst keine Sequenzähnlichkeiten teilen.
Genom und Vermehrung
Das zirkuläre Genom der bisher sequenzierten Ascoviren ist zwischen 120 und 180 kBp groß (z. B. SfAV-1a: 156.922 bp und DpTV – früher DpAV-4a: 119.343 bp[9][10]); damit gehören sie zusammen mit den Herpesvirales und Poxviridae zu den größten Viren. Aus den noch nicht ganz aufgeklärten Offenen Leserahmen des Genoms leiten sich mindestens 15 Polyproteine ab. Die Vermehrung des Genoms und der Zusammenbau des Kapsids geschieht im Zellkern der Insektenzelle, wobei dieser aufquillt und die Kernmembran zerreißt. Es kommt zur Bildung von typischen Membranfalten und vielfachen Abschnürungen im Inneren der Zelle. Die zuerst gebildeten Kapside werden mit einer de novo gebildeten Lipidmembran umkleidet und dieses innere Partikel wird durch eine Knospung an der Zellmembran mit der Virushülle umkleidet.
Das Genom von Diadromus pulchellus ascovirus 4a (DpTV) kodiert voraussichtlich 119 Proteine.[10]
Biologische Eigenschaften


Ascoviren infizieren die Larven von Schmetterlingen und Faltern überwiegend aus der Familie Noctuidae (Eulenfalter). Die Larven sterben bei einer chronischen Ascovirus-Infektion ab und sind zuvor in ihrer Entwicklung erheblich verlangsamt; die Vermehrung des Virus geschieht überwiegend im Fettgewebe der Raupen.[11] Die Ascoviren sind wahrscheinlich weltweit überall dort verbreitet, wo Eulenfalter-Arten anzutreffen sind.
Bisher wurden unterschiedliche Virusspezies aus Arten der Familie Noctuidae isoliert, und zwar bei Spodoptera frugiperda, Trichoplusia ni, Heliothis virescens, Helicoverpa spp. und Autographa precationis. Eine Infektion ist auch bei der Lauchmotte Acrolepiopsis assectella (Familie Yponomeutidae) beschrieben. Die Virusspezies TnAV-2a und HvAV-3a sind bei mehreren Falterarten zu finden und können sich experimentell in Insektenzellen aus sehr vielen Spezies der Familie Noctuidae vermehren. Die Vermehrung des SfAV-1a ist strikt auf die Spezies Spodoptera frugiperda beschränkt.
Die Übertragung der Viren geschieht durch parasitische Schlupf- und Brackwespen (Ichneumonoidea: Familien Ichneumonidae und Braconidae), deren Eiablage-Apparat (Ovipositor) bei der Eiablage in infizierten Raupen kontaminiert wird. Bei erneuter Eiablage in anderen Raupen kann das Virus weiter verbreitet werden. Bei einer Wespenart (Diadromus pulchellus) liegt das Genom des Ascovirus DpTV-4a in nicht-integrierter Form in den Zellkernen vor, so dass auch innerhalb der übertragenden (aber nicht erkrankten) Wespenpopulation das Virus schon auf die Wespeneier übertragen wird.[12]
Systematik
Innere Systematik
Die Systematik der Ascoviridae nach International Committee on Taxonomy of Viruses (ICTV), Stand 4. April 2024 ist wie folgt:[13][14]
Familie Ascoviridae
- Gattung Ascovirus
- Spezies Ascovirus hvav3a mit
- Heliothis virescens ascovirus 3a (HvAV-3a, Referenz oder „Exemplar“)
- Heliothis virescens ascovirus 3f (HvAV-3f)
- Heliothis virescens ascovirus 3g (HvAV-3g)
- Spezies Ascovirus sfav1a mit
- Spodoptera frugiperda ascovirus 1a (SfV, SfAV-1a und SfAV-1b)
- Spezies Ascovirus tnav2a mit
- Trichoplusia ni ascovirus 2a (TnV oder TnAV-2a, inkl. TnAV-6a[A. 1])
- Spezies „Heliothis virescens ascovirus 3i“ (HvAV-3i)
- Spezies „Spodoptera exigua ascovirus 5a“
- Spezies „Spodoptera frugiperda ascovirus 1c“ (SfAv-1c)
- Spezies „Spodoptera frugiperda ascovirus 1d“ (SfAv-1d)
- Spezies „Trichoplusia ni ascovirus 2b“ (TnAV-2b)
- Spezies „Trichoplusia ni ascovirus 2c“ (TnAV-2c)
- Spezies „Trichoplusia ni ascovirus 2d“ (TnAV-2d)
- Spezies „Trichoplusia ni ascovirus 6b“ (TnAV-6b)
- Spezies Ascovirus hvav3a mit
- Gattung Toursvirus (abgetrennt von Gattung Ascovirus
- Spezies Toursvirus dptv1a mit
- Diadromus pulchellus toursvirus (DpTV, DpTV-1a, früher Diadromus-pulchellus-Ascovirus 4a, DpAV-4a)
- Spezies „ Dasineura jujubifolia toursvirus 2a“
- Spezies „Diabrotica toursvirus 3a“
- Spezies Toursvirus dptv1a mit
- ohne Gattungszuweisung
Für die genauen Verwandtschaftsbeziehungen innerhalb der Familie Ascoviridae schlägt das ICTV folgendes Kladogramm vor:[15]
| Ascoviridae |
| ||||||||||||||||||
Äußere Systematik
Aufgrund von Sequenzuntersuchungen ist anzunehmen, dass die Ascoviridae und die morphologisch doch sehr abweichenden Iridoviridae einen gemeinsamen Vorfahren teilen.
Einen Kladogramm der Asco- und Iridiviridae findet man beim ICTV,[15] und in Fenner’s Veterinary Virology (Fifth Edition) 2017[18] Danach sind die Iridoviridae eine Schwestergruppe der Gattung Toursvirus (mit DpTV alias DpAV), während die Gattung Ascovirus eine basale Stellung in der gemeinsamen Klade einnimmt. Nach Andreani et al. (2018) sind umgekehrt die Ascoviridae eine Schwestergruppe der Alphairidovirinae, während hier die Betairidovirinae basal in der gemeinsamen Klade stehen.[19] Diese Ansicht wird auch durch Rolland et al. (2019) unterstützt. Neben den Unterfamilien der Iridoviridae erscheinen die Ascoviridae vom Rang einer Unterfamilie innerhalb einer gemeinsamen Familie Irido-Ascoviridae.[20]
Weiter wird vermutet, dass sich aus den Ascoviridae die Gattung Ichnovirus (Familie Polydnaviridae) entwickelt hat.[6]
Literatur
- B. A. Federici et al.: Family Ascoviridae, Genus Ascovirus. In: C. M. Fauquet, M. A. Mayo et al: Eighth Report of the International Committee on Taxonomy of Viruses. London / San Diego 2004, 2. 269–274
- David M. Knipe, Peter M. Howley et al. (Hrsg.): Fields’ Virology. 4. Auflage. Philadelphia 2001.
Weblinks
- Ascoviren in der TEM-Abbildung
- Ascoviridae in der Datenbank des ICTV
- Referenzsequenzen einiger Ascoviren
- Ascoviridae. Viralzone
Einzelnachweise
- ICTV: ICTV Taxonomy history: Spodoptera frugiperda ascovirus 1a, EC 51, Berlin, Germany, Ju<niwiki>ly 2019; Email ratification March 2020 (MSL #35)
- Eugene V. Koonin, Natalya Yutin: Evolution of the Large Nucleocytoplasmatic DNA Viruses of Eukaryotes and Convergent Origins of Viral Gigantism, in: Advances in Virus Research, Band 103, AP 21. Januar 2019, doi:10.1016/bs.aivir.2018.09.002, S. 167–202. Als Ovoid werden eiförmige dreidimensionale Körper bezeichnet.
- B. A. Federici: Enveloped double-stranded DNA insect virus with novel structure and cytopathology. In: PNAS. 80, 24, 1983, S. 7664–7668. PMID 16593397
- K. Stasiak, M. V. Demattei, B. A. Federici, Y. Bigot: Phylogenetic position of the Diadromus pulchellus ascovirus DNA polymerase among viruses with large double-stranded DNA genomes. In: The Journal of General Virology. Band 81, Pt 12, Dezember 2000, S. 3059–3072, doi:10.1099/0022-1317-81-12-3059, PMID 11086137.
- K. Stasiak, S. Renault, M. V. Demattei, Y. Bigot, B. A. Federici: Evidence for the evolution of ascoviruses from iridoviruses. In: The Journal of General Virology. Band 84, Pt 11, November 2003, S. 2999–3009, doi:10.1099/vir.0.19290-0, PMID 14573805.
- B. A. Federici, D. K. Bideshi, Y. Tan, T. Spears, Y. Bigot: Ascoviruses: superb manipulators of apoptosis for viral replication and transmission. In: Current Topics in Microbiology and Immunology. Band 328, 2009, ISBN 978-3-540-68617-0, S. 171–196, doi:10.1007/978-3-540-68618-7_5, PMID 19216438.
- B. Piégu, S. Asgari, D. Bideshi, B. A. Federici, Y. Bigot: Evolutionary relationships of iridoviruses and divergence of ascoviruses from invertebrate iridoviruses in the superfamily Megavirales. In: Molecular Phylogenetics and Evolution. Band 84, März 2015, S. 44–52, doi:10.1016/j.ympev.2014.12.013, PMID 25562178.
- V. G. Chinchar, T. Waltzek, K. Subramaniam, V. G. Faria, D. Ebert, J. Jancovich, P. Hick, Q.-Y. Zhang, R. Marschang, R. Whittington, T. Williams, I. A. Ince, H. Jie: 2020.018D.R.Betairidovirinae_1ngen_1nsp.zip (docx, xlsx), ICTV Proposal 2020.018D.R.Betairidovirinae_1ngen_1nsp (accepted). Hier: Fig. 2 im Word-Docx
- NCBI Taxonomy Browser: Toursvirus dptv1a, Nucleotide: Complete DpAV4 genome.
- Disa Bäckström, Natalya Yutin, Steffen L. Jørgensen, Jennah Dharamshi, Felix Homa, Katarzyna Zaremba-Niedwiedzka, Anja Spang, Yuri I. Wolf, Eugene V. Koonin, Thijs J. G. Ettema: Virus Genomes from Deep Sea Sediments Expand the Ocean Megavirome and Support Independent Origins of Viral Gigantism. In: mBio, Band 10, Nr. 2, März–April 2019, S. e02497-18; doi:10.1128/mBio.02497-18, PMID 30837339, PMC 6401483 (freier Volltext), ResearchGate:331531846 (englisch).
- R. Govindarajan, B. A. Federici: Ascovirus infectivity and effects of infection on the growth and development of noctuid larvae. In: J. Invertebr. Pathology, Band 56, Nr. 3, 1990, S. 291–299; PMID 2250099 (englisch).
- Y. Bigot, A. Rabouille et al.: Biological and molecular features of the relationships between Diadromus pulchellus ascovirus, a parasitoid hymenopteran wasp (Diadromus pulchellus) and its lepidopteran host, Acrolepiopsis assectella. In: J. Gen. Virol. 78, 5, 1997, S. 1149–1163. PMID 9152436
- ICTV: Taxonomy Browser.
- ICTV: Virus Metadata Resource (VMR).
- Sassan Asgari, Dennis K. Bideshi, Yves Bigot, Brian A. Federici, Xiao-Wen Cheng; ICTV Report Consortium: Ascoviridae, auf: ICTV online, Dezember 2016 (hier: Fig. 2)
- NCBI Nucleotide: Trichoplusia ni ascovirus 2a … LOCUS: AY197700.
- Padhoe: Famili(e) Ascoviridae, 15. Oktober 2011
- Fenner’s Veterinary Virology (Fifth Edition): Chapter 8 - Asfarviridae and Iridoviridae, online 4. November 2016, S. 175–188, doi:10.1016/B978-0-12-800946-8.00008-8 (hier: Fig. 1)
- Julien Andreani, Jacques Y. B. Khalil, Emeline Baptiste, Issam Hasni, Caroline Michelle, Didier Raoult, Anthony Levasseur, Bernard La Scola: Orpheovirus IHUMI-LCC2: A New Virus among the Giant Viruses, in: Front. Microbiol., 22. Januar 2018, doi:10.3389/fmicb.2017.02643
- Clara Rolland, Julien Andreani, Amina Cherif Louazani, Sarah Aherfi, Rania Francis, Rodrigo Rodrigues, Ludmila Santos Silva, Dehia Sahmi, Said Mougari, Nisrine Chelkha, Meriem Bekliz, Lorena Silva, Felipe Assis, Fábio Dornas, Jacques Yaacoub Bou Khalil, Isabelle Pagnier, Christelle Desnues, Anthony Levasseur, Philippe Colson, Jônatas Abrahão, Bernard La Scola: Discovery and Further Studies on Giant Viruses at the IHU Mediterranee Infection That Modified the Perception of the Virosphere. In: Viruses, 11(4), März/April 2019, pii: E312, doi:10.3390/v11040312, PMC 6520786 (freier Volltext), PMID 30935049, Fig. 2