Alkandiole
Die Alkandiole, zusammengesetzt aus Alkan und Diol, bilden eine Stoffgruppe, die aus geradlinigen oder verzweigten Kohlenwasserstoffketten bestehen, die an unterschiedlichen Stellen genau zwei Hydroxygruppen enthalten. Sie enthalten keine anderen Heteroatome oder Mehrfachbindungen.
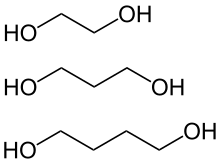
Gemäß der Erlenmeyer-Regel sind dabei in der Regel beide Hydroxygruppen an verschiedene Kohlenstoffatome gebunden, da Verbindungen mit zwei Hydroxygruppen an einem Kohlenstoffatom in der Regel eine geringe Stabilität besitzen.
Beispiele zweiwertige Alkohole
| Alkandiole | ||||||||
|---|---|---|---|---|---|---|---|---|
| Anzahl der C-Atome |
Summenformel | Molare Masse in g·mol−1 |
Systematischer Name | Trivialname | Schmelzpunkt in °C |
Siedetemperatur in °C |
Dichte in g·cm−3 |
Löslichkeit in Wasser in g·l−1 |
| 2 | C2H6O2 | 62,1 | Ethan-1,2-diol | Ethylenglycol, 1,2-Glycol |
−16[1] | 197[1] | 1,11 (20 °C)[1] | ∞[1] |
| 3 | C3H8O2 | 76 | Propan-1,2-diol | Propylenglycol | −60[2] | 188[2] | 1,04 (20 °C)[2] | ∞[2] |
| Propan-1,3-diol | Trimethylenglycol | −26[3] | 213[3] | 1,05 (20 °C)[3] | ∞[3] | |||
| 4 | C4H10O2 | 90 | Butan-1,2-diol | 1,2-Butylenglycol | −114[4] | 192[4] | 1,01 (20 °C)[4] | ∞[4] |
| Butan-1,3-diol | 1,3-Butylenglycol | < −50[5] | 207[5] | 1,01 (20 °C)[5] | ∞[5] | |||
| Butan-1,4-diol | Tetramethylenglycol | 20[6] | 230[6] | 1,02 (20 °C)[6] | ∞[6] | |||
| Butan-2,3-diol | 2,3-Butylenglycol | 19[7] | 180[7] | 1,01 (20 °C)[7] | ∞[7] | |||
| 5 | C5H12O2 | 104 | Pentan-1,2-diol | 1,2-Pentylenglycol | < −40[8] | 206[8] | 0,97 (20 °C)[8] | ∞[8] |
| Pentan-1,5-diol | Pentamethylenglycol | −16[9] | 242[9] | 0,99 (20 °C)[9] | ∞[9] | |||
| 6 | C6H14O2 | 118 | Hexan-1,2-diol | 1,2-Hexylenglycol | 2[10] | 223–224[10] | 0,95 (20 °C)[10] | ∞[10] |
| Hexan-1,6-diol | Hexamethylenglycol | 40–45[11][12] | 250[12][11] | 0,96 (20 °C)[12] | 1000[11] | |||
| 7 | C7H16O2 | 132 | Heptan-1,7-diol | Heptamethylenglycol | 17–19[13] | 259[13] | 0,95[13] | |
| 8 | C8H18O2 | 146 | Octan-1,2-diol | 1,2-Octylenglycol | 30[14] | 131 (10 Torr)[14] | ||
| Octan-1,8-diol | Octamethylenglycol | 63[15] | 274[15] | 0,91 (63 °C)[15] | ||||
| 2-Ethylhexan-1,3-diol | Ethylhexylenglycol | −40[16] | 243[16] | 0,94 (20 °C)[16] | 42[16] | |||
| 9 | C9H20O2 | 160 | Nonan-1,9-diol | Nonamethylenglycol | 45–48[17] | 288[17] | 0,95[17] | 9[17] |
| 10 | C10H22O2 | 174 | Decan-1,10-diol | Decamethylenglycol | 72–75[18] | 297[18] | 0,89 (80 °C)[18] | |
| 12 | C12H26O2 | 202 | Dodecan-1,2-diol | Laurylglycol | 58–60[19] | < 0,01[19] | ||
Eigenschaften
Schmelzpunkte
Die Schmelzpunkte der Reihe der linearen 1,2-Alkandiole zeigen eine intessante Anomalie. Sie sinken zunächst vom Ethan-1,2-diol zum Butan-1,2-diol, bevor sie dann mit steigendem Molekulargewicht wieder ansteigen. Die Schmelzpunkte der Reihe der linearen 1,n-Alkandiole (mit zwei endständigen Hydroxygruppen), zeigen einen generell steigenden Verlauf, wobei aber die Schmelzpunkte der 1,n-Alkandiole mit ungerader Kohlenstoffanzahl in der Kette jeweils geringer sind, als die Schmelzpunkte der benachbarten Alkandiole mit einer geraden Anzahl an Kohlenstoffatomen.
Herstellung und Verwendung
Für die Herstellung der Alkandiole sind verschiedene Synthesewege möglich. 1,4-Butandiol lässt sich durch die Reaktion von Formaldehyd und Ethin herstellen, wobei das im ersten Schritt entstehende 1,4-Butindiol hydriert wird. Eine weitere Darstellungsmöglichkeit ist die Hydroformylierung des Allylalkohols zum 4-Hydroxybutanal. Unter Hydrierung der Aldehydfunktion lässt sich das Alkandiol gewinnen. Die Oxidation von Butan zum Maleinsäureanhydrid unter anschließender Hydrolyse und Hydrierung ist ein weiterer Herstellungsweg.[20] Die Alkandiole werden unter anderem für die Herstellung von Polyestern oder Polyurethanen verwendet.
Einzelnachweise
- Eintrag zu Ethylenglykol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Oktober 2021. (JavaScript erforderlich)
- Eintrag zu 1,2-Propandiol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Oktober 2021. (JavaScript erforderlich)
- Eintrag zu 1,3-Propandiol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Oktober 2021. (JavaScript erforderlich)
- Eintrag zu 1,2-Butandiol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Oktober 2021. (JavaScript erforderlich)
- Eintrag zu 1,3-Butandiol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Oktober 2021. (JavaScript erforderlich)
- Eintrag zu 1,4-Butandiol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Oktober 2021. (JavaScript erforderlich)
- Eintrag zu 2,3-Butandiol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Oktober 2021. (JavaScript erforderlich)
- Eintrag zu 1,2-Pentandiol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Oktober 2021. (JavaScript erforderlich)
- Eintrag zu 1,5-Pentandiol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Oktober 2021. (JavaScript erforderlich)
- Eintrag zu DL-1,2-Hexandiol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 27. Oktober 2021. (JavaScript erforderlich)
- Datenblatt 1,6-Hexandiol bei Merck, abgerufen am 26. Oktober 2021.
- Eintrag zu 1,6-Hexandiol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Oktober 2021. (JavaScript erforderlich)
- Datenblatt 1,7-Heptandiol, 95% bei Sigma-Aldrich, abgerufen am 26. Oktober 2021 (PDF).
- David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 87. Auflage. (Internet-Version: 2006–2007), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-402 – 3-402 (eingeschränkte Vorschau in der Google-Buchsuche).
- Eintrag zu 1,8-Octandiol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Oktober 2021. (JavaScript erforderlich)
- Eintrag zu 2-Ethylhexan-1,3-diol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Oktober 2021. (JavaScript erforderlich)
- Datenblatt 1,9-Nonanediol, 97% bei Alfa Aesar, abgerufen am 26. Oktober 2021 (Seite nicht mehr abrufbar).
- Datenblatt 1,10-Decandiol, 98% bei Sigma-Aldrich, abgerufen am 26. Oktober 2021 (PDF).
- Eintrag zu 1,2-Dodecandiol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 26. Oktober 2021. (JavaScript erforderlich)
- Manfred Baerns, Arno Behr, Axel Brehm, Jürgen Gmehling, Hanns Hofmann, Ulfert Onken, Albert Renken: Technische Chemie. Verlag Wiley-VCH, 2006, ISBN 3-527-31000-2, S. 590.