Alizarin-Aluminium-Calciumkomplex
Das Aluminium-Calciumkomplexsalz des Alizarins ist ein Vertreter der Krapplacke, die als traditionelle Farbmittel gelten.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
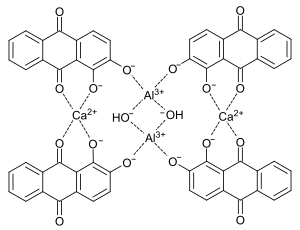 | |||||||||||||
| Allgemeines | |||||||||||||
| Name | Alizarin-Aluminium-Calciumkomplex | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | [(Al(OH)(C14H6O4)2Ca)2] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 1118,91 g/mol | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||
Es ist ein monometallischer Chelatkomplex, der aus Alizarinmolekülen als Liganden und Aluminium- und Calciumionen als Zentralteilchen durch Verlackung gebildet wird.
Der Strukturvorschlag von Kiel und Heertjes (1963).[2] wird von der heutigen Literatur noch oft übernommen oder variiert (z. B.[3][4][5]), war jedoch noch nicht mit Sicherheit geklärt[6] Neuere Untersuchungen haben gezeigt, dass diese bisherigen Modelle falsch waren. Im aktuellen Modell von Wunderlich und Bergerhoff[7] wird für das Molekül ein mehrkerniger, verbrückter Komplex vorgeschlagen, in dem zwei Aluminiumatome und zwei Calciumatome chelatartig von 4 Alizarinmolekülen komplexiert werden. Außerdem sind die Metallatome durch Oxobrücken miteinander verbunden. Da der Calcium-Aluminium-Komplex von Alizarin nicht elektrisch neutral ist, müssen noch zwei Protonen pro Molekül für den Ladungsausgleich in der Struktur vorhanden sein. Die Lage der Protonen im Komplex konnte bisher jedoch noch nicht bestimmt werden.
Verwendung

Umwelttechnisch lässt sich die Aluminium-Komplexierung durch Alizarin und seine Derivate nutzen, um gelöstes Aluminium (toxisch) in Trinkwasser einfach und kostengünstig nachzuweisen.[8]
Der Komplex ist ein traditionelles rotes Färberpigment, das im Einzelhandel unter der Bezeichnung „Alizarin Krapplack dunkel“ erhältlich ist.[9] Es wird vor allem als Künstlerfarbe und als Druckfarbe für Lebensmittelverpackungen verwendet.[3]
Einzelnachweise
- Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- E. G. Kiel, P. M. Heertjes: Metal complexes of alizarin. I. The structure of the calcium-aluminum lake of alizarin. In: J. Soc. Dyers Col. Band 79, 1963, S. 21–27.
- W. Herbst, K. Hunger: Industrial Organic Pigments. Production, Properties, Applications. 3. Auflage. Wiley-VCH, Weinheim 2004, ISBN 3-527-30576-9.
- V. Ya. Fain u. a.: Metal Complexes with Alizarin and Alizarin Red S: Electronic Absorption Spectra and Structure of Ligands. In: Russian Journal of Coordination Chemistry. Band 30, Nr. 5, 2004, S. 365–370.
- E. J. Tiedemann, Y. Yang: Fiber-save extraction of red mordant dyes from hair fibers. In: Journal of the American Institute of Conservation (JAIC). Band 34, Nr. 3, 1995, S. 195–206.
- H. Zollinger: Color Chemistry. Syntheses, Properties, and Applications of Organic Dyes and Pigments. 3. Auflage. VHCH, Zürich 2003, ISBN 3-906390-23-3, S. 255.
- C.-H. Wunderlich, G. Bergerhoff: Konstitution und Farbe von Alizarin- und Purpurin-Farblacken. In: Chemische Berichte. Band 127, 1994, S. 1185–1190.
- S. Bi, Z. Zhang: A.C. Oscillopolarographic determination of aluminum in natural and drinking waters using the adsorption of the Al(III)-1,2-Dihydroxyanthraquinone-3-sulfonic acid complex. In: Collect Czech Chem Commun. Band 61, 1996, S. 1745–1753, doi:10.1135/cccc19961745.
- Sicherheitsdatenblatt gemäß 2001/58/EC zu Alizarin Krapplack dunkel. Kremer Pigmente 2009.