4-Heptanol
4-Heptanol ist eine chemische Verbindung aus der Gruppe der Alkohole. Neben dem 4-Heptanol existieren weitere Isomere, zum Beispiel das 1-Heptanol, 2-Heptanol und 3-Heptanol. Es gibt insgesamt 39 Heptanole, die konstitutionsisomer zueinander sind.[4]
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
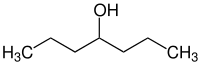 | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 4-Heptanol | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C7H16O | |||||||||||||||
| Kurzbeschreibung |
gelbliche Flüssigkeit[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 116,20 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig[1] | |||||||||||||||
| Dichte |
0,82 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
156 °C[1] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex |
1,4205 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Eigenschaften
4-Heptanol ist eine gelbliche entzündbare Flüssigkeit, die praktisch unlöslich in Wasser ist.[1]
Sicherheitshinweise
Die Dämpfe von 4-Heptanol können mit Luft ein explosionsfähiges Gemisch (Flammpunkt 54 °C, Zündtemperatur 295 °C) bilden.[1]
Einzelnachweise
- Eintrag zu CAS-Nr. 589-55-9 in der GESTIS-Stoffdatenbank des IFA, abgerufen am 19. Juni 2016. (JavaScript erforderlich)
- J. Buckingham: Dictionary of Organic Compounds. 1996, ISBN 0-412-54090-8, S. 3413 (eingeschränkte Vorschau in der Google-Buchsuche).
- William M. Haynes: CRC Handbook of Chemistry and Physics, 94th Edition. CRC Press, 2016, ISBN 978-1-4665-7115-0, S. 290 (eingeschränkte Vorschau in der Google-Buchsuche).
- Paul Niggli: Grundlagen der Stereochemie. Springer Basel, 1945, ISBN 978-3-0348-4039-2, S. 34 (eingeschränkte Vorschau in der Google-Buchsuche).
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.

