1,3-Dipolare Cycloaddition
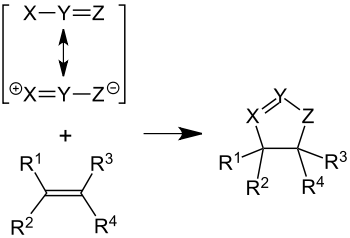
1,3-Dipolare Cycloaddition ist eine Bezeichnung für bestimmte chemische Reaktionen der organischen Chemie. Es handelt sich dabei um Cycloadditionen, bei denen ein 1,3-dipolares Molekül oder Fragment beteiligt ist.[1] Als mesomeriestabilisierter 1,3-Dipol werden dabei Ozon, Azide, Diazoalkane, Nitriloxide, Nitrilimine, Nitrone etc.[2] an Alkene oder Alkine addiert.[3] Die Atomökonomie der 1,3-dipolaren Cycloadditionen ist durchgängig hervorragend.
Ein Beispiel für eine 1,3-dipolare Cycloaddition ist die Huisgen-Reaktion. Diese Reaktion war bereits früher bekannt, jedoch konnte erst Rolf Huisgen den genauen Mechanismus anhand seiner systematischen Studien der 1,3-dipolaren Cycloaddition aufklären. Die Reaktion wird meist mit einem Azid sowie einem Alkin durchgeführt. Diese stellt, wenn sie unter Kupfer-Katalyse abläuft, den ersten und prominentesten Vertreter der sogenannten Click-Chemie dar, die CuAAC (copper-catalyzed azide-alkyne cycloaddition). Die Reaktion kann in wässriger Lösung bei Raumtemperatur durchgeführt werden. Sie wurde von den Nobelpreisträgern Barry Sharpless und Morten Meldal um 2000 unabhängig voneinander in die Click-Chemie eingeführt.
Eine doppelte 1,3-dipolare Cycloaddition ist die Ozonolyse: Hierbei wird erst der 1,3-Dipol Ozon und, nach dem Brechen der C-C- sowie einer O-O-Bindung, anschließend das 1,3-dipolare Carbonyloxid addiert.
Einzelnachweise
- Milton Orchin, Roger S. Macomber, Allan R. Pinhas, R. Marshall Wilson: The Vocabulary and Concepts of Organic Chemistry. 2. Auflage, John Wiley & Sons, Hoboken 2005, ISBN 0-471-68028-1, S. 583–584.
- Benoit Braida, Christof Walter, Bernd Engels, Philippe C. Hiberty: A Clear Correlation between the Diradical Character of 1,3-Dipoles and Their Reactivity toward Ethylene or Acetylene. In: Journal of the American Chemical Society. Band 132, Nr. 22, 9. Juni 2010, ISSN 0002-7863, S. 7631–7637, doi:10.1021/ja100512d.
- Ivan Ernest: Bindung, Struktur und Reaktionsmechanismen in der organischen Chemie, Springer-Verlag, 1972, ISBN 3-211-81060-9, S. 349–350.