1,2-Dibromcyclohexan
1,2-Dibromcyclohexan ist eine chemische Verbindung aus der Gruppe der Cyclohexanderivate.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
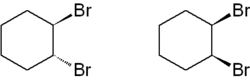 | |||||||||||||||||||
| cis- und trans-Dibromcyclohexan | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 1,2-Dibromcyclohexan | ||||||||||||||||||
| Summenformel | C6H10Br2 | ||||||||||||||||||
| Kurzbeschreibung |
farblose bis gelbliche Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 241,95 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1,79 °C (trans-Form)[1] | ||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Löslichkeit |
löslich in Ethanol, Diethylether, Aceton und Benzol[3] | ||||||||||||||||||
| Brechungsindex | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Gewinnung und Darstellung
1,2-Dibromcyclohexan kann durch Reaktion von Cyclohexen mit Brom gewonnen werden, wobei die trans-Form entsteht.[4][2]
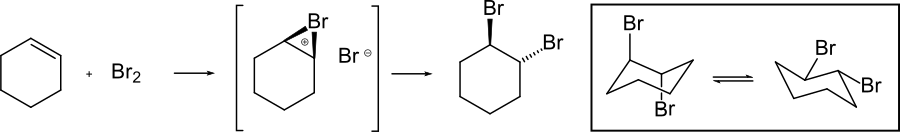 Reaktion von Cyclohexen mit Brom zu trans-1,2-Dibromcyclohexan (mit Konformationen)
Reaktion von Cyclohexen mit Brom zu trans-1,2-Dibromcyclohexan (mit Konformationen)
Die Addition von Bromwasserstoff an 1-Bromcyclohexen ist insofern regioselektiv, als sie nur cis-1,2-Dibromcyclohexan ergibt.[5]
Eigenschaften
(+/-)-trans-1,2-Dibromcyclohexan ist eine farblose bis gelbliche, klare Flüssigkeit.[1] Es gibt drei Stereoisomere von 1,2-Dibromcyclohexan, wobei die cis-Verbindung in zwei untereinander konvertierbaren Sesselkonformationen vorliegt. Sie liegt als racemisches Gemisch vor, und es ist unmöglich, seine optisch aktive Probe zu erhalten. trans-1,2-Dibromcyclohexan hat keine Symmetrieebene und liegt als Enantiomerenpaar vor.[6][7] Der Anteil der Konformere von trans-Dibromcyclohexan hängt vom Aggregatszustand und dem Lösungsmittel ab.[8]
cis-1,2-Dibromcyclohexan kann durch Reaktion mit Kaliumiodid in Methanol in Cyclohexen umgewandelt werden.[9]
Verwendung
1,2-Dibromcyclohexan kann zur Alkylierung von Dicarbonylverbindungen verwendet werden.[10]
Einzelnachweise
- Eintrag zu (±)-trans-1,2-Dibromocyclohexane, >95.0% bei TCI Europe, abgerufen am 30. September 2023.
- S. Coffey: Including the Official Reports of a Number of Learned Societies. Elsevier Science, ISBN 978-1-4832-2387-2, S. 33 (eingeschränkte Vorschau in der Google-Buchsuche).
- Richard Montgomery Stephenson, Stanisław Malanowski: Handbook of the Thermodynamics of Organic Compounds. Springer Netherlands, 2012, ISBN 978-94-009-3173-2, S. 191 (eingeschränkte Vorschau in der Google-Buchsuche).
- Janice Smith: Ebook: Organic Chemistry. McGraw-Hill Education, 2014, ISBN 978-0-07-717185-8, S. 408 (eingeschränkte Vorschau in der Google-Buchsuche).
- Michael B. Smith, Jerry March: March's Advanced Organic Chemistry. Wiley, 2007, ISBN 0-470-08494-4, S. 1011 (eingeschränkte Vorschau in der Google-Buchsuche).
- P.S. Kalsi: Stereochemistry & Mechanism Through solved Problems. New Age International, ISBN 978-81-224-1177-5, S. 93 (eingeschränkte Vorschau in der Google-Buchsuche).
- G. Kainz: Über eine spektroskopische Konformationsanalyse von trans-1,2-Dichlorcyclohexan bzw. trans-1,2-Dibromcyclohexan. In: Fresenius' Zeitschrift für analytische Chemie. Band 164, Nr. 3, 1958, S. 367–367, doi:10.1007/BF00455817.
- Metin Balcı: Reaction Mechanisms in Organic Chemistry. Wiley, 2021, ISBN 978-3-527-83459-4, S. 109 (eingeschränkte Vorschau in der Google-Buchsuche).
- Including the Official Reports of a Number of Learned Societies. Elsevier Science, ISBN 978-1-4832-2387-2, S. 35 (eingeschränkte Vorschau in der Google-Buchsuche).
- N. S. Sadykhov, Sh. S. Nasibov, F. M. Muradova, R. A. Gasymov: Alkylation of β-dicarbonyl compounds with 1,2-dibromocyclohexane. In: Russian Chemical Bulletin. Band 47, Nr. 2, 1998, S. 310–312, doi:10.1007/BF02498956.