δ-Aminolävulinatsynthase
Die δ-Aminolävulinatsynthase (δ-ALAS) ist ein mitochondriales Enzym, das sich in Hepatozyten und Erythroblasten findet. Es existieren zwei Isoenzyme, ein ubiquitär vorkommendes (Gen: ALAS1) und eines, das spezifisch für Erythroblasten (Gen: ALAS2) ist. Das Enzym katalysiert die Reaktion von Succinyl-CoA aus dem Citratzyklus mit der Aminosäure Glycin zu δ-Aminolävulinat unter Abspaltung von CO2. Diese Reaktion stellt den geschwindigkeitsbestimmenden Schritt der Häm-Biosynthese dar. Die Reaktion ist von Pyridoxalphosphat abhängig. Gehemmt wird die δ-Aminolävulinatsynthase durch Schwermetalle wie Blei und durch Häm selbst als Endprodukt des Häm-Biosyntheseweges.[1]
| 5-Aminolävulinatsynthase, unspezifische | ||
|---|---|---|
| ||
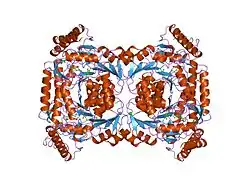
| Bändermodell (Tetramer) der ALAS von Rhodobacter, nach PDB 2BWN | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 584 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Homodimer | |
| Kofaktor | Pyridoxalphosphat | |
| Isoformen | 2 | |
| Bezeichner | ||
| Gen-Name | ALAS1 | |
| Externe IDs | ||
| Enzymklassifikation | ||
| EC, Kategorie | 2.3.1.37, Transferase | |
| Substrat | Succinyl-CoA + Glycin | |
| Produkte | 5-Aminolävulinat + CoA + CO2 | |
| Vorkommen | ||
| Übergeordnetes Taxon | Lebewesen | |
Ein Defekt des ALAS2-Gens führt zu einer (sehr seltenen) Chromosom X-gebundenen sideroblastischen Anämie. Dabei kommt es zu einer Eisenakkumulation in den Mitochondrien der Knochenmarkszellen.