ইউরেনিয়াম
টেমপ্লেট:Infobox uranium ইউরেনিয়াম একটি মৌলিক পদার্থ। এর রাসায়নিক প্রতীক U এবং পারমাণবিক সংখ্যা ৯২। এটি পর্যায় সারণীর অ্যাক্টিনাইড সিরিজের একটি রূপালী-ধূসর বর্ণের ধাতু। একটি ইউরেনিয়াম পরমাণুতে ৯২টি প্রোটন এবং ৯২টি ইলেকট্রন রয়েছে, এরমধ্যে ৬টি যোজ্যতা ইলেকট্রন। ইউরেনিয়াম দুর্বলভাবে তেজস্ক্রিয় কারণ ইউরেনিয়ামের সকল আইসোটোপ পরিবর্তনশীল; এর প্রাকৃতিকভাবে ঘটা আইসোটোপের অর্ধায়ু ১,৫৯,২০০ বছর থেকে ৪৫০ কোটি বছরের মধ্যে। প্রাকৃতিক ইউরেনিয়ামের সবচেয়ে সাধারণ আইসোটোপগুলি হল ইউরেনিয়াম-২৩৮ (যার মধ্যে ১৪৬ নিউট্রন রয়েছে এবং পৃথিবীর ইউরেনিয়ামের ৯৯% এর বেশি এই আইসোটোপ) এবং ইউরেনিয়াম-২৩৫ (যাতে ১৪৩ নিউট্রন রয়েছে)। প্রাথমিকভাবে উদ্ভূত পদার্থগুলির মধ্যে ইউরেনিয়ামের পারমাণবিক ওজন সবচেয়ে বেশি। এর ঘনত্ব সীসার তুলনায় প্রায় ৭০% বেশি এবং সোনা বা টাংস্টেনের তুলনায় কিছুটা কম। এটি প্রাকৃতিকভাবে মাটি, শিলা এবং পানিতে প্রতি মিলিয়নে কয়েক অংশের কম ঘনত্বে পাওয়া যায় এবং বাণিজ্যিকভাবে ইউরেনিয়াম-যুক্ত খনিজ যেমন ইউরেনাইট থেকে নিষ্কাষণ করা হয়।[1]
| |||||||||||||||||||||||||||||||||||||||||||
| সাধারণ বৈশিষ্ট্য | |||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| নাম, প্রতীক, পারমাণবিক সংখ্যা | ইউরেনিয়াম, U, ৯২ | ||||||||||||||||||||||||||||||||||||||||||
| রাসায়নিক শ্রেণী | অ্যাক্টিনাইড | ||||||||||||||||||||||||||||||||||||||||||
| Group, Period, Block | n/a, 7, f | ||||||||||||||||||||||||||||||||||||||||||
| Appearance | রূপালী ধূসর ধাতব;; বাতাসে বড় কালো অক্সাইড আবরণ ক্ষয়প্রাপ্ত হয়  | ||||||||||||||||||||||||||||||||||||||||||
| পারমাণবিক ভর | 238.02891(3) g/mol | ||||||||||||||||||||||||||||||||||||||||||
| ইলেক্ট্রন বিন্যাস | [Rn] 5f3 6d1 7s2 | ||||||||||||||||||||||||||||||||||||||||||
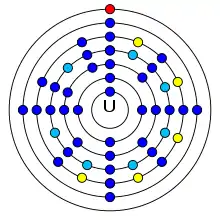
| প্রতি শক্তিস্তরে ইলেকট্রন সংখ্যা | 2, 8, 18, 32, 21, 9, 2 | ||||||||||||||||||||||||||||||||||||||||||
| ভৌত বৈশিষ্ট্য | |||||||||||||||||||||||||||||||||||||||||||
| দশা | solid | ||||||||||||||||||||||||||||||||||||||||||
| ঘনত্ব (সাধারণ তাপ ও চাপে) | 19.1 g/cm³ | ||||||||||||||||||||||||||||||||||||||||||
| গলনাংকে তরল ঘনত্ব | 17.3 গ্রাম/সেমি³ | ||||||||||||||||||||||||||||||||||||||||||
| গলনাঙ্ক | 1405.3 K (1132.2 °C, 2070 °F) | ||||||||||||||||||||||||||||||||||||||||||
| স্ফুটনাঙ্ক | 4404 K (4131 °C, 7468 °F) | ||||||||||||||||||||||||||||||||||||||||||
| গলনের লীন তাপ | 9.14 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||
| বাষ্পীভবনের লীন তাপ | 417.1 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||
| তাপধারণ ক্ষমতা | (২৫ °সে) 27.665 জুল/(মোল·কে) | ||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| পারমাণবিক বৈশিষ্ট্য | |||||||||||||||||||||||||||||||||||||||||||
| কেলাসীয় গঠন | orthorhombic | ||||||||||||||||||||||||||||||||||||||||||
| জারণ অবস্থা | 4, 6 (weakly basic oxide) | ||||||||||||||||||||||||||||||||||||||||||
| তড়িৎ ঋণাত্মকতা | 1.38 (পাউলিং স্কেল) | ||||||||||||||||||||||||||||||||||||||||||
| Ionization energies | 1st: 597.6 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||
| 2nd: 1420 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||
| পারমাণবিক ব্যাসার্ধ | 175 pm | ||||||||||||||||||||||||||||||||||||||||||
| Van der Waals radius | 186 pm | ||||||||||||||||||||||||||||||||||||||||||
| অন্যান্য বৈশিষ্ট্য | |||||||||||||||||||||||||||||||||||||||||||
| Magnetic ordering | paramagnetic | ||||||||||||||||||||||||||||||||||||||||||
| Electrical resistivity | (0 °C) 0.280 µΩ·m | ||||||||||||||||||||||||||||||||||||||||||
| তাপ পরিবাহিতা | (300 K) 27.5 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||
| Thermal expansion | (25 °C) 13.9 µm/(m·K) | ||||||||||||||||||||||||||||||||||||||||||
| Speed of sound (thin rod) | (20 °C) 3155 m/s | ||||||||||||||||||||||||||||||||||||||||||
| ইয়ং এর গুণাঙ্ক | 208 GPa | ||||||||||||||||||||||||||||||||||||||||||
| Shear modulus | 111 GPa | ||||||||||||||||||||||||||||||||||||||||||
| Bulk modulus | 100 GPa | ||||||||||||||||||||||||||||||||||||||||||
| Poisson ratio | 0.23 | ||||||||||||||||||||||||||||||||||||||||||
| Mohs hardness | 6.0 | ||||||||||||||||||||||||||||||||||||||||||
| Vickers hardness | 1960 MPa | ||||||||||||||||||||||||||||||||||||||||||
| Brinell hardness | 2400 MPa | ||||||||||||||||||||||||||||||||||||||||||
| সি এ এস নিবন্ধন সংখ্যা | 7440-61-1 | ||||||||||||||||||||||||||||||||||||||||||
| কয়েকটি উল্লেখযোগ্য সমস্থানিক | |||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||
| References | |||||||||||||||||||||||||||||||||||||||||||
ইউরেনিয়ামের অনন্য পারমাণবিক বৈশিষ্ট্যের কারণে এর অনেক সমকালীন ব্যবহার রয়েছে। ইউরেনিয়াম-২৩৫ হল একমাত্র প্রাকৃতিকভাবে প্রাপ্ত ফিসাইল আইসোটোপ যা পারমাণবিক বিদ্যুৎ কেন্দ্র এবং পারমাণবিক অস্ত্রে ব্যাপকভাবে ব্যবহৃত হয়। যাইহোক প্রকৃতিতে এটি খুবই কম পরিমাণে পাওয়ার কারণে ইউরেনিয়ামকে সমৃদ্ধকরণের মাধ্যমে পর্যাপ্ত পরিমানে ইউরেনিয়াম-২৩৫ আহরণ করা হয়। ইউরেনিয়াম-২৩৮ দ্রুত নিউট্রন দ্বারা বিদারণযোগ্য এবং এটি ফলপ্রসূ, যার অর্থ এটি একটি পারমাণবিক চুল্লীতে ফিসাইল প্লুটোনিয়াম-২৩৯-এ পরিবর্তিত হতে পারে। আরেকটি ফিসাইল আইসোটোপ হলো ইউরেনিয়াম-২৩৩, এটি প্রাকৃতিক থোরিয়াম থেকে উৎপাদন করা যেতে পারে এবং ভবিষ্যতে পারমাণবিক প্রযুক্তিতে শিল্প ব্যবহারের জন্য গভেষণা করা হচ্ছে।
ইউরেনিয়াম-২৩৮ এর স্বতঃস্ফূর্ত ফিশন বা এমনকি দ্রুত নিউট্রনের সাথে প্ররোচিত ফিশনের একটি ছোট সম্ভাবনা রয়েছে; ইউরেনিয়াম-২৩৫ এবং একটি কম মাত্রার ইউরেনিয়াম-২৩৩ ধীর নিউট্রনের জন্য অনেক বেশি ফিশন প্রস্থচ্ছেদ রয়েছে। পর্যাপ্ত ঘনত্বে এই আইসোটোপগুলি একটি স্থায়ী নিউক্লিয় শৃঙ্খল বিক্রিয়া বজায় রাখে। এটি পারমাণবিক শক্তি চুল্লিতে তাপ উৎপন্ন করে এবং পারমাণবিক অস্ত্রের জন্য ফিসাইল উপাদান তৈরি করে। ক্ষয়প্রাপ্ত ইউরেনিয়াম (২৩৮U) কাইনেটিক এনার্জি পেনেট্রেটর এবং আর্মার প্লেটিং এ ব্যবহৃত হয়।[2][3]
১৭৮৯ সালে খনিজ পিচব্লেন্ডে ইউরেনিয়াম আবিষ্কারের কৃতিত্ব মার্টিন হেনরিক ক্ল্যাপ্রোথকে দেওয়া হয়, তিনি সম্প্রতি আবিষ্কৃত গ্রহ ইউরেনাসের নামানুসারে নতুন উপাদানটির নামকরণ করেন। ইউজিন-মেলচিওর পেলিগট প্রথম ধাতুটিকে পৃথক করেন এবং ১৮৯৬ সালে হেনরি বেকারেল এর তেজস্ক্রিয় বৈশিষ্ট্য আবিষ্কার করেন। অটো হান, লিজে মাইটনার, এনরিকো ফের্মি এবং অন্যান্যদের গবেষণা, যেমন জে. রবার্ট ওপেনহাইমার ১৯৩৪ সালে শুরু করে পারমাণবিক শক্তি শিল্পে জ্বালানী হিসাবে এর ব্যবহার শুরু করেন এবং যুদ্ধে ব্যবহৃত প্রথম পারমাণবিক অস্ত্র লিটল বয় এ এর ব্যবহার করেন। মার্কিন যুক্তরাষ্ট্র এবং সোভিয়েত ইউনিয়নের মধ্যে স্নায়ুযুদ্ধ চলাকালীন সময় একটি পরবর্তী অস্ত্র প্রতিযোগিতার ফলে হাজার হাজার পারমাণবিক অস্ত্র তৈরি করে যাতে ইউরেনিয়াম ধাতু এবং ইউরেনিয়াম থেকে প্রাপ্ত প্লুটোনিয়াম-২৩৯ ব্যবহার করা হয়। বিভিন্ন পারমাণবিক নিরস্ত্রীকরণ কর্মসূচির মধ্যে এই অস্ত্র ও সংশ্লিষ্ট পারমাণবিক স্থাপনাগুলোকে ভেঙে ফেলা হয় এবং এর জন্য লক্ষ কোটি ডলার খরচ হয়। পারমাণবিক অস্ত্র থেকে প্রাপ্ত অস্ত্র-মানের ইউরেনিয়ামকে ইউরেনিয়াম-২৩৮ এ মিশ্রিত করা হয় এবং পারমাণবিক চুল্লির জন্য জ্বালানী হিসাবে পুনরায় ব্যবহার করা হয়। এই পারমাণবিক চুল্লীর উন্নয়ন এবং বিস্তার বিশ্বব্যাপী চলতে থাকে কারণ এগুলি কার্বন ডাই অক্সাইড (CO2)-মুক্ত শক্তির শক্তিশালী উৎস। ব্যয়িত পারমাণবিক জ্বালানী তেজস্ক্রিয় বর্জ্য গঠন করে যার বেশিরভাগই ইউরেনিয়াম-২৩৮ এবং তা উল্লেখযোগ্যভাবে স্বাস্থ্যের জন্য হুমকির সৃষ্টি করে।
বৈশিষ্ট্য

পরিশোধনের পর ইউরেনিয়াম রূপালী সাদা বর্ণের এবং দুর্বলভাবে তেজস্ক্রিয় ধাতু। এটির কাঠিন্য মাত্রা ৬, যা গ্লাস স্ক্র্যাচ করার জন্য যথেষ্ট এবং এটি টাইটানিয়াম, রোডিয়াম, ম্যাঙ্গানিজ এবং নিওবিয়ামের প্রায় সমান। এটি নমনীয়, প্রসারণীয়, সামান্য প্যারাচৌম্বক পদার্থ, শক্তিশালী ইলেক্ট্রোপজিটিভ এবং দুর্বল বৈদ্যুতিক পরিবাহী।[4][5] ইউরেনিয়াম ধাতুর ঘনত্ব ১৯.১ গ্রাম/ঘন সে.মি.,[6] এটি সীসার চেয়ে ঘন (১১.৩ গ্রাম/ঘন সে.মি.),[7] কিন্তু টাংস্টেন এবং সোনার (১৯.৩ গ্রাম/ঘন সে.মি.) থেকে সামান্য কম ঘনত্বের পদার্থ।[8][9]
আইসোটোপ
ইউরেনিয়ামের দুইটি আইসোটোপ আছে ৷ যথাঃ
১# ইউরেনিয়াম ২৩৫ ২# ইউরেনিয়াম ২৩৮
আরও দেখুন
তথ্যসূত্র
- "Uranium"। Encyclopaedia Britannica। সংগ্রহের তারিখ ২২ এপ্রিল ২০১৭।
- Emsley 2001, পৃ. 479.
- Hammond, C. R. (২০০০)। The Elements, in Handbook of Chemistry and Physics (পিডিএফ) (81st সংস্করণ)। CRC press। আইএসবিএন 978-0-8493-0481-1।
- "Uranium"। Royal Society of Chemistry।
- "Lead"। Royal Society of Chemistry।
- "Tungsten"। Royal Society of Chemistry।
- "Gold"। Royal Society of Chemistry।
গ্রন্থসূত্র
- উচ্চ মাধ্যমিক রসায়ন প্রথম পত্র - প্রফেসর মো. মহির উদ্দিন, লায়লা মুসতারিন, ড. তানভীর মুসলিম, হাছিনা বেগম।
- উচ্চ মাধ্যমিক রসায়ন প্রথম পত্র - ড. সরোজ কান্তি সিংহ হাজারী, হারাধন নাগ।
