| Фазавыя пераходы |
|---|
|
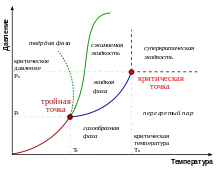
Крытычны пункт — спалучэнне значэнняў тэмпературы і ціску (ці, што эквівалентна, малярных аб'ёмаў ), пры якіх знікае адрозненне ва ўласцівасцях вадкай і газападобнай фаз рэчыва.
Крытычная тэмпература фазавага пераходу — значэнне тэмпературы ў крытычным пункце. Пры тэмпературы вышэй за крытычную газ немагчыма скандэнсаваць ні пры якім ціску.
Фізічнае значэнне
У крытычным пункце шчыльнасць вадкасці і яе насычанай пары становяцца роўныя, а павярхневае нацяжэнне вадкасці падае да нуля, таму знікае мяжа падзелу фаз вадкасць-пара.
Для сумесі рэчываў крытычная тэмпература не з'яўляецца пастаяннай велічынёй і можа быць прадстаўлена прасторавай крывой (якая залежыць ад прапорцыі складнікаў кампанентаў), крайнімі кропкамі якой з'яўляюцца крытычныя тэмпературы чыстых рэчываў — кампанентаў разгляданай сумесі.
Крытычнаму пункту на дыяграме стану рэчывы адпавядаюць гранічныя кропкі на крывых раўнавагі фаз, у ваколіцах пункту фазавая раўнавага парушаецца, адбываецца страта тэрмадынамічнай устойлівасці па шчыльнасці рэчыва. Па адзін бок ад крытычнага пункта рэчыва аднароднае (звычайна пры ), а па другі — падзяляецца на вадкасць і пару.
У наваколлі пункта назіраюцца крытычныя з'явы: з-за росту характарыстычных памераў флуктуацый шчыльнасці рэзка ўзмацняецца рассейванне святла пры праходжанні праз рэчыва — пры дасягненні памераў флуктуацый парадкаў соцень нанаметраў, г.зн. даўжынь хваль святла, рэчыва становіцца непразрыстым. Рост флуктуацый прыводзіць таксама да ўзмацнення паглынання гуку і росту яго дысперсіі, змены характару броўнаўскага руху, анамалій вязкасці, цеплаправоднасці, запаволення ўстанаўлення цеплавой раўнавагі і т. п.
Гісторыя
Практычна з'ява крытычнага пункта была выяўлена пры награванні вадкасці, якая часткова запаўняе запаяную трубку. Па меры нагрэву меніск паступова губляў сваю крывізну і станавіўся ўсё больш плоскім, а пры дасягненні крытычнай тэмпературы пераставаў быць бачным.
| Рэчыва | |||
|---|---|---|---|
| Адзінкі | Кельвіны | Атмасферы | см³/моль |
| Вадарод | 33,0 | 12,8 | 61,8 |
| Кісларод | 154,8 | 50,1 | 74,4 |
| Ртуць | 1750 | 1500 | 44 |
| Этанол | 516,3 | 63,0 | 167 |
| Дыяксід вугляроду | 304,2 | 72,9 | 94,0 |
| Вада | 647 | 218,3 | 56 |
| Азот | 126.25 | ||
| Аргон | 150.86 | ||
| Бром | 588 | ||
| Гелій | 5.19 | ||
| Ёд | 819 | ||
| Крыптон | 209.45 | ||
| Ксенон | 289.73 | ||
| Мыш’як | 1673 | ||
| Неон | 44.4 | ||
| Радон | 378 | ||
| Селен | 1766 | ||
| Сера | 1314 | ||
| Фосфар | 994 | ||
| Фтор | 144.3 | ||
| Хлор | 416.95 |
Крытычныя пункты існуюць не толькі для чыстых рэчываў, але і, у некаторых выпадках, для іх сумесей і вызначаюць параметры страты ўстойлівасці сумесі (з падзелам фаз) — раствор (адна фаза). Прыкладам такой сумесі можа служыць сумесь фенол-вада.