Etanolamin
Etanolamin- HO-CH2CH2-NH2 -
| Etanolamin | |
|---|---|
| Ümumi | |
| Kimyəvi formulu | C2H7NO |
| Molyar kütlə | 61,08q/mol q/mol |
| Fiziki xassələri | |
| Sıxlıq | 1,012 q/sm³ |
| Termik xüsusiyyətlər | |
| Ərimə nöqtəsi | 10,3 °C °S |
| Qaynama nöqtəsi | 170 °C °S |
| Öz-özünə yanma temperaturu | 450 °C |
| Buxarın təzyiqi | 0,4 ± 0,1 mm Hg[1] |
| Kimyəvi xassələri | |
| Turşunun dissosasiya sabiti | 9,5 ± 0,01[2] |
| Optik xüsusiyyətlər | |
| Sındırma əmsalı | 1,4539 |
| Təsnifatı | |
| CAS-da qeyd. nöm. | 141-43-5 |
| PubChem | 700 |
| RTECS | KJ5775000 |
| ChEBI | 16000 |
| ChemSpider | 13835336 |
(2-aminoetanol, trivial adı kolamin), sadə stabil aminospirtdir, birli amin və birli spirtdir.
Dietanolamin - (NH(CH2CH2OH)2)
və trietanolamin kimi (N(CH2CH2OH)3)
bu maddə də monoetanolamin adlandırılır.
Fiziki xassəlləri
Qatı yağvarı mayedir (T qayn. 170 oC), zəif amin iylidir, su ilə bütün nisbətlərdə qarışır. Etanol, benzol, xloroformda yaxşı həll olunur.
Alınması
Sənayedə etanolaminin alınması ammoniumun etilenoksidə birləşməsi ilə az miqdarda suyun iştirakıyla həyata keçirilir. Proses 1 mərhələlidir, 90-130 oc və 710 Mpa təzyiqdə aparılır. Nəticədə 78.3 % mono-, 16 % di- və 44% trietanolamin alınır.
Kimyəvi xassələri
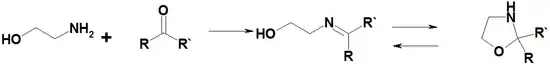
Etanolamin- zəif əsaslıdır. Mineral və güclü üzvi duzlarla duzlar əmələ gətirir. Mürəkkəb efirlər və karbon turşuları və ya anhidridlər və xloranhidridlərlə monoetanolamin N-(2-hidroksietil)amid duzlarına çevrilir. Monoetanolamin aldehidlərlə (formaldehid istisna olmaqla) və ketonlarla Şiff əsasini əmələ gətirir. Əsasən oksazolidinin izomerləri ilə tarazlıq yaradır:
Monoetanolaminin duzları KCN və ya NaCN ilə aldehid və ketonlarla N-(hidroksietil)aminonitrillər əmələ gətirir.
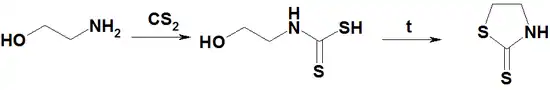
Monoetanolaminin CS2 ilə reaksiyasında N-(2-hidroksietil)ditiokarbamin turşusu alınır ki, bu da qızdırıldıqda merkaptotiazolin əmələ gətirir:
Moçevina ilə qızdırıldıqda etilenmoçevina əmələ gətirir:
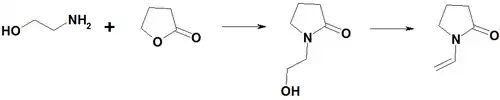
y-butirolaktonla, N-(2-hidroksietil)pirrolidon, sonra isə N-vinilpirrolidona çevrilir:
Monoetanolaminin H2 və (Ni və Cu)-un katalizator kimi iştirakı ilə ammonolizi etilendiaminin əmələ gəlməsinə gətirib çıxarır.
- ::

Tədbiqi
Etanolaminin sulu məhlulları qələvi reaksiyalıdır, turş qazları yaxşı udma qabiliyyətinə malikdir, buna görə də etanolaminin məhlullarından adsorbent kimi müxtəlif qaz təmizləmə proseslərində (məs. neftqaz və neftkimya sənayesində )kükürdün, karbon turşusu və tiolların udulması üçün, saç rənglərində isə ammonium əvəzedicisi kimi istifadə olunur. Etanolamin taurinin sintezində ilkin maddə kimi istifadə edilir.
Mənbə
- Кремлёв А. М., Менделеев Д. И.,. Этаноламин // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907
- http://www.cdc.gov/niosh/npg/npgd0256.html.
- Hall H. K. Correlation of the Base Strengths of Amines 1 (ing.). // J. Am. Chem. Soc. / P. J. Stang ACS, 1957. Vol. 79, Iss. 20. P. 5441–5444. ISSN 0002-7863; 1520-5126; 1943-2984 doi:10.1021/JA01577A030