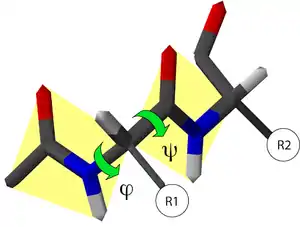
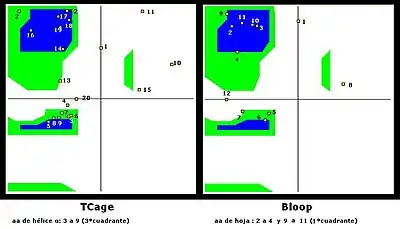
El gráficu (o diagrama) de Ramachandran foi creáu pol bioquímicu hindú Gopalasamudram Narayana Ramachandran xunto con Viswanathan Sasisekharan. Nél puédense visualizar toles combinaciones posibles d'ángulos diédricos Ψ (psi) contra Φ (phi) nos aminoácidos d'un polipéptido, y que contribúin a la conformanza de la estructura de les proteínes.[1] Esti gráficu dexa, poro, averar a priori cuál va ser la estructura secundaria del péptido, yá que esisten combinaciones d'ángulos típiques pa cada estructura (α- héliz y fueyaβ). La conformanza de los péptidos definir por aciu la asignación de valores pa cada par d'esquines Φi, Ψi pa cada aminoácidu. Nel segundu cuadrante tópense les combinaciones de la fueyaβ, nel tercer cuadrante tópense la héliz α derecha y los xiros o bucles (loops); nel primer cuadrante les combinaciones de la héliz α esquierda.
Matemáticamente, un gráficu de Ramachandran ye la visualización d'una función . El dominio d'esta función ye'l toru, polo que'l gráficu convencional de Ramachandran correspuende a una proyeición del toru sobre'l planu, resultando nuna vista aburuyada y na presencia de discontinuidaes.
El gráficu de Ramachandran diseñóse xusto primero que se determinaren les primeres estructures proteiques a resolución atómicu. Cuarenta años dempués había decenes de miles d'estructures de proteínes d'altu resolución, determinaes por cristalografía de rayos X, depositaes nel Protein Data Bank (PDB). D'un millar de distintes cadenes proteiques, llográronse gráficos de Ramachandran d'alredor de 200 000 aminoácidos, llográndose diferencies significatives especialmente pa la glicina (Hovmöller et al. 2002). Atopóse que la rexón cimera izquierda podía estremase en dos: una a la izquierda conteniendo aminoácidos n'hoja beta, y la otra a la derecha con aminoácidos en conformances de duviellos aleatorios.
Ángulos dexaos y prohibíos. Los casos especiales de la Glicina y Prolina
Non tolos pares d'ángulos son realmente posibles dientro de les estructures de los péptidos. Esto debe a los efeutos estéricos ente los residuos (cadenes llaterales) de los aminoácidos.
Nel casu de la glicina, les zones de posible conformanza de la tabla con una simetría central, y son muncho más amplies que les de los demás aminoácidos, por cuenta de que tien solo H como cadena llateral.
Otru casu especial ye la prolina, únicu aminoácidu capaz de tener enllaces CIS y TRANS.
Software
- Ramachandran plot 2.0
- Ferramienta basada en web para dibuxara'l gráficu de Ramachandran de cualquier entrada PDB
- STING
- Pymol cola estensión DynoPlot
- VMD, distribuyida con plugin pa gráficos de Ramachandran
- Sirius
- Swiss PDB Viewer
- TALOS
Ver tamién PDB pa una llista de software similar.
Referencies
- S. Hovmöller, T. Zhou & T. Ohlson (2002) Conformations of amino acids in proteins. In: Acta Cryst. vol. D58, p. 768-776.
Enllaces esternos
- Wiki de DynoPlot en PyMOL
- Enllaz a gráficos de Ramachandran de llocalizaciones de hélices alfa y hoja beta
- Enllaz a gráficos de Ramachandran calculaos sobre estructures de proteínes determinaes por cristalografía de rayos X, comparaos col Ramachan. orixinal
- Gráficu de Ramachandran en Proteopedia