ميضاع
الميضاع[1] (بالإنجليزية: Locant) في التسمية النظامية للمركبات العضوية هو مصطلح يشير إلى موضع المجموعة الوظيفية أو المستبدل داخل جزيء.[2]
ميضاعات الحروف الإغريقية
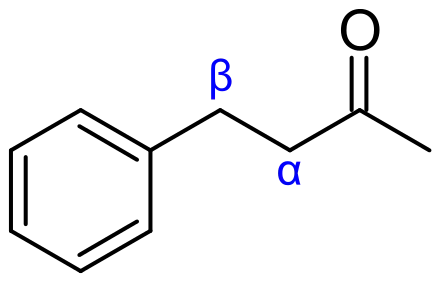
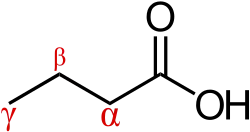
يستخدم نظام شائع آخر بادئات الحروف الإغريقية كميضاعات، وهو أمر مفيد في تحديد الموضع النسبي لذرات الكربون وكذلك ذرات الهيدروجين بالنسبة لمجموعات وظيفية أخرى.
يشير الكربون-α (الكربون-ألفا) إلى أول ذرة كربون مرتبطة بمجموعة وظيفية، مثل مجموعة الكربونيل (كما في الصورة). تسمى ذرة الكربون الثانية الكربون-β (الكربون-بيتا) والثالثة هي ذرة الكربون-γ (الكربون-غاما) ويستمر نظام التسمية بترتيب أبجدي.[3]
يمكن كذلك تطبيق نظام التسمية [الإنجليزية] هذا على ذرات الهيدروجين المرتبطة بذرات الكربون. تسمى ذرة الهيدروجين المرتبطة بـ بالكربون-ألفا "بالهيدروجين-α" (الهيدروجين-ألفا) وذرة الهيدروجين الموجودة على الكربون-بيتا "بالهيدروجين-β" (هيدروجين بيتا) وهكذا.
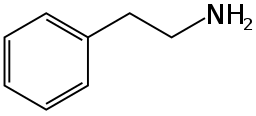
يمكن أن تكون الجزيئات العضوية التي تحتوي على أكثر من مجموعة وظيفية مصدر حيرة والتباس. بشكل عام، المجموعة الوظيفية المسؤولة عن اسم أو نوع الجزيء هي المجموعة "المرجعية" التي تسمى ذرات الكربون استنادا لها. على سبيل المثال جزيء النيتروسترين [الإنجليزية] وجزيء الفينيثيلامين متشابهان لحد كبير بحيث يمكن اختزال الأول إلى الأخير. ومع ذلك يختلفان في ذرة الكربون-ألفا، ففي جزيء النيتروسترين المجموعة المرجعية هي الفينيل وذرة الكربون-ألفا مجاورة لها أما في الفينيثيلامين فالمجموعة المرجعية هي الأمين وذرة الكربون-ألفا الخاصة بها هي نفسها هي ذرة الكربون-بيتا الخاصة بالنيتروسترين. تبدأ تسمية ذرات الكربون في الفينيثيلامين (كونه أمينًا وليس ستيرين) من مجموعة الأمين وذلك عكس النيتروسترين الذي تبدأ فيه التسمية من "الطرف" المقابل للجزيء.[4]
البروتينات والأحماض الأمينية
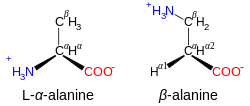
في الأحماض الأمينية المجموعة المرجعية هي مجموعة الكربوكسيل والكربون ألفا هو ذرة الكربون التي تليها. لذلك القراءة على طول العمود الفقري لبروتين نموذجي ستعطي التسلسل -(كربوكسيل-كربون ألفا(Cα)-مجوعة أمين (N))ن-. الكربون ألفا هو المكان الذي ترتبط فيه المستبدلات المختلفة (السلاسل الجانبية) بالحمض الأميني وهذه السلاسل الجانبية هي ما يميز كل حمض أميني عن غيره. تعطي هذه السلاسل الجانبية الكربون ألفا خصائصه المركزية الفراغية لكل حمض أميني باستثناء الغليسين. لذلك الكربون ألفا هو المركز الفراغي لكل حمض أميني باستثناء الغليسين. لا يحتوي الغليسين على كربون-بيتا بينما يفعل ذلك كل حمض أميني آخر.
الكربون ألفا الخاص بالحمض الأميني مهم في تطوي البروتين. عند وصف البروتين -وهو سلسلة من الأحماض الأمينية- غالبا ما يُقدَّر موقع كل حمض أميني بموقع الكربون ألفا الخاص به. بشكل عام، تكون المسافة بين كربونات ألفا الخاصة بأحماض أمينية مجاورة في بروتين حوالي 3.8 أنغستروم (380 بيكومتر).
مراجع
- محمد هيثم الخياط (2006). المعجم الطبي الموحد (بالعربية والإنجليزية) (ط. 4). بيروت: مكتبة لبنان ناشرون، منظمة الصحة العالمية. ص. 848. ISBN:978-9953-33-726-5. OCLC:192108789. QID:Q12193380.
- Nomenclature of Organic Chemistry. IUPAC Recommendations and Preferred Names 2013 (PDF). London: International Union of Pure and Applied Chemistry. ISBN:978-0-85404-182-4. مؤرشف من الأصل (PDF) في 2023-06-23. اطلع عليه بتاريخ 2022-12-14.
- Hackh's Chemical Dictionary. 1969. ص. 95.
- "Nomenclature". Ask Dr. Shulgin Online. مؤرشف من الأصل في 2022-10-22. اطلع عليه بتاريخ 2010-08-05.
- بوابة الكيمياء
- بوابة الكيمياء الحيوية
![نيتروسترين [الإنجليزية]](../I/Beta-nitrostyrene.svg.png.webp)