متلازمة لامبرت-إيتون
متلازمة لامبرت-إيتون الوهنية العضلية أو متلازمة لامبرت-إيتون (بالإنجليزية: Lambert-Eaton Myasthenic Syndrome) (LEMS) هي اضطراب مناعي ذاتي نادر يتميز بضعف عضلات الأطراف.
| متلازمة لامبرت-إيتون | |
|---|---|
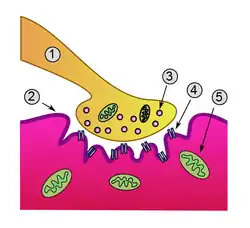 Detailed view of a neuromuscular junction: 1. مشبك كيميائي terminal 2. غمد الليف العضلي 3. حويصلة مشبكية 4. مُستَقبِِل أسيتيل كولين النيكوتين 5. ميتوكندريون Detailed view of a neuromuscular junction: 1. مشبك كيميائي terminal 2. غمد الليف العضلي 3. حويصلة مشبكية 4. مُستَقبِِل أسيتيل كولين النيكوتين 5. ميتوكندريون | |
| معلومات عامة | |
| الاختصاص | طب الجهاز العصبي |
| من أنواع | اعتلال القنوات، وتحلل مخيخي مصاحب للورم، ومرض مناعي ذاتي في الجهاز العصبي الطرفي ، ومرض |
يعاني نحو 60% من المصابين بمتلازمة لامبرت إيتون الوهنية العضلية من ورم خبيث أساسي، والأكثر شيوعًا هو سرطان الرئة ذو الخلايا الصغيرة. لذلك يعد متلازمة الأباعد الورمية (حالة تنشأ نتيجة السرطان في مكان آخر من الجسم). ويعد ذلك نتيجة الأجسام المضادة ضد قنوات الكالسيوم ذات الجهد الكهربي قبل المشبكي، ومن المحتمل أن تكون البروتينات الطرفية الأخرى للأعصاب، في الوصل العصبي العضلي (الاتصال بين الأعصاب والعضلة التي تمدها). عادة ما يؤكد التشخيص بواسطة تخطيط كهربية العضلات واختبارات الدم. تميزه هذه أيضًا عن الوهن العضلي الشديد، وهو مرض عصبي عضلي ذاتي متعلق بالمناعة.[1][2]
إذا كان المرض مرتبطًا بالسرطان، فإن العلاج المباشر للسرطان غالبًا ما يخفف من أعراض متلازمة لامبرت إيتون الوهنية العضلية. العلاجات الأخرى المستخدمة غالبًا هي الستيرويدات، والآزوثيوبرين، التي تثبط الجهاز المناعي، والغلوبولين المناعي الوريدي، الذي يتفوق على الجسم المضاد التلقائي لمستقبلات Fc، والبيريدوستيغمين و3,4-ديامينوبيريدين، ما يعزز الانتقال العصبي العضلي. من حين لآخر، يلزم تبادل البلازما لإزالة الأجسام المضادة.
تؤثر الحالة على نحو 3.4 لكل مليون شخص. عادةً ما تحدث متلازمة لامبرت إيتون الوهنية العضلية عند الأشخاص الذين تزيد أعمارهم عن 40 عامًا، ولكن قد تحدث في أي عمر.[3]
العلامات والأعراض
عادةً ما يتضمن الضعف الناتج عن متلازمة لامبرت إيتون الوهنية العضلية عضلات الذراعين والساقين القريبة (العضلات الأقرب إلى الجذع). على عكس الوهن العضلي الشديد، فإن الضعف يؤثر على الساقين أكثر من الذراعين. وهذا يؤدي إلى صعوبة صعود السلالم والارتفاع من وضعية الجلوس. غالبًا ما يخف الضعف مؤقتًا بعد بذل مجهود أو ممارسة الرياضة البدنية. يمكن أن تؤدي درجات الحرارة المرتفعة إلى تفاقم الأعراض. يحدث أحيانًا ضعف في السبيل القشري البصلي (عضلات الفم والحلق). ضعف عضلات العين أمر غير شائع. قد يعاني البعض من ازدواج الرؤية وتدلي الجفون وصعوبة في البلع، ولكن بشكل عام يصاحب ذلك ضعف في الساق فقط؛ هذا أيضًا يميز متلازمة لامبرت إيتون الوهنية العضلية عن الوهن العضلي الشديد، حيث تكون علامات العين أكثر شيوعًا. في المراحل المتقدمة من المرض، قد يحدث ضعف في عضلات الجهاز التنفسي. قد يعاني البعض أيضًا من مشاكل في التنسيق (ترنح).[4]
يعاني ثلاثة أرباع الأشخاص المصابين بمتلازمة لامبرت إيتون الوهنية العضلية أيضًا من اضطراب في الجهاز العصبي اللاإرادي. قد يكون هذا بمثابة جفاف الفم، والإمساك، وعدم وضوح الرؤية، وضعف التعرق، وانخفاض ضغط الدم الانتصابي (انخفاض ضغط الدم عند الوقوف، ما قد يؤدي إلى الإغماء). يذكر البعض الشعور بطعم معدني في الفم.
في الفحص العصبي، غالبًا ما يكون الضعف الذي يظهر مع الاختبار الطبيعي للقوة أقل حدة مما هو متوقع على أساس الأعراض. تتحسن القوة بشكل أكبر مع الاختبار المتكرر، على سبيل المثال تحسين القوة على قبضة اليد المتكررة (ظاهرة تعرف باسم علامة لامبرت). في حالة الراحة، عادة ما تقلل ردود الفعل؛ مع استخدام العضلات، تزداد قوة الانعكاس. تعد هذه سمة مميزة لمتلازمة لامبرت إيتون الوهنية العضلية. قد يكون المنعكس الحدقي بطيئًا.
في متلازمة لامبرت إيتون الوهنية العضلية المرتبطة بسرطان الرئة، لا يعاني معظمهم من أعراض موحية للسرطان في ذلك الوقت، مثل السعال والسعال الدموي وفقدان الوزن غير المقصود. قد تكون متلازمة لامبرت إيتون الوهنية العضلية المصاحبة لسرطان الرئة أكثر حدة.[4]
الأسباب
غالبًا ما ترتبط متلازمة لامبرت إيتون الوهنية العضلية بسرطان الرئة (50-70%)، وتحديدًا سرطان الخلايا الصغيرة، ما يجعل متلازمة لامبرت إيتون الوهنية العضلية متلازمة الأباعد الورمية. من الأشخاص المصابين بسرطان الرئة ذو الخلايا الصغيرة، يعاني 1-3% من متلازمة لامبرت إيتون الوهنية العضلية. في معظم هذه الحالات، تكون متلازمة لامبرت إيتون الوهنية العضلية هي العرض الأول لسرطان الرئة، وهو بخلاف ذلك يكون بدون أعراض.[4]
قد ترتبط متلازمة لامبرت إيتون الوهنية العضلية أيضًا بأمراض الغدد الصماء، مثل قصور الغدة الدرقية (خمول الغدة الدرقية) أو داء السكري من النمط 1. قد يحدث الوهن العضلي الوبيل أيضًا في وجود الأورام (ورم الغدة الزعترية، ورم الغدة الزعترية في الصدر)؛ الأشخاص المصابون بالتهاب الكبد الوبائي بدون ورم والأشخاص المصابين بمتلازمة لامبرت إيتون الوهنية العضلية بدون ورم لديهم اختلافات جينية مماثلة يبدو أنها تعرضهم لهذه الأمراض. يبدو أن HLA-DR3-B8 (نوع فرعي من HLA)، على وجه الخصوص، يؤهب لحدوث متلازمة لامبرت إيتون الوهنية العضلية.[5]
المظاهر السريرية
- تتظاهر هذه المتلازمة عادة في سن 50-60 سنة، وتعد إصابة الذكور أكثر شيوعاً من إصابة الإناث.
- تتظاهر بشكل ضعف عضلي مركزي دانٍ، ونادراً ما تصاب عضلات العين الخارجية أو عضلات البلع.
- تخف الأعراض مؤقتاً بعد إجراء جهد عضلي صغير، ثم يظهر الضعف والوهن مع استمرارالجهد.
- غالباً ماتكون المنعكسات الوترية ضعيفة أو معدومة، وقد تتحسن بعد إجراء جهد عضلي. (لا يوجد تفسير واضح لذلك)
- يترافق مع مظاهر إنباتية، كالإمساك وجفاف الفم والعنانة و نقص التعرق.
- يترافق مع سرطان القصبات صغير الخلايا في أكثر من 60% من الحالات.
- وقد تظهر الاعراض المذكورة قبل تشخيص الورم أو تظاهره (ففي ثلث الحالات لم يكشف الورم حتى يعد المتابعة ل25 سنة)، لذلك يجب استقصاء سرطان القصبات عند كل مريض كشف لديه (م.ل.إ) الوهنية قبل السرطان.
التشخيص
بتخطيط العضلات الكهربائي.
التدبير
لوحظ أن الاستجابة لمضادات الكولين استراز ضعيفة أو معدومة. كما أن الاستجابة لاستئصال الغدة الصعترية ضعيفة أو معدومة. وأيضاً دور تبديل البلازما أو مثبطات المناعة و الستيروئيدات بسيط.
يتحسن المرض سريرياً باستخدام أحد الأدوية التالية: 1- الغوانيدين، ومن مخاطره حدوث تثبيط نقي العظم – القصور الكلوي. 2- 3-4-ثنائي أمينو بيريدين، قد يسبب نوباً اختلاجية.
المآل
سيء عند الترافق بالسرطان.
مراجع
- Verschuuren JJ، Wirtz PW، Titulaer MJ، Willems LN، van Gerven J (يوليو 2006). "Available treatment options for the management of Lambert–Eaton myasthenic syndrome". Expert Opin. Pharmacother. ج. 7 ع. 10: 1323–36. DOI:10.1517/14656566.7.10.1323. PMID:16805718. S2CID:31331519.
- Mareska M، Gutmann L (يونيو 2004). "Lambert–Eaton myasthenic syndrome". Semin. Neurol. ج. 24 ع. 2: 149–53. DOI:10.1055/s-2004-830900. PMID:15257511. S2CID:19329757. مؤرشف من الأصل في 2021-11-30.
- Titulaer MJ، Lang B، Verschuuren JJ (ديسمبر 2011). "Lambert–Eaton myasthenic syndrome: from clinical characteristics to therapeutic strategies". Lancet Neurol. ج. 10 ع. 12: 1098–107. DOI:10.1016/S1474-4422(11)70245-9. PMID:22094130. S2CID:27421424.
- Rees JH (يونيو 2004). "Paraneoplastic syndromes: when to suspect, how to confirm, and how to manage". J. Neurol. Neurosurg. Psychiatry. 75 Suppl 2 ع. Suppl 2: ii43–50. DOI:10.1136/jnnp.2004.040378. PMC:1765657. PMID:15146039.
- Takamori M (سبتمبر 2008). "Lambert–Eaton myasthenic syndrome: search for alternative autoimmune targets and possible compensatory mechanisms based on presynaptic calcium homeostasis". J. Neuroimmunol. 201–202: 145–52. DOI:10.1016/j.jneuroim.2008.04.040. PMID:18653248. S2CID:23814568.
- بوابة طب