كأس سكري
الكأس السكري أو الكنان السكري (بالإنجليزية: Glycocalyx) ويعرف أيضًا بالنسيج الغشائي المحيط بالخلية، وهو عبارة عن غلاف بروتين سكري وشحم سكري يحيط بأغشية الخلايا لبعض البكتيريا والظهارة والخلايا الأخرى. في عام 1970 اكتشف مارتينيز وبالومو الغلاف الخلوي في الخلايا الحيوانية والذي يُعرف باسم الكأس السكري.
| كأس سكري | |
|---|---|
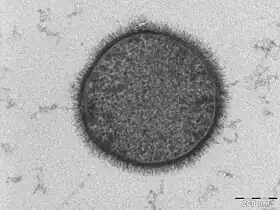 صورة مجهرية بمجهر إلكتروني نافذ لبكتيريا عصوية رقيقة، يظهر فيها كأس سكري شبيه بالشعر يحيط بغشاء الخلية (المقياس = 200 نانومتر) | |
| تفاصيل | |
| يتكون من | كربون، وأكسجين، وهيدروجين |
| معرفات | |
| ترمينولوجيا هستولوجيكا | H1.00.01.1.00002 |
| FMA | 66838 |
| ن.ف.م.ط. | A11.284.149.165.355 |
| ن.ف.م.ط. | D019276 |
تحتوي معظم الخلايا الظهارية الحيوانية على غلاف يشبه الزغب على السطح الخارجي لأغشية البلازما. يتكون هذا الغلاف من عدة أجزاء كربوهيدراتية من غليكوليبيدات غشائية وبروتينات سكرية، والتي تعمل بمثابة جزيئات العمود الفقري للدعم. بشكل عام يساعد جزء الكربوهيدرات من الغليكوليبيدات الموجود على سطح أغشية البلازما هذه الجزيئات على المساهمة في التعرف على الخلايا، والتواصل، والالتصاق بين الخلايا.[1]
يُعد الكأس السكري أداة تعريف من التي يستخدمها الجسم للتمييز بين الخلايا السليمة والأنسجة المزروعة أو الخلايا المريضة أو الكائنات الحية الغازية. يشتمل الكأس السكري على جزيئات التصاق الخلايا التي تمكن الخلايا من الالتصاق ببعضها البعض وتوجيه حركة الخلايا أثناء التطور الجنيني.[2] يلعب الكأس السكري دورًا رئيسيًا في تنظيم الأنسجة الوعائية البطانية، بما في ذلك تعديل حجم خلايا الدم الحمراء في الشعيرات الدموية.[3]
الوظيفة
غطاء سطوح مع بيوفيلم تتمسك البكتيريا بحزم بسطوح كمثال: المكورات العقدية الطافرة، تسوس (لوحة) الأسنان.
البكتيريا والطبيعة

الكأس السكري والتي تعني حرفيًا "غلاف السكر"، عبارة عن شبكة من السكريات المتعددة التي تنطلق من الأسطح الخلوية للبكتيريا، والتي تصنفها على أنها مكون سطح عالمي لخلية بكتيرية، توجد خارج البكتيريا مباشرة جدار الخلية. يطلق على الكأس الجيلاتيني البارز كبسولة، بينما تسمى الطبقة المنتشرة غير المنتظمة طبقة مخاطية. هذا الغلاف رطب للغاية ويصبغ بالروثينيوم الأحمر.
تنمو البكتيريا في النظم البيئية الطبيعية مثل التربة أو أمعاء الأبقار أو المسالك البولية البشرية، وهي محاطة بنوع من المستعمرات الصغيرة المغلفة بالكأس السكري.[4] يعمل على حماية البكتيريا من البالعات الضارة عن طريق تكوين كبسولات أو السماح للبكتيريا بالالتصاق بأسطح خاملة مثل الأسنان أو الصخور عبر الأغشية الحيوية (على سبيل المثال تلتصق المكورة الرئوية بخلايا الرئة أو بدائيات النوى أو البكتيريا الأخرى التي يمكن أن تدمج الكأس السكري لتطويق المستعمرة).
في الجهاز الهضمي
يمكن أيضًا العثور على الكأس السكري على الجزء القمي من الزغيبة داخل الجهاز الهضمي وخاصة داخل الأمعاء الدقيقة.حيث يخلق شبكة بسماكة 0.3 ميكرومتر وتتكون من عديدات السكاريد المخاطية الحمضية والبروتينات السكرية التي تنطلق من غشاء البلازما القمي للخلايا الامتصاصية الظهارية. يوفر سطحًا إضافيًا للامتزاز ويتضمن الإنزيمات التي تفرزها الخلايا الامتصاصية الضرورية للخطوات النهائية لهضم البروتينات والسكريات.
وظائف مهمة أخرى
- الحماية: يعمل على حماية غشاء البلازما من الإصابة الكيميائية
- المناعة ضد العدوى: تمكن جهاز المناعة من التعرف على الكائنات الغريبة ومهاجمتها بشكل انتقائي
- الدفاع ضد السرطان: التغيرات في الكأس السكري للخلايا السرطانية تمكن الجهاز المناعي من التعرف عليها وتدميرها
- توافق الزرع والنقل: يشكل الأساس للتوافق بين عمليات نقل الدم وزرع الأنسجة وزرع الأعضاء
- التصاق الخلية: حيث يربط الخلايا معًا حتى لا تنهار الأنسجة
- تنظيم الالتهاب: غلاف الكأس السكري على الجدران البطانية في الأوعية الدموية يمنع كريات الدم البيضاء من الالتفاف / الارتباط في الحالات الصحية.[5]
- الإخصاب: يمكّن الحيوانات المنوية من التعرف على البويضات وربطها
- التطور الجنيني: يوجه الخلايا الجنينية إلى وجهاتها في الجسم
الإخلال والمرض
نظرًا لأن الكأس السكري بارز جدًا في جميع أنحاء نظام القلب والأوعية الدموية فإن تعطيل هذه البنية له آثار ضارة يمكن أن تسبب المرض. قد تؤدي بعض المنبهات التي تسبب تصلب الشرايين إلى زيادة حساسية الأوعية الدموية. يمكن أن يحدث الخلل الوظيفي الأولي للكأس السكري بسبب ارتفاع السكر في الدم أو البروتينات الدهنية منخفضة الكثافة المؤكسدة (LDLs) والتي تسبب بعد ذلك تجلط الشرايين. في الأوعية الدموية الدقيقة يؤدي الخلل الوظيفي في الكأس السكري إلى اختلال توازن السوائل الداخلي وربما الوذمة. في أنسجة الأوعية الدموية الشريانية يتسبب اضطراب الكأس السكري في حدوث التهاب وتجلط الشرايين.
تم إجراء تجارب لاختبار دقيق لكيفية تغيير أو إتلاف الكأس السكري. استخدمت إحدى الدراسات الخاصة نموذجًا معزولًا للقلب المروى مصممًا لتسهيل الكشف عن حالة جزء الحاجز الوعائي. كان يُعتقد أن التروية بنقص التأكسج في الكأس السكري كافية لبدء آلية تحلل الحاجز البطاني. وجدت الدراسة أن تدفق الأكسجين في جميع أنحاء الأوعية الدموية لا يجب أن يكون غائبًا تمامًا (نقص الأكسجة الإقفاري)، ولكن الحد الأدنى من مستويات الأكسجين كافية للتسبب في التدهور. يمكن أن يتم تحفيز إفراز الكأس السكري عن طريق المنبهات الالتهابية مثل عامل نخر الورم ألفا. مهما كان المنبه مع ذلك فإن التخلص من البوق الجلدي يؤدي إلى زيادة جذرية في نفاذية الأوعية الدموية. نفاذية جدران الأوعية الدموية أمر غير ملائم لأن ذلك سيمكن من مرور بعض الجزيئات الكبيرة أو غيرها من المستضدات الضارة.
يعد إجهاد القص السائل أيضًا مشكلة محتملة إذا تدهورت نسبة الكأس السكري لأي سبب من الأسباب. ينتج هذا النوع من الإجهاد الاحتكاكي عن حركة السائل اللزج (أي الدم) على طول حدود التجويف. تم إجراء تجربة أخرى مماثلة لتحديد أنواع المحفزات التي تسبب إجهاد قص السوائل. تم أخذ القياس الأولي بواسطة الفحص المجهري داخل الحجاج والذي أظهر طبقة بلازما بطيئة الحركة (الكأس السكري) بسماكة 1 ميكرومتر. تسببت الصبغة الخفيفة في إتلاف الكأس السكري إلى الحد الأدنى، لكن هذا التغيير الطفيف زاد من الهيماتوكريت الشعري. وبالتالي لا ينبغي استخدام المجهر الضوئي الفلوري لدراسة الكأس السكري لأن هذه الطريقة المعينة تستخدم صبغة. يمكن أيضًا تقليل سمك الكأس السكري عند معالجته باستخدام LDL المؤكسد.[6] يمكن أن تتسبب هذه المحفزات إلى جانب العديد من العوامل الأخرى في تلف الكأس السكري الحساس. هذه الدراسات هي دليل على أن الكأس السكري يلعب دورًا مهمًا في صحة نظام القلب والأوعية الدموية.
روابط خارجية
- Smart carbohydrate chemistry as a means to understand glycocalyx biology – Video by the Lindhorst group at Beilstein TV
مراجع
- De Lacy، G. N. (1 يونيو 1993). "Book Reviews : S. Deery and D. Plowman (1991): Australian Industrial Relations (3rd edn) Sydney: McGraw-Hill". Asia Pacific Journal of Human Resources. ج. 30 ع. 4: 77–78. DOI:10.1177/103841119303000407. ISSN:1038-4111. مؤرشف من الأصل في 2021-01-24.
- Brace، C Loring (2002-03). "Anatomy & Physiology: The Unity of Form and Function. Second Edition. By Kenneth S Saladin. Boston (Massachusetts): McGraw‐Hill. $107.81. xxxiii + 1181 p; ill.; index. ISBN 0-07-250475-7. 2001". The Quarterly Review of Biology. ج. 77 ع. 1: 51–51. DOI:10.1086/343592. ISSN:0033-5770. مؤرشف من الأصل في 24 يناير 2021.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - Reitsma، Sietze؛ Slaaf، Dick W.؛ Vink، Hans؛ van Zandvoort، Marc A. M. J.؛ oude Egbrink، Mirjam G. A. (26 يناير 2007). "The endothelial glycocalyx: composition, functions, and visualization". Pflügers Archiv - European Journal of Physiology. ج. 454 ع. 3: 345–359. DOI:10.1007/s00424-007-0212-8. ISSN:0031-6768. مؤرشف من الأصل في 2020-07-30.
- Costerton، J W؛ Irvin، R T؛ Cheng، K J (1981-10). "The Bacterial Glycocalyx in Nature and Disease". Annual Review of Microbiology. ج. 35 ع. 1: 299–324. DOI:10.1146/annurev.mi.35.100181.001503. ISSN:0066-4227. مؤرشف من الأصل في 2 يونيو 2018.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - Smith، Michael L.؛ Long، David S.؛ Damiano، Edward R.؛ Ley، Klaus (2003-07). "Near-Wall μ-PIV Reveals a Hydrodynamically Relevant Endothelial Surface Layer in Venules In Vivo". Biophysical Journal. ج. 85 ع. 1: 637–645. DOI:10.1016/s0006-3495(03)74507-x. ISSN:0006-3495. مؤرشف من الأصل في 2022-01-24.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - Gouverneur، Mirella؛ Spaan، Jos A. E.؛ Pannekoek، Hans؛ Fontijn، Ruud D.؛ Vink، Hans (2006-01). "Fluid shear stress stimulates incorporation of hyaluronan into endothelial cell glycocalyx". American Journal of Physiology-Heart and Circulatory Physiology. ج. 290 ع. 1: H458–H452. DOI:10.1152/ajpheart.00592.2005. ISSN:0363-6135. مؤرشف من الأصل في 2023-01-29.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة)
- بوابة علم الأحياء
- بوابة علم الأحياء الخلوي والجزيئي
- بوابة علم الأحياء الدقيقة