شيفرة جينية
الشفرة الجينية أو الكودون (بالإنجليزية: Codon) عبارة عن قواعد ثلاثية مركبة من ثلاثة قواعد نتروجينية يمكنها أن تتراص طبقا للشفرة الجينية لتشكليل تسلسل الحمض النووي «DNA sequences» إلى بروتينات عن طريق مقابلة كل ثلاثية نيكليوتيدية (كودون) بحمض أميني من الحموض العشرين التي تشكل بروتينات الخلايا الحية. تقريبا جميع الخلايا الحية في الأحياء تستخدم الشفرة الجينية ذاتها مما يدعو لتسميتها بالشفرة الجينية القياسية «standard genetic code» ، وهي خاصة لكل إنسان، مع أن بعض الأنواع القليلة تقدم شفرة جينية ذات اختلافات طفيفية ولها وظائف أخرى، مثل الكودون الختامي. ,[1]
الاكتشاف
بدأت جهودا جادة لفهم كيف يتم ترميز البروتينات بعد اكتشاف تركيب الحمض النووي (DNA) من قبل جيمس واطسون وفرانسيس كريك ، الذين استخدما الأدلة التجريبية من موريس ويلكنز وروزاليند فرانكلين (وغيرهم). جورج جامو افترض أن رمز من ثلاثة أحرف يجب أن يوظف لترميز 20 من الأحماض الأمينية القياسية المستخدمة من قبل الخلايا الحية لبناء البروتينات . ومع وجود أربعة نوكليوتيدات مختلفة A وT و G وC ِ، فإذا اعتبرنا أن كل اثنين منهم ينتج حمضا أمينيا لحصلنا على عدد التباديل والتوافيق الممكنة بينهم =42 أي يمكنهم إنتاج 16 حمض أميني.[2]
وفي حالة رمز من 3 نوكليوتيدات فيكون أقصى عدد لتبادلات تركيب الـ 4 نوكليتيدات لأحماض أمينية = 64 حمض أميني مختلف.[3]
السمات البارزة
هذه الشفرة يقول عنها العلماء : انها تحمل كل الصفات الخِلْقِيَّة للكائن الحي، وهذه الشفرة امرها غريب .، لان نصف هذه الصفات الخلقية، يرثها الجنين عن الأب، ويرث النصف الآخر عن الام، وتُحمَل هذه الشفرة فيما يسمى (بالكروموسومات أو الصبغيات ) . وهي مختزنة في نواة كل خلية. وعدد الكروموسومات أو الصبغيات هو عدد محدِّد للنوع، وكل نوع له عدد محدَّد من هذه الصبغيات، فالإنسان مثلا في خليته ( 46 كروموسوم ) موجودة في (23 زوج) .
هذا بالنسبة للصفات الخلقية للمولود مثل لون العينين ولون الشعر، والشكل (الوجه واليدان والذراعان والرجلين) ، والطول والعرض، وكذلك صفات معنوية مثل الذكاء والمواهب، وصفات صحية مثل حساسية لسكر اللبن حساسية للجلوتين، احتمال التعرض مستقبلا لأمراض القلب أو السمنة، وغيرها.
أما الدنا الخاص بتركيب البروتينات فهو موجود في متقدرة الخلية ؛ حيث عمليات الأيض (إستقلاب) وإنتاج الطاقة تقوم بها المتقدرات.
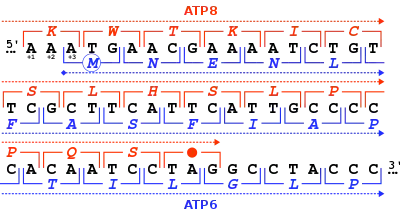
تسلسل إطار القراءة
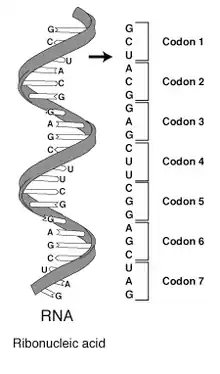
يتم تعريف تسلسل معلومات النظام الجيني من النوكليوتيدات الأولي التي تبدأ من الترجمة. على سبيل المثال، سلسلة GGGAAACCC، إذا قُرأت من الموضع الأول (من اليمين إلى اليسار) يحتوي على الكودونات GGG، AAA ، CCC؛، وإذا قرأت من الموضع الثالث (من اليمين إلى اليسار) ، نجد الكودونين المتتابعين AAC و GGA ، بهذا تختلف تركيبات البروتينات الناتجة. [5]:330 معنى ذلك أن الجزيئات الناتجة تختلف حسب موضع بدء القراءة. يقوم الرنا بقراءة الشفرة ويترجمها وينتج منها الجزيء المناسب سواء كان جزيء بروتين أو إنزيم أو غيرها.
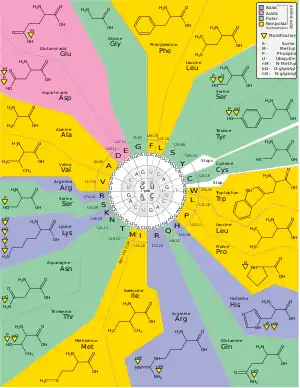
جدول كودونات الرنا (RNA)
الحمض النووي الريبوزي يُسمى اختصارًا رنا RNA، هو جزيء حيوي يتواجد تقريبًا لدى كل الكائنات الحية والفيروسات، كما يلعب أدوارًا متعددة في نقل و تشفير و فك تشفير وتنظيم التعبير الجيني من المعلومات الوراثية وتحفيز العديد من التفاعلات الكيميائية الحيوية. الرنا والدنا (DNA) هما أهم الأحماض النووية التي تُشكِّل أيضا البروتينات والليبيدات و السكريات المتعددة الضرورية للحياة. يتكون الرنا وكذلك الدنا من مجموعات ثلاثية من الجزيئات، تسمى كودونات . هذا الجزء من المقال يوضح تركيب بروتينات في جسم الإنسان من مختلف الكودونات. الكودونات هي أحماض أمينية بسيطة، تنتجها عمليات الهضم والاستقلاب من الغذاء. بعضها يمكن للجسم تكوينها والبعض الآخر لا بد للإنسان من تناولها عن طريق تنويع غذائه (غذاء صحي).
| غير قطبي | قطبي | قاعدي | حامضي | (كودون التوقف) |
| القاعدة الثانية | |||||
|---|---|---|---|---|---|
| U | C | A | G | ||
| القاعدة الأولى |
U | UUU (Phe/F) فينيل ألانين فينيل ألانين UUC (Phe/F) Phenylalanine |
UCU (Ser/S) سرين UCC (Ser/S) سرين |
UAU (Tyr/Y) تيروسين UAC (Tyr/Y) تيروسين |
UGU (Cys/C) سيستين UGC (Cys/C) سيستين |
| UUA (Leu/L) ليوسين | سيرين UCA (Ser/S) Serine | UAA Ochre (Stop) | UGA Opal (Stop) | ||
| UUG (Leu/L) Leucine | UCG (Ser/S) سرين | UAG Amber (Stop) | UGG (Trp/W) تريبتوفان | ||
| C | CUU (Leu/L) Leucine CUC (Leu/L) Leucine |
CCU (Pro/P) برولين CCC (Pro/P) Proline |
CAU (His/H) هستيدين CAC (His/H) Histidine |
CGU (Arg/R) أرجنين CGC (Arg/R) Arginine | |
| CUA (Leu/L) Leucine CUG (Leu/L) Leucine |
CCA (Pro/P) Proline CCG (Pro/P) Proline |
CAA (Gln/Q) جلوتامين
CAG (Gln/Q) Glutamine |
CGA (Arg/R) Arginine CGG (Arg/R) Arginine | ||
| A | AUU (Ile/I) إيزوليوسين AUC (Ile/I) Isoleucine |
ACU (Thr/T) ثريونين ACC (Thr/T) Threonine |
AAU (Asn/N) أسباراجين AAC (Asn/N) Asparagine |
AGU (Ser/S) Serine AGC (Ser/S) Serine | |
| AUA (Ile/I) Isoleucine | ACA (Thr/T) Threonine | AAA (Lys/K) لايسين | AGA (Arg/R) Arginine | ||
| AUG[A] (Met/M) ميثيونين |
ACG (Thr/T) Threonine | AAG (Lys/K) Lysine | AGG (Arg/R) Arginine | ||
| G | GUU (Val/V) ڤالين GUC (Val/V) ڤالين |
GCU (Ala/A) ألانين GCC (Ala/A) ألانين |
GAU (Asp/D) حمض الأسپارتيك GAC (Asp/D) حمض الأسپارتيك |
GGU (Gly/G) گلايسين GGC (Gly/G) گلايسين | |
| GUA (Val/V) ڤالين GUG (Val/V) ڤالين |
GCA (Ala/A) ألانين GCG (Ala/A) Alanine |
GAA (Glu/E) حمض الجلوتاميك GAG (Glu/E) Glutamic acid |
GGA (Gly/G) گلايسين GGG (Gly/G) گلايسين | ||
- A تسلسل معلومات النظام الجيني يبدأ بالكودون AUG لالميثيونين ويعمل كموقع بدء قراءة البروتين: يظهر AUG في مقدمة تشفير حمض نووي ريبوزي رسول المنطقة حيث يبدأ ترجمتها إلى البروتين.[6] كما يبدأ الكودون AUG بمقدمة الكودونات المتتابعة لتشكيل البروتين في حقيقيات النوى بواسطة mRNA المرسال وينتج نوعا آخر من الميثيونين ويرمز له ب (fMet/M). وكما نجد للبروتين بداية فله نهاية أيضا ؛ ينتهي بكودون توقف stop codon.
| Ala/A | GCU, GCC, GCA, GCG | Leu/L | UUA, UUG, CUU, CUC, CUA, CUG |
|---|---|---|---|
| Arg/R | CGU, CGC, CGA, CGG, AGA, AGG | Lys/K | AAA, AAG |
| Asn/N | AAU, AAC | Met/M | AUG |
| Asp/D | GAU, GAC | Phe/F | UUU, UUC |
| Cys/C | UGU, UGC | Pro/P | CCU, CCC, CCA, CCG |
| Gln/Q | CAA, CAG | Ser/S | UCU, UCC, UCA, UCG, AGU, AGC |
| Glu/E | GAA, GAG | Thr/T | ACU, ACC, ACA, ACG |
| Gly/G | GGU, GGC, GGA, GGG | Trp/W | UGG |
| His/H | CAU, CAC | Tyr/Y | UAU, UAC |
| Ile/I | AUU, AUC, AUA | Val/V | GUU, GUC, GUA, GUG |
| START | AUG | STOP | UAA, UGA, UAG |
السمات المميزة
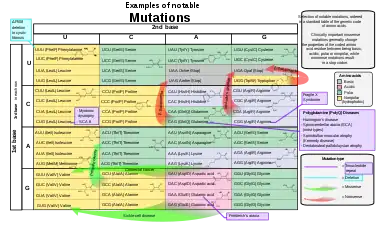
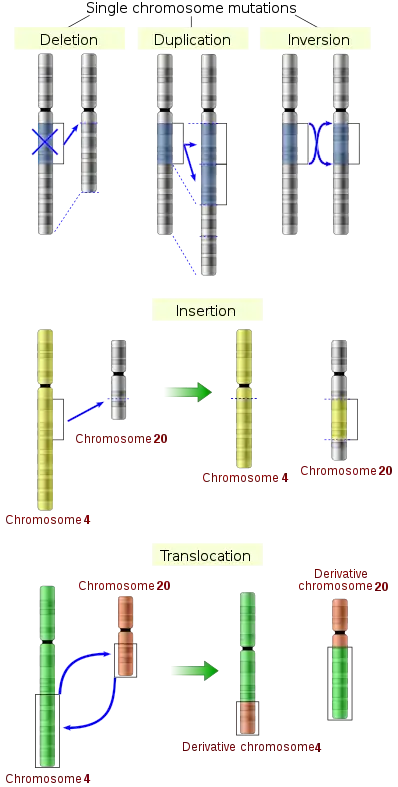
تأثير الطفرات
انظر أيضا
المراجع
|
قراءات إضافية
- Griffiths, Anthony J. F.; Miller, Jeffrey H.; Suzuki, David T.; Lewontin, Richard C.; Gelbart, William M. (1999). An Introduction to genetic analysis (ط. 7th). San Francisco: W.H. Freeman. ISBN:0-7167-3771-X. مؤرشف من الأصل في 2020-02-23.
{{استشهاد بكتاب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - Alberts, Bruce; Johnson, Alexander; Lewis, Julian; Raff, Martin; Roberts, Keith; Walter, Peter (2002). Molecular biology of the cell (ط. 4th). New York: Garland Science. ISBN:0-8153-3218-1. مؤرشف من الأصل في 2020-03-09.
{{استشهاد بكتاب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - Lodish, Harvey F.; Berk, Arnold; Zipursky, S. Lawrence; Matsudaira, Paul; Baltimore, David; Darnell, James E. (2000). Molecular cell biology (ط. 4th). San Francisco: W.H. Freeman. ISBN:0-7167-3706-X. مؤرشف من الأصل في 2020-02-21.
{{استشهاد بكتاب}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link)
وصلات خارجية
- The Genetic Codes → Genetic Code Tables
- Online DNA → Amino Acid Converter
- Online DNA Sequence → Protein Sequence converter
- Online DNA to protein translation (6 frames/17+ genetic codes)
- The Codon Usage Database → Codon frequency tables for many organisms
- Symmetries in the genetic code
- بوابة طب
- بوابة علم الأحياء
- بوابة علم الأحياء الخلوي والجزيئي