سيستين بروتياز
سيستين بروتياز المعروف أيضا باسم ثيول البروتياز (بالإنجليزية: Cysteine protease) وهي الأنزيمات التي تحلل البروتينات. تتشارك هذه الانزيمات في آلية تحفيزية شائعة تشتمل على ثيول السيستين المحب للنواة ثنائي أو ثلاثي التحفيز.
| سيستين بروتياز | |
|---|---|
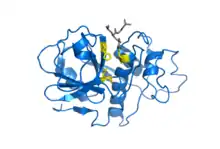 | |
| التركيب البلوري للسيستئين بيبتايديزباباين في معقد مع المثبط التساهمي E-64. المقدم من PDB 1PE6 | |
| معرف | |
| رمز | Peptidase_C1 |
| قاعدة بيانات عوائل البروتينات | PF00112 |
| قاعدة بيانات عوائل البروتينات clan | CL0125 |
| إنتربرو | IPR000668 |
| SMART | SM00645 |
| بروسايت | PDOC00126 |
| ميروبس | C1 |
| قاعدة بيانات التصنيف الهيكلي للبروتينات | 1aec |
| قاعدة بيانات توجهات البروتينات في الأغشية | 355 |
| قاعدة بيانات توجهات البروتينات في الأغشية | 1m6d |
وتكون عادة انزيمات السيستين في الفواكه بما في ذلك البابايا والأناناس والتين والجريفروت. نسبة البروتياز تميل إلى أن تكون أعلى عندما تكون الفاكهة غير ناضجة. في الواقع من المعروف أن عشرات من اللاتكس من عائلات نباتية مختلفة تحتوي على انزيمات السيستين.[1] وتستخدم أيضا كمكون في مغرضات اللحوم.
التصنيف
يحتوي نظام تصنیف بروتياز ميروبس علی 14 فصيلة بالإضافة إلی العدید من العائلات غیر المحددة حالیا (حتی عام 2013) كل منھا تحتوي علی العدید من العائلات تستخدم كل فصيلة ثالوثية حفازة أو ثنائياً في تضاعف بروتين مختلف، وهكذا تمثل تطورًا متقاربًا للآلية التحفيزية.
بالنسبة للعلائلات، P = هي فصيلة تحتوي على خليط من أسر امحب للنواة، C = بروتياز السيستين النقي. في كل فصيلة، يتم تعيين العائلات من خلال النيوكليوفيل التحفيزي (C = بروتياز السيستين).
عائلات السيستين بروتياز
| الفصائل | العائلات | الأمثلة |
|---|---|---|
| CA | C1, C2, C6, C10, C12, C16, C19, C28, C31, C32, C33, C39, C47, C51, C54, C58, C64,
C65, C66, C67, C70, C71, C76, C78, C83, C85, C86, C87, C93, C96, C98, C101 |
باباين (ببايا),[2] بروميلين (أناناس), cathepsin K (نباتات كبدية)[3] and calpain (إنسان عاقل)[4] |
| CD | C11, C13, C14, C25, C50, C80, C84 | كاسباز 1 (جرذ بني) and separase (فطريات الخميرة) |
| CE | C5, C48, C55, C57, C63, C79 | Adenain (human فيروسات غدانية type 2) |
| CF | C15 | Pyroglutamyl-peptidase I (Bacillus amyloliquefaciens) |
| CL | C60, C82 | Sortase A (مكورة عنقودية ذهبية) |
| CM | C18 | Hepatitis C virus peptidase 2 (hepatitis C virus) |
| CN | C9 | Sindbis virus-type nsP2 peptidase (فيروس سندبيس) |
| CO | C40 | Dipeptidyl-peptidase VI (Lysinibacillus sphaericus) |
| CP | C97 | DeSI-1 peptidase (فأر المنازل) |
| PA | C3, C4, C24, C30, C37, C62, C74, C99 | أنزيم TEV بروتياز (Tobacco etch virus) |
| PB | C44, C45, C59, C69, C89, C95 | Amidophosphoribosyltransferase precursor (إنسان عاقل) |
| PC | C26, C56 | Gamma-glutamyl hydrolase (جرذ بني) |
| PD | C46 | Hedgehog protein (ذبابة فاكهة شائعة) |
| PE | P1 | DmpA aminopeptidase (Ochrobactrum anthropi) |
| غير المحددة | C7, C8, C21, C23, C27, C36, C42, C53, C75 |
الآلية التحفيزية

الخطوة الأولى في آلية التفاعل التي بواسطتها يحفز سيستين بروتياز التحلل المائي للروابط الببتيدية هو إزالة بروتين ثيول في الموقع النشط للإنزيم بواسطة حمض أميني مجاور بسلسلة جانبية أساسية، عادة ما تكون بقايا هيستيدين. والخطوة التالية هي الهجوم النيكليوفيلي بواسطة الكبريت السالب الشحنة المنبع من سيستين على كربونة مجموعة الكربونيل. في هذه الخطوة، يتم تحرير جزء منها مع نهاية الأمين، ويتم استعادة بقايا الحامض الهيستيني في البروتياز إلى شكله المنتفخ، ويتم تشكيل مركب وسطي ثيوايستر الذي يربط نهاية الكربوكسيل الجديدة للطبقة السفلية بالسيستين الثيول. لذلك، يشار إليها أحيانا باسم ثيول البروتياز. في وقت لاحق يتم تحلل الرابطة الثيوايسترية لتوليد شق حمض كاربوكسيلي على الجزء المتبقي من الركيزة، في حين إعادة تكوين الانزيم الحر.
الأهمية البيولوجية
تلعب السيستين بروتياز أدوارًا متعددة الأوجه، تقريبًا في كل جانب من جوانب علم وظائف الأعضاء والتنمية. في النباتات تكون مهمة في النمو والتطور وتراكم وتعبئة البروتينات التخزينية مثل البذور. بالإضافة إلى ذلك، فهي تشارك في مسارات التأشير وفي الاستجابة للضغوط الحيوية واللاحيوية.[5] في البشر والحيوانات الأخرى، فهي مسؤولة عن الشيخوخة وموت الخلايا المبرمج (موت الخلية المبرمج)، والاستجابات المناعية من الدرجة الثانية من معقد التوافق النسيجي الكبير، ومعالجة طليعة الهرمون، وإعادة تشكيل المصفوفة خارج الخلية الهامة لتنمية العظام. قدرة البلاعم والخلايا الأخرى على تعبئة السيستين البروتينية على أسطحها تحت ظروف متخصصة قد تؤدي أيضًا إلى تسارع الكولاجين وتدهور الإيلاستين في مواقع الالتهاب في أمراض مثل تصلب الشرايين وانتفاخ الرئة.[6] والعديد من الفيروسات (مثل شلل الأطفال، والتهاب الكبد الوبائي C) تعبر عن الجينوم بأكمله كبروتينات بولي بروتينية ضخمة وتستخدم بروتياز لإلحاقه بوحدات وظيفية (على سبيل المثال، فيروس بروتيازالتبغ Etch).
التنظيم
عادةً ما يتم تصنيع البروتياز كوحدات بنائية كبيرة للبروتينات وتسمى زايموجين، مثل بروتياز سيرين سلائف تريبسينوجين وكيموتريبسينوجين، وبروفينين البوتاسيوم. ويتم تنشيط البروتياز عن طريق إزالة الجزء مثبط أو البروتين. ويحدث التنشيط بمجرد توصيل البروتياز إلى حجرة محددة داخل الخلايا (مثل لايزمومز) أو البيئة خارج الخلية (على سبيل المثال المعدة). يمنع هذا النظام الخلية التي تنتج البروتياز من التلف.
مثبطات البروتيز هي عادة بروتينات ذات نطاقات تدخل أو تغلق موقع نشط للبروتياز لمنع الوصول إلى الركيزة. في التثبيط التنافسي، يرتبط المثبط بالموقع النشط، وبالتالي يمنع تفاعل الانزيم والركيزة. وفي منع التثبيط غير التنافسي، يرتبط المانع بموقع متبادل، يغير الموقع النشط ويجعله غير قابل للدخول إلى الركيزة.
أمثلة من مثبطات الأنزيم البروتيني تشمل:
- سيربن
- ستيفن
- IAP
الاستخدامات
لا يوجد حاليا استخدام واسع النطاق لبروتياز السيستين على أنه طارد معتمد وفعال للديدان، لكن البحث في هذا الموضوع هو مجال دراسي واعد. ووجد أن بروتياز السيستين في النباتات المعزولة من هذه النباتات لديها أنشطة عالية للبروتينات معروفة بهضم نيماتودا البشرة، مع سمية منخفضة جدا.[7] تم الإبلاغ عن نتائج ناجحة ضد الديدان الخيطية مثل Heligmosomoides bakeri , الشعرينة الحلزونية, انكلوستوما سيلانيسم, المشعرة الفأرية, والنيبونية البرازيلية; الدودة الشريطية رودينتوليبز المرشفة, والخنزيري مشوكات الرأس Macracanthorynchus hirundinaceus.[8] وهناك خاصية مفيدة للبروتياز السيستين هي مقاومة الهضم الحمضي، مما يسمح بالإعطاء عن طريق الفم. أنها توفر آلية بديلة للعمل على الدودة الحالية وتطور المقاومة ويعتقد أنه من غير المحتمل لأنها تتطلب تغيير كامل في بنية بشرة الديدان الطفيلية.
في العديد من الأدوية التقليدية، تستخدم فاكهة أو ثمار اللابيا والأناناس والتين على نطاق واسع لعلاج عدوى الديدان المعوية في البشر والماشية.
أخرى
وتستخدم البروتياز السيستين كإضافات أعلاف للماشية لتحسين هضم البروتينات والأحماض النووية.[9]
انظر أيضا
- بروتياز
- سيرين-
- ثيرونين-
- ميتالو-
- أنزيم
- التحلل البروتيني
- ميروبس - قاعدة بيانات لمجموعات التطورية البروتينية
المراجع
- Domsalla A، Melzig MF (يونيو 2008). "Occurrence and properties of proteases in plant latices". Planta Med. ج. 74 ع. 7: 699–711. DOI:10.1055/s-2008-1074530. PMID:18496785.
- Mitchel، R. E.؛ Chaiken، I. M.؛ Smith، E. L. (1970). "The complete amino acid sequence of papain. Additions and corrections". The Journal of Biological Chemistry. ج. 245 ع. 14: 3485–92. PMID:5470818.
- Sierocka، I؛ Kozlowski، L. P.؛ Bujnicki، J. M.؛ Jarmolowski، A؛ Szweykowska-Kulinska، Z (2014). "Female-specific gene expression in dioecious liverwort Pellia endiviifolia is developmentally regulated and connected to archegonia production". BMC Plant Biology. ج. 14: 168. DOI:10.1186/1471-2229-14-168. PMC:4074843. PMID:24939387.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - Sorimachi، H؛ Ohmi، S؛ Emori، Y؛ Kawasaki، H؛ Saido، T. C.؛ Ohno، S؛ Minami، Y؛ Suzuki، K (1990). "A novel member of the calcium-dependent cysteine protease family". Biological Chemistry Hoppe-Seyler. 371 Suppl: 171–6. PMID:2400579.
- Grudkowska M، Zagdańska B (2004). "Multifunctional role of plant cysteine proteinases" (PDF). Acta Biochim. Pol. ج. 51 ع. 3: 609–24. PMID:15448724. مؤرشف من الأصل (PDF) في 2018-10-24.
- Chapman HA، Riese RJ، Shi GP (1997). "Emerging roles for cysteine proteases in human biology". Annu. Rev. Physiol. ج. 59: 63–88. DOI:10.1146/annurev.physiol.59.1.63. PMID:9074757.
- Stepek G، Behnke JM، Buttle DJ، Duce IR (يوليو 2004). "Natural plant cysteine proteinases as anthelmintics?". Trends Parasitol. ج. 20 ع. 7: 322–7. DOI:10.1016/j.pt.2004.05.003. PMID:15193563.
- Behnke JM، Buttle DJ، Stepek G، Lowe A، Duce IR (2008). "Developing novel anthelmintics from plant cysteine proteinases". Parasit Vectors. ج. 1 ع. 1: 29. DOI:10.1186/1756-3305-1-29. PMC:2559997. PMID:18761736.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - O'Keefe، Terrence (6 أبريل 2012). "Protease enzymes improve amino acid digestibility". Wattagnet. مؤرشف من الأصل في 2018-09-23. اطلع عليه بتاريخ 2018-01-06.
روابط خارجية
- قاعدة بيانات ميروبس على الإنترنت عن البيبتايديز ومثبطاتها
- سيستين+اندوبيبتايديز في المكتبة الوطنية الأمريكية للطب نظام فهرسة المواضيع الطبية (MeSH).
- بوابة الكيمياء
- بوابة علم الأحياء
- بوابة علم الأحياء الخلوي والجزيئي
- بوابة الكيمياء الحيوية