تفاعل ماص للحرارة
إن التفاعل الماص للحرارة في الكيمياء وفي الديناميكا الحرارية (بالإنجليزية: Endothermic reaction) هو التفاعل الذي يحتاج تكسير روابط المواد المتفاعلة أو الداخلة بالتفاعل إلى طاقة أكبر من طاقة المواد الناتجة من التفاعل. بالتالي يحتاج سريان التفاعل إلى حرارة نعطيها له من الخارج بحيث يتم التفاعل. ولهذا نقول إنه تفاعل يمتص حرارة، بدون تلك الحرارة التي نزوده بها لا يبدأ التفاعل ولا يستمر. وقد يتم التفاعل عن طريق امتصاص الحرارة من الوسط المحيط.
زيادة درجة الحرارة لمثل هذه التفاعلات يؤدي إلى زيادة سرعة التفاعل وبالتالي اتجاه التفاعل إلى الاتجاه الأمامي (في التفاعل العكوس). والتفاعلات الماصة للحرارة هي عكس التفاعلات المنتجة للحرارة، والتي ينبعث منها حرارة. مثال على التفاعل المنتج للحرارة أحتراق الخشب بأكسجين الهواء.
وبالرغم من أن عملية تكسر الروابط بين المتفاعلات في أي عملية كيميائية تتطلب كمية مبدئية من الطاقة (طاقة تنشيط). يسير التفاعل الماص للحرارة بالطريقة الآتية:
- المتفاعلات + طاقة ← النواتج
الإنثالبي قبل وبعد التفاعل
توصف التفاعلات الكيميائية بأنها ماصة للحرارة عندما يكون الفرق في الإنثالبية العيارية ذو إشارة موجبة.[1]
والإنثالبي H هو مجموع الطاقة الداخلية للنظام الداخل في التفاعل وحاصل ضرب الضغط في الحجم. وتلك هي المحتوي الحراري للنظام عندما يكون الضغط ثابتا.[2] أي أن التفاعل الماص للحرارة هو تفاعل يمتص طاقة من الوسط المحيط به في شكل حرارة. وهو يشكل معكوس التفاعل الناشر للحرارة.
إذا رمزنا إنثالبي المواد الداخلة في التفاعل وإنثالبي المواد الناتجة من التفاعل فيكون الفرق . وبناء على ذلك تكون كمية الطاقة التي يمتصها التفاعل الماص للحرارة هي:
تدل المعادلة على أن إشارة أكبر من الصفر، أي أن إشارتها موجبة. هذا الاصطلاح اخاص بالإشارة معناه أن التفاعل يمتص حرارة من الوسط المحيط. أي أنه لا بد لنا من إمداد مثل هذا التفاعل بحرارة من الخارج لكي يتم.
سريان التفاعل الماص للحرارة
مثلما يسير التفاعل الناشر للحرارة يسير التفاعل الماص للحرارة على خطوتين. تلزم طاقة تنشيط معينة تعطى إلى المواد الداخلة في التفاعل، وبعد التفاعل سيتحرر جزء من تلك الطاقة وتنطلق حرة. والاختلاف بين ذلك وتفاعل الناشر للحرارة هو ان تلك الطاقة الناتجة من التفاعل تكون اقل من الطاقة المنشطة، وهي من أجل ذلك لا تكفي لاستمرار التفاعل.
تكون طاقة التفاعل موجبة.
ذلك إذا أردنا أن يستمر التفاعل فلا بد من أن نقوم بتزويد التفاعل بطاقة من الخارج باستمرار.
لكي يسير التفاعل الماص للحرارة لا بد من السماح لإنتروبية النظام من الزيادة، بذلك يمتلك النظام إنثالبي حر ذو إشارة سالبة. ولذلك تحتاج التفاعلات الماصة للحرارة عادة إلى درجة حرارة عالية، حيث أن تحت تلك الظروف يتزايد جزء الإنتروبيا المنتمي إلي الإنثالبي الحر طبقا لمعادلة جيبس-هلمهولتز.
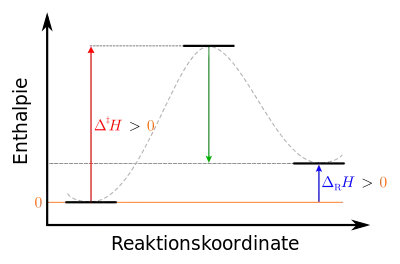 |
Legende: إلى اليسار: حالة المواد الداخلة في التفاعل: مستقرة في الوسط: حالة انتقالية لمواد المتفاعلة: غير مستقرة إلى اليمين: الحالة النهائية لنواتج التفاعل: شبه مستقرة]] |
مثال: عندما نمرر بخار الماء على سطح فحم حجري يجري تفاعل ماص للحرارة :
- .
ينتج عنه غاز الهيدروجين وغاز أول أكسيد الكربون.
المراجع
- الاتحاد الدولي للكيمياء البحتة والتطبيقية: Goldbook: endothermic reaction نسخة محفوظة 03 مارس 2016 على موقع واي باك مشين.
- الاتحاد الدولي للكيمياء البحتة والتطبيقية: Goldbook: enthalpy, H نسخة محفوظة 03 مارس 2016 على موقع واي باك مشين.
- بوابة الفيزياء
- بوابة كيمياء فيزيائية
- بوابة الكيمياء