بيكربونات الأمونيوم
بيكربونات الأمونيوم هو مركب كيميائي له الصيغة NH4HCO3 ، ويكون على شكل مسحوق بلوري أبيض عديم الرائحة.[1][2]
| بيكربونات الأمونيوم | |
|---|---|
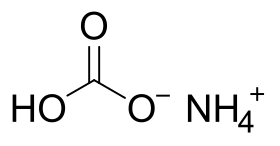 بيكربونات الأمونيوم | |
| الاسم النظامي (IUPAC) | |
بيكربونات أمونيوم | |
| أسماء أخرى | |
* كربونات أمونيوم حامضية
| |
| المعرفات | |
| رقم CAS | 1066-33-7 |
| بوب كيم | 14013 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | NH4HCO3 |
| الكتلة المولية | 79.06 غ/مول |
| المظهر | مسحوق بلوري أبيض |
| الكثافة | 1.58 غ/سم3 |
| نقطة الانصهار | 106 °س يتصعد |
| الذوبانية في الماء | 18 غ/100 مل ماء عند 20 °س |
| الذوبانية | لا ينحل في الإيثانول |
| المخاطر | |
| ترميز المخاطر |  Xn Xn |
| توصيف المخاطر | |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
الخواص
- ينحل مركب بيكربونات الأمونيوم في الماء، لكنه لا ينحل في الإيثانول.
- محاليله المائية لها صفة معتدلة (محلول 0.1 مولي من مركب بيكربونات الأمونيوم له pH مقدارها 7.8 )
- يتفكك مركب بيكربونات الأمونيوم عند التسخين حتى 60°س إلى مكوناته من الماء والأمونياك وثنائي أكسيد الكربون،
وذلك بعكس معادلة تحضيره. يلاحظ أن عملية التفكك هذه لا تترك خلفها بواقي إذ أن المنتجات غازية (في حال تصور تشكل بخار الماء).
التحضير
يحضر مركب بيكربونات الأمونيوم من تمرير غاز ثنائي أكسيد الكربون على محلول مركز من الأمونياك حيث نحصل على بلورات سهلة التصفية (الفلترة) من المركب الناتج.
NH3 + CO2 + H2O ↔ NH4HCO3
المصادر
- "معلومات عن بيكربونات الأمونيوم على موقع pubchem.ncbi.nlm.nih.gov". pubchem.ncbi.nlm.nih.gov. مؤرشف من الأصل في 2019-07-28.
- "معلومات عن بيكربونات الأمونيوم على موقع enciclopedia.cat". enciclopedia.cat. مؤرشف من الأصل في 2020-04-14.
- بوابة الكيمياء
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.