ملاريا
المَلَارْيَا[4][5][6] أو البُرَداء[4][5][7] أو الأَجَمِيَّة[5][7] هو مرض طفيلي معدي يسببه طفيلي المتصورة (أو بلازموديوم)، ينتقل عن طريق لعاب أنثى بعوض الأنفوليس، ينتقل إلى الكبد ويتكاثر ثم يطلق إلى الدم ويهاجم خلايا الدم الحمراء ويدمرها، يترافق ذلك مع مجموعة من الأعراض أهمها الحمى، فقر الدم، وتضخم الطحال. تم اكتشاف الطفيلي المسبب لمرض الملاريا في 6 نوفمبر 1880 في المستشفى العسكري بقسنطينة في الجزائر من قبل طبيب في الجيش الفرنسي يدعى ألفونس لافيران والذي حاز على جائرة نوبل في الطب والفزيولوجيا لعام 1907 عن اكتشافه هذا.
| ملاريا | |
|---|---|
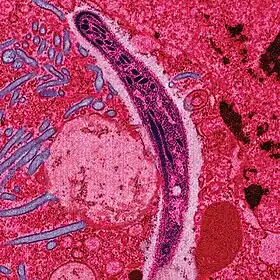 متصورة من لعاب أنثى بعوضة تنتقل خلال خلية البعوضة متصورة من لعاب أنثى بعوضة تنتقل خلال خلية البعوضة | |
| معلومات عامة | |
| الاختصاص | أمراض معدية |
| من أنواع | مرض بعدوى الأوليات ، ومرض |
| الأسباب | |
| الأسباب | متصورة منجلية، ومتصورة نشيطة، ومتصورة وبالية، ومتصورة بيضية، ومتصورة نولسية |
| طريقة انتقال العامل المسبب للمرض | عبر البعوض [1]، ونقل الدم |
| المظهر السريري | |
| الأعراض | حمى متقطعة، وتضخم كبد، وفقر الدم، وتضخم الطحال، ويرقان، وغيبوبة، ونافض[2] |
| الإدارة | |
| أدوية | |
| الوبائيات | |
| أعباء المرض | 55111095 معدل السنة الحياتية للإعاقة (2012)[3] 216000000 1 (2016) |
| التاريخ | |
| المكتشف | رونالد روس، وشارل لافران |
| سُمي باسم | نظرية ميازما، ومنطقة رطبة |
| وصفها المصدر | الموسوعة السوفيتية الأرمينية، وقاموس بروكهاوس وإفرون الموسوعي، والموسوعة السوفيتية الكبرى ، ومعجم التخاطب لماير ، وقاموس بروكهاوس وإفرون الموسوعي الصغير ، والموسوعة البريطانية نسخة سنة 1911 |
تحدث الملاريا نتيجة الاصابة بنوع من الكائنات وحيدة الخلية من عائلة المتصورات.[8] التي تنتقل إلى الانسان عن طريق لدغة أنثى بعوض الأنوفيلة .[8][9] يحدث ذالك عندما تدخل الطفيليات المتواجدة في لعاب البعوضة إلى دم الإنسان.[8] تنتقل الطفيليات إلى الكبد حيث تنضج وتتكاثر.[10] يوجد خمسة أنواع من المتصورة يمكن أن تصيب البشر.[10] وتعد المتصورة المنجلية من أكثر الأنواع خطورة وأكثرها تسببًا للوفاة، في حين أن المتصورة النشيطة والمتصورة البيضوية، و متصورة الملاريا عمومًا تسبب أعراض أقل حدة من تلك التي تسببها المتصورة المنجلية .[8] نادرًا ما تسبب الأنواع P. knowlesi المرض في البشر.[8] عادة ما يتم تشخيص الملاريا عن طريق الفحص المجهري للدم باستخدام أغشية الدم، أو باختبارات التشخيص السريع المستندة إلى البحث عن المستضد .[10] أيضًا تم تطوير طرق تستخدم تفاعل البوليميراز المتسلسل للكشف عن الحمض النووي للطفيلي، ولكنها لا تستخدم على نطاق واسع في المناطق التي تنتشر فيها الملاريا، بسبب تكلفتها وتعقيدها.[11]
يمكن الحد من خطر الإصابة بمرض الملاريا عن طريق مكافحة البعوض من خلال استخدام الناموسيات والمواد الطاردة للحشرات أو باستخدام تدابير مكافحة البعوض مثل رش المبيدات الحشرية وتصريف المياه الراكدة .[10] تتوفر العديد من الأدوية للوقاية من الملاريا بالنسبة للمسافرين الذين سينتقلون إلى مناطق ينتشر فيها المرض.[8] يوصى بجرعات من دواء مركب سلفادوكسين / بيريميثامين عند الرضع وبعد الأشهر الثلاثة الأولى من الحمل في المناطق التي ترتفع فيها معدلات الإصابة بالملاريا. اعتبارًا من عام 2020 ، تم إيجاد لقاح واحد ثبت أنه يمكنه تقليل خطر الإصابة بالملاريا بنسبة 40٪ لدى الأطفال في إفريقيا.[12][13] أظهرت دراس في لقاح آخر أكثر فاعلية وبنسبة 77٪، لكن هذه الدراسة لم تجتز المراجعة بعد.[14] هناك جهود مستمرة لتطوير لقاحات أكثر فعالية.[13] العلاج الموصى به للملاريا هو مزيج من الأدوية المضادة للملاريا التي تشمل الأرتيميسينين .[10][15][16] قد يكون الدواء الثاني إما ميفلوكين أو لوميفانترين أو سلفادوكسين / بيريميثامين.[17] يمكن استخدام الكينين مع الدوكسيسيكلين في حالة عدم توفر الأرتيميسينين.[17] تطورت المقاومة بين طفيليات الملاريا للعديد من أدوية مضادة للملاريا. على سبيل المثال، المتصورة المنجلية المقاومة للكلوروكين انتشرت في معظم المناطق المتوطنة بالملاريا، وأصبحت مقاومة مادة الأرتيميسينين مشكلة في بعض أجزاء جنوب شرق آسيا.[8]
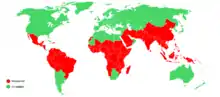
ينتشر المرض في المناطق المدارية وشبه الاستوائية الموجودة في نطاق واسع حول خط الاستواء.[10][18] وهذا يشمل جزء كبير من أفريقيا وآسيا وأمريكا اللاتينية .[8] في عام 2020 ، كان هناك 241 مليون حالة إصابة بالملاريا في جميع أنحاء العالم نتج عنها ما يقدر بنحو 627000 حالة وفاة. ما يقرب من 95 ٪ من الحالات والوفيات في أفريقيا خصوصًا في مناطق جنوب الصحراء الكبرى. انخفضت معدلات المرض من عام 2010 إلى عام 2014 ولكنها زادت من عام 2015 إلى عام 2020.[19] ترتبط الملاريا بشكل شائع بالفقر ولها تأثيرات سلبية كبيرة على التنمية الاقتصادية.[20][21] في أفريقيا، تشير التقديرات إلى أنها تؤدي إلى خسائر تُقدر بـ 12 مليار دولار أمريكي سنويًا بسبب زيادة تكاليف الرعاية الصحية، وفقدان القدرة على العمل، والآثار السلبية على السياحة.[22]
أصل الكلمة
ملاريا (بالإنجليزية: Malaria) أصلها الكلمة اللاتينية malus aria وبالإيطالية mala aria أي الهواء الفاسد إشارة إلى توالد بعوض الملاريا في المستنقعات والمياه الراكدة. كان القدماء يعتقدون أن الملاريا ينقلها هواء المستنقعات. لهذا كان الإنجليز يسمونها حمى المستنقعات (بالإنجليزية: swamp fever) والعرب يطلقون عليها البرداء لأنها تسبب الرعشة الشديدة.
البعوض المسبب للملاريا

أنثى بعوضة أنوفليس Anopheles هي الأكثر قدرة على نقل الطفيلي المسبب للملاريا أثناء امتصاصها لدم الإنسان وتعرف انها دموية التغذية الذي تحتاجه لتتمكن من وضع البيض مع ملاحظة أن ذكر البعوض لا يتغذى على الدم ولكن على رحيق الأزهار وعصارة النباتات. ويوجد 380 نوع من بعوض الأنوفليس منها حوالي 60 نوعاً له القدرة على نقل الطفيل. وكباقي أنواع البعوض تعيش معظم أطواره في الماء الآسن. بعد مرور مائة عام على اكتشاف أن البعوض ينقل طفيليات مرض الملاريا، توصل العلماء إلى اكتشاف الخريطة الجينية لمرض الملاريا وللبعوضة التي تنقل هذا المرض. ويؤدي هذا الاكتشاف إلى طرق جديدة لمعالجة عدوى مرض الملاريا الذي يعاني منه عدد كبير من المرضى في العالم.
تمتص البعوض دم مصاب بالملاريا مسبقًا و يحوي دمه على أمشاج مذكرة وأخرى مؤنثة نتجت أثناء دورة حياة الطفيلي في خلية الدم الحمراء، بعد أن يمتص البعوض الدم المحتوي على الأمشاج المذكرة والمؤنثة(Gametocytes) ، تصل هذه الأمشاج إلى التجويف الهضمي للبعوضة ويحدث لها عملية تخصيب وتنتج أفراد جديدة تسمى إسبوروزويتات(Sporozoites) والتي تصعد إلى لعاب البعوضة بعد إختراقها بطانة التجويف الهضمي للبعوضة وتستقر في لعاب البعوضة بانتظار لدغ شخص أخر سليم وحقنة بالطفيلي. هذه العملية التي يتطور بها الطفيل في البعوضة تسمى طور التكاثر الجنسي بعكس طور التكاثر اللاجنسي الذي لايلزمه وجود أمشاج مذكرة ومؤنثة والذي يحدث غالبًا في خلايا الكبد و خلايا الدم الحمراء للأنسان، حيث ينقسم الطفيل إلى أجزاء أصغر تسمى ميروزويتات merozoite وهذه تمثل السلاسلة الجديدة التي باستطاعتها غزو خلايا دم حمراء و إنتاج المزيد من الميروزويتات ولا حاجة لاندماج أمشاج مذكرة و مؤنثة كما في التجويف الهضمي للبعوضة.[23]
تسبب مرض الملاريا طفيليات من الأواليات تنتمي إلى جنس المتصورات، تحملها أنواع معينة من حشرة البعوض. ومن أجل أن تتم الطفيليات دورتها الحياتية يجب عليها أن تدخل أجسام البعوض والبشر. لاتوجد أمصال واقية لهذا الطفيل. وتختلف درجة الإصابة من موسم لآخر فأعلى معدل يكون في مواسم الأمطار نظراً لانتشار البعوض بكثرة لوجود برك ماء. ويكثر البعوض الناقل للملاريا في المناطق الدافئة الرطبة ويؤدي استقرار المناخ إلى انتشار المرض لفترة طويلة قد تمتد طوال العام. تهدف البحوث الحالية إلى خلق بعوض معدل وراثيا «مضاد للملاريا» وغير قادر على حمل الطفيليات المسببة للمرض. توجد محاولات علمية لإجراء تعديل وراثي في البعوض الناقل للمرض بما لا يسمح للطفيل بالبقاء في أحشاء الحشرة، ثم إطلاق هذه السلالات المعدلة وراثياً لتنتقل منها هذه الصفة إلى السلالات المهجنة.
أنواع الملاريا
هناك نوعان من الملاريا: حميدة وخبيثة. الملاريا الحميدة أقل خطورة وأكثر استجابة للعلاج. الملاريا الخبيثة قد تكون شديدة الخطورة، وقاتلة أحياناً. إذا كان هناك شك أن الحالة خبيثة، يجب توفير الرعاية الصحية بأسرع وقت. مسببات الملاريا حوالي 170 نوع من المتصورات، ولكن أربعة فقط يسبب الملاريا في البشر.
- المتصورة المنجلية: هذا النوع السائد في أفريقيا، وهو أكثر الأعراض شدة، وهي مسؤولة عن معظم الوفيات الناجمة عن الملاريا.
- المتصورة النشيطة: هذا النوع يوجد معظمه في أسيا، ويسبب أعراض أقل في الحدة ولكن الطفيلي يبقى في الكبد ويسبب انتكاسات لمدة تصل إلى أربع سنوات.
- المتصورة الملارية: هذا النوع يوجد في أفريقيا، ويمكن أن يسبب أعراض الملاريا النمطية، ولكن في حالات نادرة من الممكن أن يبقى الطفيل في مجرى الدم لسنوات بدون ظهور أي أعراض، في هذه الحالات من الممكن أن ينقل الشخص الحامل للطفيل العدوى إلى أخر سليم إذا قامت البعوضة بلدغه ثم لدغ الشخص السليم.
- المتصورة البيضوية: يتواجد هذا النوع ومعظمها في غرب أفريقيا، على الرغم من ندرته إلا أنه يبقى في الكبد ويسبب انتكاسات لمدة تصل إلى أربع سنوات.
يذكر أن فترة الحضانة ما بين دخول الطفيلي إلى جسم المريض وظهور أعراض المرض بحسب نوع الطفيلي وفي أغلب الحالات يتراوح بين 7 إلى 30 يوم.
دورة حياة الطفيل
تنتقل الملاريا بواسطة أنثى بعوض من جنس الأنوفيل الذي ينقل المتصورة (طفيلي من الأوليات) المسببة للمرض. وتمر دورة حياة الطفيل بعدة مراحل نمو في الإنسان والبعوض الذي ينقله من شخص لديه عدوي الملاريا عن طريق لدغ أنثى بعوضة من نوع أنوفيلس Anopheles عادة لشخص مصاب بالملاريا حيث يمتص الطفيل المسبب للملاريا من دم الإنسان المصاب ولابد لهذا الطفيل أن ينضج في القناة الهضمية للبعوض ولمدة أسبوع أو أكثر ليكون قادراً علي إصابة شخص سليم ينتقل بعدها إلى الغدد اللعابية للبعوضة ويسمي هذا الطور باسم سبوروزيت Sporozoite وعندما تلدغ هذه البعوضة شخصاً سليماً فإن الطفيل ينتقل إلى دم الإنسان في كل مرة تمتص فيها دمه. يهاجر الطفيل مباشرة إلى كبد الإنسان ويدخل خلاياه وينمو فيها متكاثراً وفي خلال هذه الفترة التي يتواجد فيها الطفيل داخل الكبد لايشعر الإنسان بأعراض المرض. وبعد فترة تتراوح بين 8 أيام إلى عدة شهور ينتقل الطفيل من الكبد ليدخل كرات الدم الحمراء حيث ينمو ويتكاثر بداخلها ثم تنفجر الكرات ليخرج منها أعداد كبيرة من الطفيل تهاجم كرات دم جديدة ويخرج من الكرات سموم أيضاً مما يؤدي إلى الشعور بالمرض. وفي هذه الفترة إذا تمكن البعوض من لدغ الإنسان المصاب فإنه يمتص الطفيل من الدم ليظل في جسمه لمدة أسبوع أو أكثر بعدها يصبح قادراً علي نقل المرض لشخص آخر. حيث يمتص دمه ليصيب شخصًا سليمًا بالمرض عن طريق بث لعابه بعد لدغ جلده. واللعاب به إسبيروزريدات (Sporozoites) التي تعيش في الغدد اللعابية للبعوض. وتتجه عبر الدم لكبد الشخص المصاب حيث تنقسم السبيرزيدات في خلاياه إلى آلاف الأقاسيم (Merozoites) التي تنساب في مجري الدم لتهاجم خلاياه الحمراء وتنقسم يها وتورمها وتكسرها ويتكاثر الطفيل داخل خلايا الدم الحمراء التي تتكسر خلال 48 – 72 ساعة ليصيب خلايا دم حمراء جديدة بالجسم، وأول الأعراض تحدث من 10 أيام – 4 أسابيع بعد العدوي. والهراض تحدث في دورات كل 48 – 72 ساعة. والأعراض تحدث من انطلاق الأقاسيم Merozoites بمجري الدم والأنيميا سببها تكسير خلايا الدم الحمراء وانظلاق الهيموجلوبين بالدم. لهذا السبب يشعر المصاب بالحمي نتيجة تفجر الخلايا المتورمة لتفرز سموما ونفايات في الدم ومقاومة جهازه المناعي لتأثيرها. والأعراض تظهر خلال عشرة أيام إلى أربعة أسابيع بعد العدوى بالرغم من أن الإحساس بالمرض يحدث بعد 5 - 8 أيام وقد تصل هذه الفترة إلى عام كامل. وتتسبب الملاريا عن الإصابة بواحد أو أكثر من جنس المتصورات.
الفيسيولوجيا المرضية
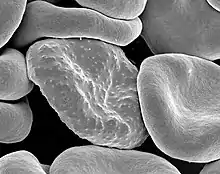
تتطور عدوى الملاريا عبر مرحلتين: الأولى تشمل الكبد (طور خارج كريات الدم الحمراء) ، والأخرى كريات الدم الحمراء (طور كريات الدم الحمراء). عندما تخترق البعوضة المصابة جلد الشخص لامتصاص الدم، تدخل الأبواغ الموجودة في لعاب البعوضة إلى مجرى الدم وتهاجر إلى الكبد حيث تصيب خلايا الكبد، وتتكاثر لا جنسيًا وبدون ظهور أي أعراض لمدة 8-30 يومًا.[24]
بعد فترة خمول في الكبد، تتمايز هذه الكائنات لإنتاج الآلاف من الميروزويتات التي تخرج من الخلايا الكبدية بعد تمزقها وتهرب إلى الدم وتصيب خلايا الدم الحمراء لتبدأ مرحلة كريات الدم الحمراء .[24] يهرب الطفيل من الكبد دون أن يكتشف عن طريق لف نفسه ببقايا غشاء الخلية الكبدية المتمزقة.[25]
تتكاثر الطفيليات مرة أخرى لاجنسيًا داخل كريات الدم الحمراء مؤدية إلى تمزيقها، ثم تخرج لتغزو خلايا دم حمراء جديدة. تتكر هذه العملية وهكذا، فإن الأوصاف الكلاسيكية لموجات الحمى تنشأ من موجات متزامنة من هروب الميروزويتات وإصابة خلايا الدم الحمراء.[24]
لا تتطور بعض أبواغ المتصورة النشيطة على الفور إلى ميروزويتات خارج الكريات الحمر، ولكنها بدلاً من ذلك يمكنها أن تنتج أطوارًا تظل كامنه لفترات تتراوح من (7-10 أشهر ) إلى عدة سنوات.[26] بعد فترة من السكون، تقوم بإعادة تنشيط وإنتاج الميروزويت. Hypnozoites هي المسؤولة عن الحضانة الطويلة والانتكاسات المتأخرة في عدوى المتصورة النشيطة.[26]
الطفيل محمي نسبيًا من هجوم الجهاز المناعي للجسم لأنه يتواجد في معظم دورة حياته البشرية داخل الكبد وخلايا الدم وغير مرئي نسبيًا للمراقبة المناعية. ومع ذلك، يتم تدمير خلايا الدم المصابة المنتشرة في الطحال . لتجنب هذا المصير، يعرض طفيلي المتصورة المنجلية بروتينات لاصقة على سطح خلايا الدم المصابة، مما يتسبب في التصاق خلايا الدم بجدران الأوعية الدموية الصغيرة، وبالتالي عزل الطفيل عن المرور عبر الدورة الدموية العامة والطحال.[27] يسبب انسداد الأوعية الدموية الدقيقة أعراضًا مثل تلك الموجودة في الملاريا المشيمية.[28] يمكن لخلايا الدم الحمراء المنفصلة أن تخترق الحاجز الدموي الدماغي وتسبب الملاريا الدماغية.[29]
أعراض الملاريا
الرعشة والانتفاضة والحمى والعرق والصداع والغثيان والقيء وآلام في العضلات وبراز مدمم ويرقان وتشنجات واغماءات. ارتفاع في درجة الحرارة قد تصاحبه قشعريرة وعرق غزير وصداع. والملاريا تُحدث أعراضاً أشبه إلى حد كبير بأعراض أمراض أخرى خاصة نزلات الإنفلونزا ولكن إذا حدث لك شك في إصابتك بالملاريا فلا تتردد في أخذ العلاج في الحال دون انتظار زيارتك للطبيب المتخصص. ويلاحظ أن أنواع الملاريا شديدة الخطورة تحدث أعراضاً مرضية شديدة مثل الغيبوبة خاصة في حالة الملاريا المخية وتحدث أيضاً أنيميا ـ نزلات معوية ـ فشل كلوي ـ ضيق في النفس. وعليك أن تلجأ إلى المستشفيات المختصة إذا ظهر عليك أعراض الملاريا حتى لو بعد مدة 3 شهور أو حتى عام كامل من تاريخ عودتك من المنطقة المنتشر بها المرض. وعادة لا يشعر المسافر بأعراض المرض إلا بعد عودته من السفر. ويجب أن ينبه الطبيب أولاً أنه كان مسافراً لمنطقة ينتشر فيها الملاريا.
وتتسبب الملاريا في حدوث أنيميا واصفرار في لون الجلد نتيجة انحلال كريات الدم الحمراء وقد تتطور أعراض المرض بسرعة في الأشخاص من ذوي المناعة الضعيفة لدرجة خطيرة ترتفع معها درجة الحرارة ويتلف الجهاز الحسي وتتكرر التشنجات مصحوبة بالغيبوبة ثم ينتهي الأمر إلى الموت وفي حالة الملاريا المتسببة عن الطفيل falciparum P. إذا لم يعالج المريض بسرعة فإن ذلك قد يتسبب عنه فشل كلوي وتشنجات وارتباك في الذاكرة والتفكير وغيبوبة تنتهي بالموت. وقد تصل الملاريا إلى المخ فتعمل كرات الدم المصابة بالطفيل والمتحللة على انسداد أوعيته الدموية وتسمي هذه الحالة بالملاريا المخية. تتمثل أعراض الإصابة بالملاريا عادة في ارتفاع درجة حرارة الجسم إلى حوالي 38 درجة م لمدة قصيرة وتتكرر الأعراض كل 48 ساعة إذا ما كانت حالة المصاب الصحية جيدة وتتشابة أعراض الإصابة مع أعراض الإنفلوانزا يصاحبها رعشة وقشعريرة وصداع وألام مستمرة في العضلات وإجهاد شديد وغثيان وقيء وإسهال خفيف وآلام شديدة في الجهاز الهضمي وأعراض قرحة معدية وتشنجات وغيبوبة قد تنتهي بموت المصاب. وتظهر الأعراض خلال أسبوع ـ عدة أشهر من تاريخ لدغ البعوض. ومن المؤكد أن إهمال علاج الملاريا خاصة المتسببة عن النوع P. falciparum قد يؤدي إلى الموت. ومن الثابت إحصائياً أن أكثر من 2% من المصابين يموتون بسبب تأخر العلاج. فيصابون بفشل كبدي وكلوي وتكسير خلايا الدم الحمراء والالتهاب السحائي وتمزق الطحال Rupture of the spleen والنزيف المتكرر.
انتكاسة الملاريا
يمكن لأعراض الملاريا أن تتكرر بعد مرور فترات متفاوتة خالية من الأعراض وتسمى انتكاسة(malaria relapse) حيث تعاود الأعراض الظهور بعد فترة خالية من الأعراض تسببها الطفيليات_غالبًا p.vivax _التي دخلت فترة كمون في الكبد نتيجة لعلاج غير ملائم أو غير فعال.[30] الانتكاسة هي معاودة ظهور الأعراض بعد القضاء على الطفيليات في الدم ولكنها تستمر في الظهور مثل: الهاجِعات (من أشكال طفيليات الملاريا) الخاملة في خلايا الكبد.[31] تحدث الانتكاسة عادة بين 24-8 أسبوع وعادة يتم رصدها في أمراض البلازمود النشيط والبلازمود البيضوي.[32] ولكن غالباً يتم نسب التكرارات مثل البلازمود النشيط إلى تنشيط الهيبنوزويت. وقد يكون للبعض منهم أصل ميروزويت ممتد خارج الأوعية، مما يجعل تلك التكرارات أيبوبة وليس انتكاسة.[33] تم الاعتراف حديثاً بمصدر غيرهيبنوزويت، ويعتبر مصدر مُساهِم محتمل لتكرر peripheral P. vivax parasitemia، ألا وهو أشكال انتعاش كرات الدم الحمراء في النخاع العظمي.[34] وتتضمن حالات ملاريا البلازمود النشيط في المناطق معتدلة المناخ البيات الشتوي للهيبنوزويت، مع بداية الانتكاسات بعام بعد لدغة البعوضة.[35] عودة العدوى تعني أن الطفيليات التي تسببت في العدوى السابقة تم إزالتها من الجسد ولكن تم إدخال طفيلية جديدة. لا يمكن التفريق بين عودة العدوى والأيبوبة بسهولة، على الرغم من أن تكرار العدوى في خلال اسبوعين من العلاج للعدوى الأولية عادة يُنسب لفشل العلاج.[30] بإمكان الأشخاص أن يطوروا مناعة عند التعرض للعدوى بشكل
التشخيص

نظرًا للطبيعة غير المحددة لأعراض الملاريا، يُشتبه في التشخيص بناءً على الأعراض، ثم يتم تأكيده بالفحص المخبري. في المناطق التي تنتشر فيها الملاريا، توصي منظمة الصحة العالمية (WHO) الأطباء بالاشتباه في الإصابة بالملاريا لدى أي شخص تظهر لديه أعراض الحمى، أو ارتفاع درجة الحرارة فوق 37.5 درجة مئوية دون أي سبب واضح .[36] يجب أيضًا الاشتباه في الإصابة بالملاريا عند الأطفال الذين تظهر عليهم علامات فقر الدم، أو اختبار معملي يظهر مستويات الهيموجلوبين أقل من 8 جرام لكل ديسيلتر من الدم.[36] في المناطق التي تقل فيها إنتشار الملاريا أو لا ينتشر فيها الملاريا اطلاقًا توصي منظمة الصحة العالمية باختبار الأشخاص المعرضين للإصابة بالملاريا فقط (عادةً الذين قادمون من مناطق موبوءة بالملاريا) .[36]
عادة ما يتم تأكيد الإصابة بالملاريا عن طريق الفحص المجهري لفيلم الدم(Blood film) أو عن طريق اختبارات التشخيص السريع (Rapid diagnosis test) المستندة عن البحث عن الأنتجين في الدم . يتظمن الفجص المجهري فحص لطخة دم مصبوغة بصبغة جيمزا باستخدام المجهر الضوئي وتعتبر هي الطريقة المثلى لتشخيص. هناك طريقتين للفحص المجهوي الطرقة الأولى تسمى فيلم الدم السميك (Thic blood film) التي تسمح بفحص الدم وتشخيص الاصابة بالملاريا بدون تحديد نوع الطفيل، أما الطريقة الأخرى والأدق تسمى فيلم الدم الرقيق (Thin blood test) التي تسمح برؤية الطفيليات الفردية بوضوح وتحديد نوع الطفيلي و تعتبر أكثر دقة من فيلم الدم السميك. في ظل ظروف المختبر الميداني النموذجية، يمكن للفحص المجهري اكتشاف الطفيليات عندما يكون هناك ما لا يقل عن 100 طفيلي لكل ميكرولتر من الدم، وهو ما يقرب النطاق الأدنى للعدوى المصحوبة بأعراض.[36] التشخيص المجهري يتطلب موظفين مدربين، ومعدات محددة، وكهرباء، وإمدادات ثابتة من شرائح وبقع الفحص المجهري.[36]
في الأماكن التي لا يتوفر فيها الفحص المجهري، يتم تشخيص الملاريا بطريقة الفحص السريع المستندة عن البحث عن الأنتجين RDTs ، وهي اختبارات مستضد سريعة تكشف عن بروتينات الطفيليات في عينة الدم. تتوفر مجموعة متنوعة من الاختبارات التشخيصية السريعة تجارياً، وتستهدف بروتينات الطفيليات الغنية بالبروتين الغني بالهيستيدين 2 (HRP2 ، يكتشف المتصورة المنجلية فقط) ، نازعة هيدروجين اللاكتات، أو الألدولاز .[36] يستخدم اختبار HRP2 على نطاق واسع في إفريقيا، حيث تسود المتصورة المنجلية ذلك، نظرًا لاستمرار HRP2 في الدم لمدة تصل إلى خمسة أسابيع بعد علاج العدوى، لا يمكن لاختبار HRP2 أحيانًا التمييز بين ما إذا كان شخص ما مصابًا بالملاريا حاليًا أو أُصيب بها سابقًا. بالإضافة إلى ذلك، تفتقر بعض طفيليات المتصورة المنجلية في منطقة الأمازون إلى جين HRP2 ، مما يعقد عملية الكشف.[36] اختبارات التشخيص السريع (RDT) سريعة وسهلة الانتشار في الأماكن التي لا تحتوي على مختبرات تشخيص كاملة.[36] ومع ذلك، فإنها تعطي معلومات أقل بكثير من الفحص المجهري، وفي بعض الأحيان تختلف في الجودة من منتج إلى منتج.[36]
تم تطوير الاختبارات المصلية للكشف عن الأجسام المضادة ضد البلازموديوم من الدم، ولكنها لا تستخدم لتشخيص الملاريا بسبب ضعف حساسيتها ونوعيتها نسبيًا. تم تطوير اختبارات تضخيم الحمض النووي عالية الحساسية، ولكنها لا تستخدم سريريًا بسبب تكلفتها المرتفعة نسبيًا .[36]
العلاج
تعالج الملاريا بأدوية مضادات الملاريا . ويعتمد نوع العلاج المستخدم على على نوع وشدة المرض.[37]
الملاريا غير المعقدة
يمكن علاج الملاريا البسيطة أو غير المعقدة بالأدوية عن طريق الفم. تعتبر أدوية الأرتيميسينين فعالة وآمنة في علاج الملاريا غير المعقدة.[38] استخدام أدوية الأرتيميسينين بالاشتراك مع مضادات الملاريا الأخرى (المعروفة باسم العلاج المركب ACT) تكون فعالة بنسبة 90٪ تقريبًا عند استخدامها لعلاج الملاريا غير المصحوبة بالمضاعفات.[39] العلاج الأكثر فعالية لعدوى المتصورة المنجلية هو مادة الأرتيميسينين، وهي أدوية لم تفاومها الطفيليات بعد، بعكس بقية الأدوية التي أظهرت بعضها مقاومة من قبل الطفيليات خصوصًا في المناطق المتوطنة بالملاريا.[40][41] يعتبر دواء الأرتيميثير - لوميفانترين ( نظلم ست جرعات) أكثر فعالية من أرتيميثير - لوميفانترين (نظام أربع جرعات) أو التركيبات الأخرى التي لا تحوي على مشتقات الأرتيميسينين في علاج الملاريا المنجلية.[42][43] أيضًا يمكن استخدام تركيبة من ثنائي هيدروأرتيميسينين وبيبيراكوين .[44][45][46] أظهر العلاج المركب المكون من الأرتيميسينين-نافثوكوين نتائج واعدة في علاج الملاريا المنجلية.[47] ومع ذلك، هناك حاجة إلى مزيد من البحث لإثبات فعاليته كعلاج موثوق.[48] استخدام دواء الأرتيسونات مع الميفلوكين فعّال أكثر بكثير من لو كان الميفلوكين وحده في علاج الملاريا المنجلية غير المعقدة.[49] لم يظهر العلاج الأحادي أزيترومايسين فعالية في علاج الملاريا المتصورة أو النشيطة.[50] فعالية الأمودياكين بالإضافة إلى سلفادوكسين-بيريميثامين أقل مقارنةً بسلفادوكسين-بيريميثامين وحده في الملاريا المنجلية غير المعقدة.[51] لا توجد بيانات كافية عن الكلوربروجوانيل-دابسون في علاج الملاريا المنجلية غير المعقدة.[52][53] إضافة البريماكين كعلاج مركب مع الأرتيميسينين للملاريا المنجلية يقلل من انتقال العدوى في اليوم الثالث والرابع واليوم الثامن من الإصابة.[54] يعتبر استخدام مركب سلفادوكسين - بيريميثامين مع الأرتيسونات أفضل من سلفادوكسين - بيريميثامين مع الأمودياكين في الفعالية. ومع ذلك، فإن الأخير أفضل من السابق في تقليل الأطوار المشيجية للطفيل في الدم في اليوم السابع.[55]
عادة لا تخلف الإصابة بالمتصورة النشيطة والمتصورة البيضية ومتصورة الملاريا مضاعفات خطرة قد تهدد الحياة . يتطلب علاج ملاريا المتصورة النشيطة التخلص من أطوار الطفيل في الدم (باستخدام الكلوروكين أو العلاج المركب المحتوي على مادة الأرتيميسينين ومضادات الملاريا) كما يتطلب القضاء على أطوار الطفيل الكامنة في الكبد باستخدام علاج البريماكين أو تافينوكوين .[56][57] ظهر أن استخدام البريماكين في حالة الحمل أو في الأطفال أو في المصابين بفقر الدم الناجم عن عوز إزيم جلوكوز-٦فوسفات له أثار ضارة.
توصي منظمة الصحة العالمية باستخدام الكينين بالإضافة إلى الكليندامايسين في علاج الملاريا أثناء الحمل (الثلاثة الأشهر الأولى من الحمل) ، بينما استخدام العلاج المركب المحتوي على الأرتيميسينين ومضادات الملاريا الأخرى- في المراحل المتأخرة من الحمل (من الشهر الرابع إلى الولادة ).[58][59] لكن لاتزال الأدلة الموجودة بشأن أمان أدوية الملاريا أثناء الحمل محدودة.[60]
الملاريا المعقدة
تحدث حالات الملاريا الشديدة والمعقدة دائمًا بسبب الإصابة بالمتصورة المنجلية بينما الاصابة بالأنواع الأخرى عادة ما تسبب أعراض خفيفة كالحمى.[61] تعتبر حالات الملاريا الحادة والمعقدة من الحالات الطبية الطارئة لأن معدلات وفيات الملاريا المعقدة (الملاريا التي يسببها طفيل المتصورة المنجلية ) تصل إلى (10٪ إلى 50٪).[62]
العلاج الموصى به للملاريا الشديدة هو الاستخدام الوريدي للأدوية المضادة للملاريا. بالنسبة للملاريا الشديدة، كان الأرتيسونات بالحقن متفوقًا على الكينين في كل من الأطفال والبالغين.[63][64] في مراجعة منهجية أظهرت مشتقات الأرتيميسينين (الأرتيميثير والأرتيثر) فعالية أكثر من الكينين في علاج الملاريا الدماغية عند الأطفال.[65] يتضمن علاج الملاريا الشديدة تدابير داعمة من الأفضل القيام بها في وحدة العناية المركزة . وهذا يشمل إدارة الحمى الشديدة والنوبات التي قد تنجم عنها. ويشمل أيضًا مراقبة جهد التنفس وانخفاض نسبة السكر في الدم وانخفاض البوتاسيوم في الدم .[66] يساعد الكينين على خفض الحمى كما أنه فعال في إزالة الطفيليات من الجسم.في الملاريا الشديدة يحدث نقص لسكر الدم لذا فأعطى الجلوكوز من شأنه أن يرفع من مستوى السكر في الدم .[67]
الملاريا الدماغية
هي شكل من أشكال الملاريا التي قد تؤول إلى الموت.[68] المضاعفات العصبية تحدث نتيجة إنسداد الشعيرات الدموية في الدماغ نتيجة لترسب والتصاق خلايا الدم الحمراء المصابة بالطفيل على جدارن الشعيرات الدموية الدقيقة في الدماغ، وقد يصاحبها مضاعفات خطيرة نتيجة نقص التروية الدموية. لا توجد بيانات كافية حول ما إذا كان استخدام العوامل التناضحية مثل المانيتول فعالة في علاج الملاريا الدماغية.[69] يرتبط الفينوباربيتون الروتيني في الملاريا الدماغية بعدد أقل من التشنجات ولكن من المحتمل أن يكون هناك المزيد من الوفيات.[70]
الملاريا المقاومة للأدوية
تعتبر مقاومة الأدوية مشكلة متنامية في علاج الملاريا في القرن الحادي والعشرين.[71][72] في العقد الأول من القرن الحادي والعشرين، ظهرت الملاريا ذات المقاومة الجزئية للأرتيميسين في جنوب شرق آسيا. أصبحت المقاومة الآن شائعة ضد جميع فئات الأدوية المضادة للملاريا باستثناء عائلة الأرتيميسينيات، التي أن مقاومتها هي الأخرى قد يصبح التغلب على الملاريا أمرًا صعبًا. علاج السلالات المقاومة لأدوية الملاريا يعتمد بشكل أساسي على هذه الفئة من الأدوية(الأرتيميسينات). تكلفة مادة الأرتيميسينين تحد من استخدامها في الدول الفقيرة.[73] أظهرت سلالات الملاريا الموجودة على الحدود بين كمبوديا وتايلاند مقاومة للعلاجات المركبة من بينها أدوية الأرتيميسينين، وبالتالي قد تصبح غير قابلة للعلاج.[74] تم اكتشاف الملاريا المقاومة للأرتيميسينين في كمبوديا، ميانمار، تايلاند، وفيتنام ،[74] وكانت هناك مقاومة ناشئة في لاوس.[75][76] تم اكتشاف مقاومة الأرتيميسينين والبيبيراكين لأول مرة في عام 2013 في كمبوديا، وبحلول عام 2019 انتشرت في جميع أنحاء كمبوديا وإلى لاوس وتايلاند وفيتنام.[77]
الوقاية
تشمل الطرق المستخدمة للوقاية من الملاريا الأدوية والقضاء على البعوض والوقاية من اللدغات. اعتبارًا من عام 2020 ، يوجد لقاح واحد للملاريا (يُعرف باسم RTS ، S ) ثبت أنه فعال في تقليل خطر الإصابة بالملاريا بنسبة 40٪ لدى الأطفال في إفريقيا.[12][13] يتطلب وجود الملاريا في منطقة ما كثافة سكانية عالية، وانشار للبعوض الناقل للمرض وامكانية انتقال من الإنسان إلى البعوض ومن البعوض إلى الإنسان. إذا تم منع أو كسر هذه الدائرة بشكل كافٍ، فإن الطفيل يختفي في النهاية من تلك المنطقة، كما حدث في أمريكا الشمالية وأوروبا وأجزاء من الشرق الأوسط. ومع ذلك، ما لم يتم القضاء على الطفيل من العالم بأسره، فإنه يمكن أن يعود مرة أخرى إذا وجد الضروف الملائمة التي تسمح بتكاثره.[78]
قد تكون الوقاية من الملاريا أكثر فعالية من حيث التكلفة من علاج المرض على المدى الطويل، لكن التكاليف الأولية المطلوبة بعيدة عن متناول العديد من فقراء العالم. هناك فرق كبير في تكاليف المكافحة (أي الحفاظ على توطن منخفض) وبرامج القضاء بين البلدان. على سبيل المثال، في الصين - التي أعلنت حكومتها في عام 2010 عن استراتيجية لمتابعة القضاء على الملاريا في المقاطعات الصينية - الاستثمار المطلوب هو نسبة صغيرة من الإنفاق العام على الصحة. في المقابل، سيكلف برنامج مماثل في تنزانيا ما يقدر بخمس ميزانية الصحة العامة.[79] وفي عام 2021 أعلنت منظمة الصحة العالمية أن الصين تخلصت من الملاريا كليًا.[80]
في المناطق التي تنتشر فيها الملاريا، غالبًا ما يعاني الأطفال دون سن الخامسة من فقر الدم، والذي يرجع أسبابها إلى الإصابة تكسر خلايا الدم الحمراء نتيجة إصابتها بالطفيل. إن إعطاء الأطفال المصابين بفقر الدم في هذه المناطق الأدوية الوقائية المضادة للملاريا يحسن مستويات خلايا الدم الحمراء بشكل طفيف ولكنه لا يؤثر على خطر الوفاة أو الحاجة إلى العلاج في المستشفى.[81]
مكافحة البعوض

هي الأساليب المستخدمة لتقليل الملاريا عن طريق تقليل مستويات انتقالها. للحماية الفردية تعتبر الناموسيات المعالجة بمبيدات الحشرات (ITNs) والرش الموضعي للأماكن المغلقة (IRS) فعالة، وقد استخدمت بشكل واسع للوقاية من الملاريا، وقد ساهم استخدامها كثيرًا في انخفاض معدل الإصابة بالملاريا في القرن الحادي والعشرين.[82] د لا تكون الناموسيات المعالجة بمبيدات الحشرات في الأماكن المغلقة كافية للقضاء على المرض، حيث تعتمد هذه التغيرات على عدد الأشخاص الذين يستخدمون الناموسيات، وعدد الأشخاص الذين يكونون معرضين لخطر الاصابة عندما يكونون خارج المنزل، وزيادة معدلات البعوض المقاومة للمبيدات الحشرية.[83][83]
الناموسية

تساعد الناموسيات في إبعاد البعوض عن الناس وتقليل معدلات العدوى وانتقال الملاريا. لا تعتبر الناموسيات حاجزًا مثاليًا وغالبًا ما يتم معالجتها بمبيد حشري مصمم لقتل البعوض قبل أن يتاح لها الوقت لإيجاد طريقة لتجاوز الشبكة. تُقدَّر فعالية الناموسيات المعالجة بمبيدات الحشرات بضعف فعالية الناموسيات غير المعالجة وتوفر حماية أكبر 70٪ مقارنة بعدم وجود شبكة.[84] بين عامي 2000 و 2008 ، أنقذ استخدام الناموسيات المعالجة بمبيدات الحشرات حياة ما يقدر بنحو 250000 رضيع في أفريقيا جنوب الصحراء الكبرى.[39] حوالي 13٪ من الأسر في دول جنوب الصحراء كانت تمتلك الناموسيات المعالجة بمبيدات الحشرات في عام 2007 [39] وفي عام 2008 كان 31٪ من الأسر الإفريقية تمتلك على الأقل ناموسية معالجة بمبيدات الحشرات. في عام 2000 ، تمت حماية 1.7 مليون (1.8٪) من الأطفال الأفارقة الذين يعيشون في مناطق موبوءة بالملاريا بواسطة الناموسيات المعالجة بمبيدات الحشرات. ارتفع هذا العدد إلى 20.3 مليون (18.5٪) في عام 2007 ، بينما تُرك 89.6 مليون طفل غير محميين.[85] معظم الناموسيات مشربة بالبيروثرويدات، وهي فئة من مبيدات حشرية منخفضة السمية . تكون أكثر فاعلية عند استخدامها من الغسق حتى الفجر.[86] يوصى بتعليق "ناموسية سريرية" كبيرة فوق منتصف السرير وإما ثني الحواف أسفل المرتبة أو التأكد من أنها كبيرة بما يكفي بحيث تلامس الأرض.[80] الناموسيات المعالجة بمبيدات الحشرات مفيدة للحوامل في المناطق الموبوءة بالملاريا في أفريقيا ولكن هناك حاجة إلى مزيد من البيانات في آسيا وأمريكا اللاتينية.[87]
في المناطق ذات المقاومة العالية للملاريا، يكون البيبيرونيل بتوكسيد (PBO) مع البيريثرويدات في الناموسيات فعالة في تقليل معدلات الإصابة بالملاريا.[88] لا تزال هناك أسئلة تتعلق بفعالية البيبيرونيل بتوكسيد على الناموسيات حيث أن التأثير على معدل وفيات البعوض لم يستمر بعد عشرين غسلًا في التجارب التجريبية.[88]
الرش الموضعي للأماكن المغلقة
هو رش المبيدات الحشرية على الجدران داخل المنزل. بعد امتصاص الدم، يستريح العديد من البعوض على سطح قريب أثناء هضم الدم الممتص، لذلك إذا كانت جدران المنازل مغطاة بالمبيدات الحشرية، يمكن قتل البعوض الساكن قبل أن يتمكن من لدغ شخص آخر ونقل طفيلي الملاريا.[89] اعتبارًا من عام 2006 ، أوصت منظمة الصحة العالمية باستخدام 12 مبيدًا حشريًا في عمليات الرش الموضعي للأماكن المغلقة، بما في ذلك الـ دي.دي.تي والبيريثرويدات سيفلوثرين ودلتاميثرين .[90] هذا الاستخدام العام لكميات صغيرة من الـ دي.دي.تي مسموح به بموجب اتفاقية ستوكهولم التي تحظر استخدامه الزراعي.[91] هناك مشكلة واحدة مع جميع أشكال المبيدات وهي مقاومتها . يميل البعوض المصاب بمضخة الذي تعرض لمبيد لم يقضي عليه إلى الراحة والعيش في الداخل، وبسبب التهيج الناجم عن الرش، تميل سلالاتها إلى العيش في الهواء الطلق، مما يعني أنهم يصبحوا أقل تأثراً .[92] المجتمعات التي تستخدم الناموسيات المعالجة بالمبيدات الحشرية، بالإضافة إلى الرش الموضعي للأماكن المغلقة بمبيدات حشرية "غير شبيهة بالبيرثرويد" شهدت انخفاضًا في معدل الإصابة.[93] وعلى النقيض من ذالك، فإن استخدام المبيدات الحشرية "الشبيهة بالبيرثرويد" بالإضافة إلى الرش الموضعي للأماكن المغلقة لم يظهر عنه فائدة إضافية يمكن اكتشافها في المجتمعات التي تستخدم الناموسيات المعالجة بالمبيدات الحشرية.[93]
طرق أخرى لمكافحة البعوض
لقد جُربت العديد من الطرق الأخرى تقليل لدغات البعوض ومنع انتشار الملاريا. الجهود المبذولة لتقليل يرقات البعوض من خلال تقليل توافر المياه الراكدة والمفتوحة حيث يتطور الطفيل، أو عن طريق إضافة مواد لتقليل نموها، تكون فعالة في بعض الأماكن.[94] أجهزة طارد البعوض الإلكترونية، والتي تصدر أصواتًا عالية التردد من المفترض أن تُبقي إناث البعوض بعيدًا، ليس لديها دليل داعم على فعاليتها.[95] هناك دليل على أن الضباب قد يكون له تأثير على انتقال الملاريا.[96] قد يؤدي إبادة اليرقات الطافية في المسطحات المائية باستخدام المبيدات الحشرية الكيميائية أو الميكروبية إلى تقليل انتقال الملاريا.
الأدوية
هناك عدد من الأدوية التي يمكن أن تساعد في الوقاية من الملاريا خصوصًا عند أولائك الذين سينتقلون إلى أماكن تنتشر فيها العدوى. العديد من هذه الأدوية تستخدم أيضًا في العلاج. في الأماكن التي يكون فيها المتصورة مقاومة لواحد أو أكثر من الأدوية، يتم استخدام ثلاثة أدوية تشمل ميفلوكين، أو دوكسيسيكلين، أو مزيج من أتوفاكون / بروغوانيل ( مالارون ) للوقاية.[97] يمكن استخدام الدوكسيسيكلين والأتوفاكون / البروغوانيل بينما يتم أخذ الميفلوكين مرة واحدة في الأسبوع.[98] قد يؤدي إعطاء الأدوية المركبة من مضادة للملاريا إلى مجموعة سكانية بأكملها في نفس الوقت إلى تقليل خطر الإصابة بالملاريا بين السكان، عوامل أخرى مثل إعطاء الدواء بالإضافة إلى تدابير وقائية أخرى مثل السيطرة على البعوض، ونسبة الأشخاص الذين عولجوا في المنطقة، وخطر الإصابة بالملاريا قد تلعب دورًا في فعالية أساليب العلاج الجماعي بالعقاقير.[98]
لا يبدأ التأثير الوقائي على الفور، وعادة ما يبدأ الأشخاص الذين يزورون المناطق التي توجد بها الملاريا في تناول الأدوية قبل أسبوع إلى أسبوعين من وصولهم، ويستمرون في تناولها لمدة أربعة أسابيع بعد المغادرة (باستثناء خليط الـ الأتوفاكون / البروغوانيل، الذي يحتاج فقط إلى البدء قبل يومين والاستمرار لمدة سبعة أيام بعد ذلك).[99] غالبًا ما يكون استخدام العقاقير الوقائية غير عملي لأولئك الذين يعيشون في مناطق تنتشر فيها الملاريا، وعادةً ما يُعطى استخدامها فقط للنساء الحوامل والزائرين لفترات قصيرة. ويرجع ذلك إلى تكلفة الأدوية، والآثار الجانبية للاستخدام طويل الأمد، وصعوبة الحصول على الأدوية المضادة للملاريا في الدول الفقيرة .[100] أثناء الحمل، عُثِر على دواء للوقاية من الملاريا لتحسين وزن الطفل عند الولادة وتقليل خطر الإصابة بفقر الدم لدى الأم.[101] قد يعود تعاطي الأدوية الوقائية في المناطق الموبوءة بالمرض بنتائج عكسية حيث يشجع استخدام العقاقير الوقائية في المناطق الموبوءة على تطوير مقاومة جزئية للأدوية.[102]
إن إعطاء الأدوية المضادة للملاريا للرضع من خلال العلاج الوقائي المتقطع يمكن أن يقلل من خطر الإصابة بعدوى الملاريا، ودخول المستشفى، وفقر الدم.[103]
يعتبر الميفلوكين أكثر فعالية من سلفادوكسين/بيريميثامين في الوقاية من الملاريا للحامل المصابة بفيروس نقص المناعة البشرية. كوتريموكسازول فعال في الوقاية من عدوى الملاريا وتقليل خطر الإصابة بفقر الدم لدى النساء المصابات بفيروس نقص المناعة البشرية.[104] إعطاء سلفادوكسين-بيريميثامين لثلاث جرعات أو أكثر كعلاج وقائي متقطع أفضل من جرعتين للنساء المصابات بفيروس نقص المناعة البشرية اللائي يعشن في المناطق الموبوءة بالملاريا.[105]
قد يؤدي العلاج الفوري للحالات المؤكدة باستخدام العلاجات المركبة المكونة من مادة الأرتيميسينين (ACTs) أيضًا إلى تقليل انتقال العدوى.[106]
التثقيف الصحي
لقد تم بنجاح استخدام استراتيجيات المشاركة المجتمعية والتثقيف الصحي التي تعزز الوعي بالملاريا وأهمية تدابير المكافحة للحد من انتشار الملاريا في بعض مناطق العالم النامي.[107] التعرف على المرض في المراحل المبكرة يمكن أن يمنعه من أن يصبح قاتلاً. يمكن للتعليم أيضًا إعلام الناس بالاماكن التي يستخدمها الطفيل للعيش كالمياه الراكدة، وخزانات المياه التي تعد مناطق تكاثر مثالية للطفيلي والبعوض، وبالتالي تقليل مخاطر انتقال العدوى بين الناس. يستخدم هذا عمومًا في المناطق الحضرية حيث توجد مراكز سكانية كبيرة في مكان ضيق ومن المرجح أن يكون انتقال العدوى في هذه المناطق أكبر.[108] العلاج الوقائي المتقطع هو تدخل آخر اُستُخدم بنجاح للسيطرة على الملاريا عند النساء الحوامل والرضع ،[109] وفي الأطفال ما قبل المدرسة حيث يكون الانتقال موسميًا.[110]
القضاء على الملاريا
يُعرَّف "القضاء على الملاريا" على أنه وقف سريان نوع محدد من الطفيليات المسببة للملاريا على المستوى المحلي في منطقة جغرافية معينة نتيجة الاضطلاع بأنشطة تستهدف مكافحتها. ويتعين الاستمرار في اتخاذ تدابير ترمي إلى الوقاية من معاودة سريان المرض[111]
وبلغ عدد البلدان التي أفادت بتسجيل أقل من 1000 حالة محلية المنشأ للإصابة بالمرض 35 بلداً في عام 2021 مقارنة بعددها الذي بلغ 33 بلداً في عام 2020 واقتصر على 13 بلداً في عام 2000.[111] تكون البلدان التي لا تسجل أي حالة محلية المنشأ للإصابة بالملاريا لمدة 3 أعوام متعاقبة على الأقل مؤهلة لتقديم طلب الحصول على إشهاد منظمة الصحة العالمية على القضاء على الملاريا. وقد أعلنت منظمة الصحة العالمية عن تسعة بلدان منذ عام 2015 على خلوها من الملاريا، بما فيها ملديف (2015) وسري لانكا (2016) وقيرغيزستان (2016) وباراغواي (2018) وأوزبكستان (2018) والأرجنتين (2019) والجزائر (2019) والصين (2021) والسلفادور (2021).[111]
المضاعفات
الملاريا لها العديد من المضاعفات الخطيرة . من بين هذه المضاعفات تطور الضائقة التنفسية، التي تحدث في ما يصل إلى 25٪ من البالغين و 40٪ من الأطفال المصابين بالملاريا الشديدة . تشمل الأسباب المحتملة التعويض التنفسي للحماض الاستقلابي، والوذمة الرئوية غير القلبية، والالتهاب الرئوي، وفقر الدم الشديد . على الرغم من ندرتها عند الأطفال الصغار المصابين بالملاريا الشديدة، تحدث متلازمة الضائقة التنفسية الحادة في 5-25٪ من البالغين وما يصل إلى 29٪ من النساء الحوامل.[112] العدوى المرافقة لفيروس نقص المناعة البشرية بالملاريا تزيد من معدل الوفيات.[113] الفشل الكلوي هو سمة من سمات حمى المياه السوداء، حيث يتسرب كميات كبيرة من الهيموجلوبين من خلايا الدم الحمراء المتحللة إلى البول ويظهر البول بلون أسود و تعد من أخطر مراحل الملاريا .[114]
قد تؤدي الإصابة بالمتصورة المنجلية إلى الإصابة بالملاريا الدماغية، وهي شكل من أشكال الملاريا الحادة التي تنطوي على اعتلال دماغي . يرتبط بتبييض الشبكية، والذي قد يكون علامة سريرية مفيدة في تمييز الملاريا عن الأسباب الأخرى للحمى.[115] تضخم الطحال أو تضخم الكبد أو كلاهما، قد يحدث صداع شديد وانخفاض نسبة السكر في الدم وهيموجلوبين في البول مع الفشل الكلوي .[114] قد تشمل المضاعفات النزيف التلقائي، واعتلال التخثر، والصدمة .[116]
تعتبر الملاريا عند النساء الحوامل سببًا مهمًا للإجهاض وانخفاض الوزن عند الولادة ،,[117] خاصة في عدوى المتصورة المنجلية.[118]
ويمكن تلخيض المضاعفات المحتملة في الأتي:
- فقر الدم: نتيجة للتكسير المستمر الذي تسببه الملاريا لكريات الدم الحمراء فإن ذلك قد يسبب حالة من حالات فقر الدم الشديد حيث تصبح كريات الدم الحمراء غير قادرة على حمل كميات كافية من الأكسجين لأنحاء الجسم مما ينتج عنه شعور الجسم بالكسل والضعف والإغماء أحيانًا.
- الملاريا الدماغية: وفي بعض حالات الملاريا النادرة، فإن خلايا الدم الحمراء المصابة بالملاريا تقوم بسد وإغلاق مجرى الأوعية الدموية المؤدية إلى الدماغ وهذا ما يعرف بالأنيميا الدماغية مما يؤدي إلى انتفاخ الدماغ وفي بعض الحالات إلى إصابته بضرر دائم. كما يمكن أن تتسبب في حدوث الصرع (وهو عبارة عن نوبات مرضية تتميز بحدوث انقباضات لاإرادية لعضلات الجسم) أو أن تؤدي إلى دخول المريض في غيبوبة.
- مشاكل في التنفس (مثل تجمع المياه في الرئتين)
- جفاف وحدوث الصدمة
- تعطل وظائف الكبد
- حدوث نزيف تلقائي
- الإصابة بالصفارى (اصفرار لون الجلد نتيجة لزيادة مادة تدعى البيلليروبين في الدم)
- انخفاض مستوى السكر في الدم
- فشل كلوي
- تضخم الطحال.
الفئات المعرّضة للخطر
نصف سكان العالم تقريبًا معرضين لخطر الإصابة بالملاريا. تحدث معظم حالات الإصابات والوفيات في أفريقيا جنوب الصحراء الكبرى، وقد شهد 97 من البلدان والأقاليم استمرار سريان الملاريا في عام 2014.[119]
الفئات المعرّضة للخطر بوجه خاص هي:
احصاءات
في احصائية لمنظمة الصحة العالمية شهد عام 2020م وقوع 241 مليون حالة إصابة بالملاريا في جميع أنحاء العالم.[119] تستأثر دول القارة الإفريقية بالحصة الأكبر من الإصابات.حدث في إفريقيا فقط 95% من حالات الإصابة بالملاريا و96% من الوفيات الناجمة عنها،[119] علماً بأن الأطفال دون سن الخامسة يشكلون نحو 80٪ من مجموع وفيات الملاريا في الإقليم. بلغ العدد التقديري للوفيات الناجمة عن الملاريا 000 627 وفاة في عام 2020.[119]
المآل
عند العلاج المناسب، يمكن للأشخاص المصابين بالملاريا الشفاء بشكل كامل .[120] ومع ذلك، يمكن أن تتطور الملاريا الشديدة بسرعة كبيرة وتسبب الوفاة في غضون ساعات أو أيام.[121] في حالات المرض الشديدة، يمكن أن تصل معدلات الوفيات إلى 20٪، حتى مع العناية المركزة والعلاج.[11] على المدى الطويل تم توثيق إعاقات في النمو لدى الأطفال الذين أصيبوا بنوبات ملاريا حادة.[122] يمكن أن تحدث العدوى المزمنة بدون أعراض مرضية شديدة في متلازمة نقص المناعة المرتبطة بانخفاض الاستجابة لبكتيريا السالمونيلا وفيروس إبشتاين بار .[122]
تتسبب الملاريا بفقر الدم في مرحلة الطفولة خلال فترة نمو الدماغ السريع، مما قد يؤثر على نمو الدماغ.[122] بعض الناجين من الملاريا الدماغية لديهم مخاطر متزايدة للإصابة بالعجز العصبي والمعرفي والاضطرابات السلوكية والصرع .[123] ثبت أن الوقاية من الملاريا تحسن الوظيفة الإدراكية والأداء المدرسي في التجارب السريرية .[122]
اللقاح
لا يوجد لقاح حتى الآن يحاول العلماء في جميع أنحاء العالم تطوير لقاح آمن وفعَّال ضد الملاريا. حتى الآن، ومع ذلك، لا يوجد لقاح ضد الملاريا معتمَد للاستخدام البشري.[111]
الحمل والملاريا
أكدت البحوث أن النساء الحوامل هن أكثر عرضة للإصابة بالملاريا من النساء غير الحوامل، وذلك لأن الجهاز المناعي قد يضعف خلال فترة الحمل، مما يعني أن الجسم أقل قابلية على محاربة البكتريا والالتهابات. وإذا كانت الحامل مصابة بالملاريا، فقد يصاب طفلها أيضا بالمرض عبر المشيمة.
انظر أيضًا
المصادر
- WikiSkripta (بالتشيكية والسلوفاكية), ISSN:1804-6517, QID:Q9049250
- Disease Ontology (بالإنجليزية), 27 May 2016, QID:Q5282129
- http://www.who.int/healthinfo/global_burden_disease/estimates/en/index2.html. اطلع عليه بتاريخ 2016-07-30.
{{استشهاد ويب}}:|url=بحاجة لعنوان (مساعدة) والوسيط|title=غير موجود أو فارغ (من ويكي بيانات) (مساعدة) - محمد هيثم الخياط (2009). المعجم الطبي الموحد (بالعربية والإنجليزية والفرنسية) (ط. الرابعة). بيروت: مكتبة لبنان ناشرون، المكتب الإقليمي لمنظمة الصحة العالمية في الشرق الأوسط. ص. 1196. ISBN:978-9953-86-482-2. OCLC:978161740. QID:Q113466993.
- يوسف حتي؛ أحمد شفيق الخطيب (2011). قاموس حتي الطبي الجديد: طبعة جديدة وموسعة ومعززة بالرسوم إنكليزي - عربي مع ملحقات ومسرد عربي - إنكليزي (بالعربية والإنجليزية) (ط. الأولى). بيروت: مكتبة لبنان ناشرون. ص. 508. ISBN:978-9953-86-883-7. OCLC:868913367. QID:Q112962638.
- المعجم الموحد لمصطلحات علم الأحياء، قائمة إصدارات سلسلة المعاجم الموحدة (8) (بالعربية والإنجليزية والفرنسية)، تونس: مكتب تنسيق التعريب، 1993، ص. 228، OCLC:929544775، QID:Q114972534
- إدوار غالب، الموسوعة في العلوم الطبيعية (ط. الثانية)، دار المشرق، بيروت، ج. الأول، ص.180، يُقابله Malaria
- Walter، Kristin؛ John، Chandy C. (8 فبراير 2022). "Malaria". JAMA. ج. 327 ع. 6: 597. DOI:10.1001/jama.2021.21468. ISSN:0098-7484. PMID:35133414. S2CID:246651569. مؤرشف من الأصل في 2022-12-21.
- Nadjm B، Behrens RH (2012). "Malaria: An update for physicians". Infectious Disease Clinics of North America. ج. 26 ع. 2: 243–59. DOI:10.1016/j.idc.2012.03.010. PMID:22632637.
- "Fact sheet about Malaria". www.who.int (بالإنجليزية). Archived from the original on 2023-01-17. Retrieved 2020-05-06.
- "Malaria vaccine: WHO position paper – January 2016" (PDF). Weekly Epidemiological Record. ج. 91 ع. 4: 33–52. 4 نوفمبر 2016. PMID:26829826. مؤرشف من الأصل (PDF) في 2020-04-23.
- Datoo, Mehreen S.; Magloire Natama, Hamtandi; Somé, Athanase; Traoré, Ousmane; Rouamba, Toussaint; Bellamy, Duncan; Yameogo, Prisca; Valia, Daniel; Tegneri, Moubarak; Ouedraogo, Florence; Soma, Rachidatou (20 Apr 2021). "High Efficacy of a Low Dose Candidate Malaria Vaccine, R21 in 1 Adjuvant Matrix-M, with Seasonal Administration to Children in Burkina Faso" (بالإنجليزية). SSRN:3830681.
- Rawat, Aadish; Roy, Mrinalini; Jyoti, Anupam; Kaushik, Sanket; Verma, Kuldeep; Srivastava, Vijay Kumar (Aug 2021). "Cysteine proteases: Battling pathogenic parasitic protozoans with omnipresent enzymes". Microbiological Research (بالإنجليزية). 249: 126784. DOI:10.1016/j.micres.2021.126784. PMID:33989978. S2CID:234597200. Archived from the original on 2022-12-21.
- "World Malaria Report 2020" (PDF). WHO. مؤرشف من الأصل (PDF) في 2022-12-25.
- Guidelines for the treatment of malaria (ط. 2nd). Geneva: World Health Organization. 2010. ص. ix. ISBN:978-92-4-154792-5.
- Baiden, Frank; Malm, Keziah L.; Binka, Fred (2021). Malaria (بالإنجليزية الأمريكية). Oxford University Press. DOI:10.1093/med/9780198816805.001.0001/med-9780198816805-chapter-73 (inactive 31 Jul 2022). ISBN:978-0-19-185838-3. Archived from the original on 2022-12-21.
{{استشهاد بكتاب}}: صيانة الاستشهاد: وصلة دوي غير نشطة منذ يوليو 2022 (link) - WHO (2021). World Malaria Report 2021. Switzerland: World Health Organization. ISBN:978-92-4-004049-6. مؤرشف من الأصل في 2023-03-18.
- "Malaria parasite life cycle". PATH's Malaria Vaccine Initiative (بالإنجليزية). 19 Nov 2015. Archived from the original on 2023-01-02. Retrieved 2023-01-02.
- World Health Statistics 2010. World Health Organization. 2010. ISBN:9789240684713. OCLC:694342018. مؤرشف من الأصل في 2019-12-14.
- Markus, Miles B. (1 Nov 2011). "Malaria: Origin of the Term "Hypnozoite"". Journal of the History of Biology (بالإنجليزية). 44 (4): 781–786. DOI:10.1007/s10739-010-9239-3. ISSN:1573-0387. Archived from the original on 2020-01-23.
- Nadjm، Behzad؛ Behrens، Ron H. (1 يونيو 2012). "Malaria:: An Update for Physicians". Infectious Disease Clinics of North America. Tropical Diseases. ج. 26 ع. 2: 243–259. DOI:10.1016/j.idc.2012.03.010. ISSN:0891-5520. مؤرشف من الأصل في 2019-12-14.
{{استشهاد بدورية محكمة}}:|archive-date=/|archive-url=timestamp mismatch (مساعدة) - Markus, Miles B. (2018/11). "Biological concepts in recurrent Plasmodium vivax malaria". Parasitology (بالإنجليزية). 145 (13): 1765–1771. DOI:10.1017/S003118201800032X. ISSN:0031-1820. Archived from the original on 2019-04-06.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(help) - Markus, Miles B. (1 Jul 2017). "Malaria Eradication and the Hidden Parasite Reservoir". Trends in Parasitology (بالإنجليزية). 33 (7): 492–495. DOI:10.1016/j.pt.2017.03.002. ISSN:1471-4922. PMID:28366603. Archived from the original on 2019-12-14.
- White، Nicholas J. (11 أكتوبر 2011). "Determinants of relapse periodicity in Plasmodium vivax malaria". Malaria Journal. ج. 10 ع. 1: 297. DOI:10.1186/1475-2875-10-297. ISSN:1475-2875. PMC:3228849. PMID:21989376. مؤرشف من الأصل في 2019-12-14.
{{استشهاد بدورية محكمة}}:|archive-date=/|archive-url=timestamp mismatch (مساعدة)صيانة الاستشهاد: تنسيق PMC (link) صيانة الاستشهاد: دوي مجاني غير معلم (link) - "5.1 Diagnosing Malaria (2015)". WHO Guidelines for Malaria. World Health Organization. 13 يوليو 2021. مؤرشف من الأصل في 2023-03-18. اطلع عليه بتاريخ 2021-11-28.
- Hanboonkunupakarn B، White NJ (فبراير 2022). "Advances and roadblocks in the treatment of malaria". British Journal of Clinical Pharmacology. ج. 88 ع. 2: 374–382. DOI:10.1111/bcp.14474. PMC:9437935. PMID:32656850. S2CID:220502723.
- McIntosh HM، Olliaro P، وآخرون (Cochrane Infectious Diseases Group) (26 أبريل 1999). "Artemisinin derivatives for treating uncomplicated malaria". The Cochrane Database of Systematic Reviews. ج. 1999 ع. 2: CD000256. DOI:10.1002/14651858.CD000256. PMC:6532741. PMID:10796519.
- Pousibet-Puerto J، Salas-Coronas J، Sánchez-Crespo A، Molina-Arrebola MA، Soriano-Pérez MJ، Giménez-López MJ، وآخرون (يوليو 2016). "Impact of using artemisinin-based combination therapy (ACT) in the treatment of uncomplicated malaria from Plasmodium falciparum in a non-endemic zone". Malaria Journal. ج. 15 ع. 1: 339. DOI:10.1186/s12936-016-1408-1. PMC:4930579. PMID:27368160. S2CID:18043747.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - Omari AA، Gamble C، Garner P، وآخرون (Cochrane Infectious Diseases Group) (أبريل 2006). "Artemether-lumefantrine (four-dose regimen) for treating uncomplicated falciparum malaria". The Cochrane Database of Systematic Reviews. ج. 2006 ع. 2: CD005965. DOI:10.1002/14651858.CD005965. PMC:6532603. PMID:16625646.
- Omari AA، Gamble C، Garner P، وآخرون (Cochrane Infectious Diseases Group) (أكتوبر 2005). "Artemether-lumefantrine (six-dose regimen) for treating uncomplicated falciparum malaria". The Cochrane Database of Systematic Reviews. ج. 2005 ع. 4: CD005564. DOI:10.1002/14651858.CD005564. PMC:6532733. PMID:16235412.
- WHO 2010، صفحة 21
- Sinclair D، Zani B، Donegan S، Olliaro P، Garner P، وآخرون (Cochrane Infectious Diseases Group) (يوليو 2009). "Artemisinin-based combination therapy for treating uncomplicated malaria". The Cochrane Database of Systematic Reviews. ج. 2009 ع. 3: CD007483. DOI:10.1002/14651858.CD007483.pub2. PMC:6532584. PMID:19588433.
- Isba R، Zani B، Gathu M، Sinclair D (فبراير 2015). "Artemisinin-naphthoquine for treating uncomplicated Plasmodium falciparum malaria". The Cochrane Database of Systematic Reviews. ج. 2015 ع. 2: CD011547. DOI:10.1002/14651858.CD011547. PMC:4453860. PMID:25702785.
- Isba R، Zani B، Gathu M، Sinclair D، وآخرون (Cochrane Infectious Diseases Group) (فبراير 2015). "Artemisinin-naphthoquine for treating uncomplicated Plasmodium falciparum malaria". The Cochrane Database of Systematic Reviews. ج. 2015 ع. 2: CD011547. DOI:10.1002/14651858.CD011547. PMC:4453860. PMID:25702785.
- Blanshard A، Hine P (يناير 2021). "Atovaquone-proguanil for treating uncomplicated Plasmodium falciparum malaria". The Cochrane Database of Systematic Reviews. ج. 1 ع. 1: CD004529. DOI:10.1002/14651858.CD004529.pub3. PMC:8094970. PMID:33459345.
- van Eijk AM، Terlouw DJ، وآخرون (Cochrane Infectious Diseases Group) (فبراير 2011). "Azithromycin for treating uncomplicated malaria". The Cochrane Database of Systematic Reviews. ج. 2011 ع. 2: CD006688. DOI:10.1002/14651858.CD006688.pub2. PMC:6532599. PMID:21328286.
- McIntosh HM، Jones KL، وآخرون (Cochrane Infectious Diseases Group) (أكتوبر 2005). "Chloroquine or amodiaquine combined with sulfadoxine-pyrimethamine for treating uncomplicated malaria". The Cochrane Database of Systematic Reviews. ج. 2005 ع. 4: CD000386. DOI:10.1002/14651858.CD000386.pub2. PMC:6532604. PMID:16235276.
- Amukoye E، Winstanley PA، Watkins WM، Snow RW، Hatcher J، Mosobo M، وآخرون (أكتوبر 1997). "Chlorproguanil-dapsone: effective treatment for uncomplicated falciparum malaria". Antimicrobial Agents and Chemotherapy. ج. 41 ع. 10: 2261–2264. DOI:10.1128/AAC.41.10.2261. PMC:164103. PMID:9333058.
- Bukirwa H، Garner P، Critchley J، وآخرون (Cochrane Infectious Diseases Group) (أكتوبر 2004). "Chlorproguanil-dapsone for treating uncomplicated malaria". The Cochrane Database of Systematic Reviews. ج. 2004 ع. 4: CD004387. DOI:10.1002/14651858.CD004387.pub2. PMC:6532720. PMID:15495106.
- Graves PM، Choi L، Gelband H، Garner P، وآخرون (Cochrane Infectious Diseases Group) (فبراير 2018). "Primaquine or other 8-aminoquinolines for reducing Plasmodium falciparum transmission". The Cochrane Database of Systematic Reviews. ج. 2018 ع. 2: CD008152. DOI:10.1002/14651858.CD008152.pub5. PMC:5815493. PMID:29393511.
- Bukirwa H، Critchley J، وآخرون (Cochrane Infectious Diseases Group) (يناير 2006). "Sulfadoxine-pyrimethamine plus artesunate versus sulfadoxine-pyrimethamine plus amodiaquine for treating uncomplicated malaria". The Cochrane Database of Systematic Reviews. ج. 2006 ع. 1: CD004966. DOI:10.1002/14651858.CD004966.pub2. PMC:6532706. PMID:16437507.
- Rodrigo C، Rajapakse S، Fernando D (سبتمبر 2020). "Tafenoquine for preventing relapse in people with Plasmodium vivax malaria". The Cochrane Database of Systematic Reviews. ج. 9 ع. 4: CD010458. DOI:10.1002/14651858.CD010458.pub3. PMC:8094590. PMID:32892362.
- Tarning J (مارس 2016). "Treatment of Malaria in Pregnancy". The New England Journal of Medicine. ج. 374 ع. 10: 981–982. DOI:10.1056/NEJMe1601193. PMID:26962733.
- Orton LC، Omari AA، وآخرون (Cochrane Infectious Diseases Group) (أكتوبر 2008). "Drugs for treating uncomplicated malaria in pregnant women". The Cochrane Database of Systematic Reviews. ج. 2008 ع. 4: CD004912. DOI:10.1002/14651858.CD004912.pub3. PMC:6532683. PMID:18843672.
- Kochar DK، Saxena V، Singh N، Kochar SK، Kumar SV، Das A (يناير 2005). "Plasmodium vivax malaria". Emerging Infectious Diseases. ج. 11 ع. 1: 132–4. DOI:10.3201/eid1101.040519. PMC:3294370. PMID:15705338.
- Pasvol G (2005). "The treatment of complicated and severe malaria". British Medical Bulletin. 75–76: 29–47. DOI:10.1093/bmb/ldh059. PMID:16495509.
- "CDC - Malaria - Diagnosis & Treatment (United States) - Treatment (U.S.) - Artesunate". CDC-Centers for Disease Control and Prevention (بالإنجليزية الأمريكية). 11 Apr 2022. Archived from the original on 2023-03-14. Retrieved 2022-04-25.
- Kyu HH، Fernández E (ديسمبر 2009). "Artemisinin derivatives versus quinine for cerebral malaria in African children: a systematic review". Bulletin of the World Health Organization. ج. 87 ع. 12: 896–904. DOI:10.2471/BLT.08.060327. PMC:2789363. PMID:20454480. مؤرشف من الأصل في 2016-03-04.
- De Buck E، Borra V، Carlson JN، Zideman DA، Singletary EM، Djärv T (أبريل 2019). Cochrane Metabolic and Endocrine Disorders Group (المحرر). "First aid glucose administration routes for symptomatic hypoglycaemia". The Cochrane Database of Systematic Reviews. ج. 2019 ع. 4: CD013283. DOI:10.1002/14651858.CD013283.pub2. PMC:6459163. PMID:30973639.
- Idro R، Marsh K، John CC، Newton CR (أكتوبر 2010). "Cerebral malaria: mechanisms of brain injury and strategies for improved neurocognitive outcome". Pediatric Research. ج. 68 ع. 4: 267–74. DOI:10.1203/pdr.0b013e3181eee738. PMC:3056312. PMID:20606600.
- Okoromah CA، Afolabi BB، Wall EC، وآخرون (Cochrane Infectious Diseases Group) (أبريل 2011). "Mannitol and other osmotic diuretics as adjuncts for treating cerebral malaria". The Cochrane Database of Systematic Reviews. ج. 2011 ع. 4: CD004615. DOI:10.1002/14651858.CD004615.pub3. PMC:4018680. PMID:21491391.
- Meremikwu M، Marson AG، وآخرون (Cochrane Infectious Diseases Group) (22 أبريل 2002). "Routine anticonvulsants for treating cerebral malaria". The Cochrane Database of Systematic Reviews. ج. 2002 ع. 2: CD002152. DOI:10.1002/14651858.CD002152. PMC:6532751. PMID:12076440.
- Briggs, Helen (30 July 2014) Call for 'radical action' on drug-resistant malaria نسخة محفوظة 2014-07-31 على موقع واي باك مشين. BBC News, health, Retrieved 30 July 2013
- Gallagher J (23 Jul 2019). "Resistant malaria spreading in South East Asia" (بالإنجليزية البريطانية). Archived from the original on 2023-03-17. Retrieved 2019-07-25.
- "From 30 million cases to zero: China is certified malaria-free by WHO". www.who.int (بالإنجليزية). Archived from the original on 2023-03-14. Retrieved 2022-08-11.
- Athuman M، Kabanywanyi AM، Rohwer AC (يناير 2015). "Intermittent preventive antimalarial treatment for children with anaemia". The Cochrane Database of Systematic Reviews. ج. 1 ع. 1: CD010767. DOI:10.1002/14651858.CD010767.pub2. PMC:4447115. PMID:25582096.
- Schlagenhauf-Lawlor 2008، صفحة 215 "نسخة مؤرشفة". مؤرشف من الأصل في 2023-01-03. اطلع عليه بتاريخ 2023-01-08.
{{استشهاد ويب}}: صيانة الاستشهاد: BOT: original URL status unknown (link) - Instructions for treatment and use of insecticide-treated mosquito nets (PDF). World Health Organization. 2002. ص. 34. مؤرشف (PDF) من الأصل في 2015-07-06.
- Gleave K، Lissenden N، Chaplin M، Choi L، Ranson H (مايو 2021). "Piperonyl butoxide (PBO) combined with pyrethroids in insecticide-treated nets to prevent malaria in Africa". The Cochrane Database of Systematic Reviews. ج. 5 ع. 5: CD012776. DOI:10.1002/14651858.CD012776.pub3. PMC:8142305. PMID:34027998.
- Pryce J، Medley N، Choi L (يناير 2022). "Indoor residual spraying for preventing malaria in communities using insecticide-treated nets". The Cochrane Database of Systematic Reviews. ج. 1 ع. 1: CD012688. DOI:10.1002/14651858.CD012688.pub3. PMC:8763033. PMID:35038163.
- Pryce J، Choi L، Richardson M، Malone D، وآخرون (Cochrane Infectious Diseases Group) (نوفمبر 2018). "Insecticide space spraying for preventing malaria transmission". The Cochrane Database of Systematic Reviews. ج. 11 ع. 11: CD012689. DOI:10.1002/14651858.CD012689.pub2. PMC:6516806. PMID:30388303.
- Shah MP، Hwang J، Choi L، Lindblade KA، Kachur SP، Desai M (سبتمبر 2021). "Mass drug administration for malaria". The Cochrane Database of Systematic Reviews. ج. 2021 ع. 9: CD008846. DOI:10.1002/14651858.CD008846.pub3. PMC:8479726. PMID:34585740.
- Radeva-Petrova D، Kayentao K، ter Kuile FO، Sinclair D، Garner P (أكتوبر 2014). "Drugs for preventing malaria in pregnant women in endemic areas: any drug regimen versus placebo or no treatment". The Cochrane Database of Systematic Reviews. ج. 10 ع. 10: CD000169. DOI:10.1002/14651858.CD000169.pub3. PMC:4498495. PMID:25300703.
- Esu EB، Oringanje C، Meremikwu MM (يوليو 2021). "Intermittent preventive treatment for malaria in infants". The Cochrane Database of Systematic Reviews. ج. 2021 ع. 7: CD011525. DOI:10.1002/14651858.CD011525.pub3. PMC:8406727. PMID:34273901.
- González R، Pons-Duran C، Piqueras M، Aponte JJ، Ter Kuile FO، Menéndez C، وآخرون (Cochrane Infectious Diseases Group) (نوفمبر 2018). "Mefloquine for preventing malaria in pregnant women". The Cochrane Database of Systematic Reviews. ج. 11 ع. 11: CD011444. DOI:10.1002/14651858.CD011444.pub3. PMC:6517148. PMID:30480761.
- Mathanga DP، Uthman OA، Chinkhumba J، وآخرون (Cochrane Infectious Diseases Group) (أكتوبر 2011). "Intermittent preventive treatment regimens for malaria in HIV-positive pregnant women". The Cochrane Database of Systematic Reviews. ج. 2011 ع. 10: CD006689. DOI:10.1002/14651858.CD006689.pub2. PMC:6532702. PMID:21975756.
- Palmer J. "WHO gives indoor use of DDT a clean bill of health for controlling malaria". WHO. مؤرشف من الأصل في 2012-10-22.
- "الملاريا". www.who.int. مؤرشف من الأصل في 2022-09-13. اطلع عليه بتاريخ 2023-04-07.
- Davidson's Principles and Practice of Medicine/21st/351
- منظمة الصحة العالمية | الملاريا نسخة محفوظة 22 سبتمبر 2017 على موقع واي باك مشين.
- بوابة تمريض
- بوابة طب
- بوابة علم الأحياء