حيوان منوي
الحيوان المنوي أو النُطْفة (الاسم العلمي: Sperm)،(1) هو الخلية التناسلية الذكريّة[1] (الجاميت) في أشكالٍ متفاوتة الجاميتات من التكاثر الجنسي (الأشكال التي تتضمن خليةً تناسليةً أنثويةً أكبر وخلية ذكرية أصغر). تكون الحيوانات المنوية متحركةً مع ذيلٍ يُسمى السوط، حيث تُسمى في هذه المرحلة بالحيوانات المنوية المتحركة (الاسم العلمي: spermatozoa)، ولكنَّ بعض الطحالب الحمراء والفطريات تُنتج خلايًا منوية غير متحركةٍ تُسمى الأبواغ الذكرية (الاسم العلمي: spermatia).[2] تحتوي كاسيات البذور على حيواناتٍ منويةٍ غير متحركةٍ داخل حبوب اللقاح، بينما تحتوي بعض النباتات القاعدية مثل السراخس وبعض عاريات البذور على حيواناتٍ منوية متحركة.[3]
تتشكل خلايا الحيوانات المنوية أثناء عمليةٍ تُعرف باسم تكون الحيوانات المنوية (الاسم العلمي: spermatogenesis)، والتي تحدث في السلويات (الزواحف والثدييات) داخل النُّبَيبات الناقلة للمني في الخصيتين.[4] تتضمن هذه العملية إنتاج العديد من سلائف الخلايا المنوية المتتالية، بدءًا من البزرة، والتي تتمايز لتصبح خلايًا منوية [الإنجليزية]، والتي تخضع بدورها لانقسامٍ منصف، مما يُقلل من عدد كروموسوماتها بمقدار النصف، لتنتج عنه الطلائع المنوية، حيث تنضح بدورها، فتكون ذيلًا أو سوطًا في الإنسان والحيوانات، مما يؤدي إلى نشوء خليةٍ منويةٍ ناضجةٍ مُتحركة. تحدث هذه العملية كاملةً بشكلٍ مستمرٍ، كما تستغرق حوالي 3 أشهر من البداية حتى النهاية.
لا تستطيع الحيوانات المنوية الانقسام، كما يكون عُمرها محددًا. ولكن بعد اندماجها مع البويضات أثناء الإخصاب، يبدأ كائنٌ حيٌ جديدٌ بالنماء، حيث يبدأ بويضةً مخصبةً (زيجوتًا) شامِلُة الوُسْع. يكون الحيوان المنوي البشري فَرْدانيًّا (أحادي الكروموسومات)، بحيث يُمكن للكروموسومات البالغ عددها 23 أن تنضم إلى 23 كروموسومًا في البويضة الأنثوية، وذلك لتكوين ضِعْفانِيٍّ (ثنائي الكروموسومات) يحتوي على 46 كروموسومًا زوجيًا. تُخزن الحيوانات المنوية في بربخ الثدييات [الإنجليزية]، حيث تخرجُ من القضيب خلال القذف على شكل سائلٍ يُسمى المَنِيّ (الاسم العلمي: semen).
اشتُقت كلمة «sperm» من الكلمة الإغريقية «σπέρμα»، والتي تعني البِزْرَة (بالإنجليزية: seed).
التطور
من المقبول عمومًا أن الإِنْسال مُتماثل الجاميتات هو سلف الحيوانات المنوية والبويضات. ومع ذلك، لا توجد سجلاتٌ أحفورية لتطور الحيوانات المنوية والبويضات من الإِنْسال مُتماثل الجاميتات، مما يؤدي إلى التركيز على النماذج الرياضية لفهم تطور الحيوانات المنوية.[5]
تنصُ فرضية واسعة الانتشار على أنَّ الحيوانات المنوية تطورت بسرعة. ومع ذلك، لا يوجد دليلٌ مباشر [الإنجليزية] على أنَّ الحيوانات المنوية قد تطورت بمعدلٍ سريعٍ أو قبل الخصائص الذكرية الأخرى.[6]
في الإنسان والحيوانات
الوظيفة
تتمثل الوظيفة الرئيسية للحيوانات المنوية في الوصول إلى البويضة والاندماج معها، وذلك لتوصيل بنيتين خلويتين فرعيتين: الأولى هي النواة الأولية الذكرية التي تحتوي على المادة الوراثية، والثانية هي المريكزات، وهي هياكلٌ تُساعد على تنظيم الهيكل الخلوي للأنيبيبات الدقيقة.
التشريح
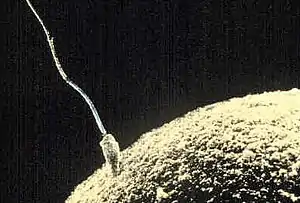

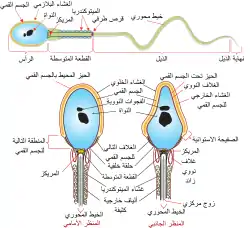
يتكون الحيوان المنوي في الثدييات من جزأين:
- الرأس: يحتوي على نواةٍ مع أليافٍ كروماتينية ملفوفةٌ بكثافةٍ، ويُحاط من الأمام بجرابٍ رفيعٍ مسطحٍ يسمى الجسيم القمي، والذي يحتوي على إنزيماتٍ تُستخدم لاختراق بويضة الأنثى. كما يحتوي أيضًا على فجواتٍ.[7]
- الذيل: يُطلق عليه أيضًا اسم السوط، وهو أطول جزءٍ ويتحرك بشكلٍ يُشبه الموجة، حيث تدفعه للسباحة وتساعده في اختراق البويضة.[8][9][10] كان يُعتقد سابقًا أن الذيل يتحرك بشكلٍ متماثلٍ للشكل الحلزوني.
يحتوي العُنق أو القطعة الواصلة على مريكزٍ واحدٍ نمطي وآخرٍ غيرُ نمطي مثل المُرَيكِز شبيه الداني [الإنجليزية].[11][12] يحتوي الجُزء الأوسط على لبٍ خيطيٍ مركزيٍ فيه العديد من الميتوكوندريا المُلتفة حوله، ويُستخدم لإنتاج الأدينوسين ثلاثي الفوسفات (ATP) للمسار عبر عنق الرحم والرحم وقناة الرحم في الإناث.
أثناء الإخصاب، يُوفر الحيوان المنوي ثلاثة أجزاءٍ أساسيةٍ للخلية البويضية، وهي: أولًا، عامل الإشارة أو التنشيط، مما يؤدي إلى تنشيط البويضة الساكنة أيضيًا. ثانيًا، المجموع المورثي (الجينوم) الأبوي أُحادي الصيغة الصبغية (أو الكروموسومية). ثالثًا، المريكز، وهو المسؤول عن تكوين الجسيم المركزي ونظام الأنيبيبات الدقيقة.[13]
المنشأ
تُنتج الحيوانات المنوية المُتحركة في الإنسان والحيوانات عبر عمليةٍ تُعرف باسم تكوين الحيوانات المنوية، والتي تحدث داخل الغدد التناسلية الذكرية (الخصيتين) عبر الانقسام المنصف. يستغرق اكتمال عملية تكوين الحيوانات المنوية الأولية حوالي 70 يومًا. تبدأ العملية بإنتاج البزرة من سلائف الخلايا الجنسية، والتي تنقسم وتتمايز إلى خلايًا منوية [الإنجليزية]، وتخضع بعدها للانقسام المنصف لتشكيل طليعة الحيوان المنوي. في هذه المرحلة، يطور الحيوان المنوي ذيلًا. تستغرق المرحلة التالية حيث يصبح ناضجًا تمامًا حوالي 60 يومًا، ويُعرف آنذاك بالحيوان المنوي الأولي.[14] تخرج خلايا الحيوانات المنوية من جسم الذكر في سائلٍ يُعرف باسم السائل المنوي (المني). يُمكن لخلايا الحيوانات المنوية البشرية البقاء على قيد الحياة داخل الجهاز التناسلي الأنثوي لأكثر من 5 أيام بعد الجماع.[15] يُنتج السائل المنوي في الحويصلات المنوية والبروستاتا والغدد الإحليلية.
ادعى علماءٌ في جامعة نانجينغ الطبية [الإنجليزية] عام 2016 أنهم أنتجوا خلايًا تُشبه طليعة الحيوانات المنوية للفئران باستعمال خلايًا جذعية جنينية للفأر بشكلٍ اصطناعي. حقنوا هذه الطلائع المنوية في بويضات الفئران وأنتجوا الجراء.[16]
الكفاءة

تُعد كمية وكفاءة الحيوانات المنوية العوامل الرئيسية في جودة السائل المنوي، وهو مقياسٌ لقدرة السائل المنوي على إحداث الإخصاب. بالتالي، تُعد مقياسًا للخصوبة عند الرجال في البشر. عادةً ما تنخفض الكفاءة الجينية للحيوانات المنوية، فضلاً عن حجمها وحركتها، مع تقدم العمر.[17]
يمكن إصلاح أضرار الحمض النووي الرايبوزي منقوص الأكسجين (الدنا) الموجودة في خلايا الحيوانات المنوية في الفترة التي تلي الانقسام المنصف ولكن قبل الإخصاب في البويضة المخصبة، ولكن إذا لم تُصلح، فإنها قد تؤدي إلى آثارٍ ضارةٍ خطيرةٍ على الخصوبة والجنين النامي. تُعد خلايا الحيوانات المنوية البشرية معرضةً بشكلٍ خاص لهجمات الجذور الحرة وإحداثٍ ضررٍ مؤكسدٍ للدنا.[18]
إنَّ مرحلة ما بعد الانقسام المنصف في تكوين الحيوانات المنوية لدى الفئران تُعد حساسةً جدًا للعوامل البيئية السامة للجينات؛ وذلك لأنَّ الخلايا الجنسية الذكرية تُشكل حيواناتٍ منويةٍ ناضجةٍ، ولكنها تفقد تدريجيًا القدرة على إصلاح تلف الدنا.[19] قد يؤدي تعريض ذكور الفئران إلى الإشعاع أثناء تكوين الحيوانات المنوية المتأخر إلى تلفٍ يستمر لمدة 7 أيام على الأقل في خلايا الحيوانات المنوية المُخصبة، كما يؤدي تعطيل مسارات إصلاح كسر الشرائط المزدوجة للحمض النووي للأم إلى زيادة الانحرافات الكرومومسومية المُشتقة من خلايا الحيوانات المنوية.[20] يؤدي علاج ذكور الفئران بالميلفالان، وهو عامل مؤلكلٌ ثنائيُ الوظيفة يُستخدم كثيرًا في العلاج الكيميائي، يتسبب في حدوث آفاتٍ في الدنا أثناء الانقسام المنصف، والتي قد تستمر في حالةٍ تالفة حيث تتقدم الخلايا الجنسية عبر مراحل تطور تكوين الحيوانات المنوية التي تكون قادرة على إصلاح الدنا.[21] قد يؤدي تلف الدنا في خلايا الحيوانات المنوية بعد الإخصاب، إلى إنجابٍ نسلٍ يُعاني من تشوهاتٍ مُختلفة.
الحجم
يرتبط حجم الحيوانات المنوية بكفاءتها، وذلك على الأقل في بعض الحيوانات. مثلًا، يصل طول الحيوانات المنوية في بعض أنواع ذبابة الفاكهة إلى 5.8 سم، أي حوالي 20 ضعف طول الذبابة نفسها. تُعد خلايا الحيوانات المنوية الأطول أفضل من نظيراتها الأقصر في إبعاد المنافسين عن المستلم المنوي الأنثوي. يُعود هذا على الإناث بالفائدة، حيث أنَّ الذكور الأصحاء فقط هم من يحملون الجينات «الجيدة» التي يُمكنها إنتاج حيواناتٍ منويةٍ طويلة بكمياتٍ كافيةٍ للتغلب على منافسيها.[22][23]
أسواق الحيوانات المنوية البشرية
تحتوي بعض بنوك الحيوانات المنوية على ما يصل إلى 170 لترًا (37 غالونًا إمبراطوريًا، أي 45 غالونًا أمريكيًا) من الحيوانات المنوية.[24]
يُمكن استخراج الحيوانات المنوية عبر القذف، وأيضًا باستعمال تقنية استخراج الحيوانات المنوية الخصوي [الإنجليزية] (اختصارًا TESE).
تمتلك الدنمارك نظامًا متطورًا لتصدير الحيوانات المنوية البشرية على مستوى الأسواق العالمية، ويأتي هذا النجاح أساسًا من سُمعة المتبرعين الدنماركيين بالحيوانات المنوية؛ وذلك كونَّ هذه الحيوانات تتمع بكفاءةٍ عالية،[25] وذلك على عكس القانون في بلدان شمال أوروبا الأخرى، حيث يُمنح المتبرعون حرية الاختيار في أن يكونوا مجهولين أو غير مجهولين للزوجين المتلقيين.[25] إضافةً لهذا، فإنَّ المتبرعين في بلدان شمال أوروبا عادةً ما يكونوا طويلي القامة وحاملين لشهاداتٍ عُليا[26] ولديهم دوافع إيثارية لتبرعاتهم،[26] ويرجع ذلك جزئيًا إلى التعويضات النقدية المنخفضة نسبيًا في دول الشمال. تستورد أكثر من 50 دولة حول العالم الحيوانات المنوية الدنماركية، وتتضمن الباراغواي وكندا وكينيا وهونغ كونغ.[25] ومع ذلك، فقد حظرت إدارة الغذاء والدواء الأمريكية (FDA) استيراد أي حيوانٍ منويٍ؛ وذلك بسبب خطر انتقال مرض كروتزفيلد جاكوب، على الرغم من أنَّ هذا الخطر ضئيلٌ، حيث أنَّ الإمناء الاصطناعي يختلف تمامًا عن طريق انتقال مرض كروتزفيلد جاكوب.[27] يبلغُ معدل انتشار هذا المرض بين المتبرعين واحدًا في المليون على الأكثر، وإذا كان المتبرع ناقلًا، فلا يزال يتعين على البروتينات المٌعدية عبور الحاجز الدموي الخصوي [الإنجليزية] ليكون انتقال المرض ممكنًا.[27]
التاريخ
لُوحظ وجود الحيوانات المنوية للمرة الأولى في عام 1677 بواسطة أنطوني فان ليفينهوك[28] باستخدام المجهر، وكان قد وصفها بأنها حييويناتٌ (حيواناتٌ صغيرة)، وربما يُرجع ذلك إلى اعتقاده بالتكون المسبق للكائنات، والذي يتحدث أنَّ كل حيوانٍ منويٍ يحتوي على إنسانٍ مُكتمل التكوين ولكنه صغير.[بحاجة لمصدر]
التحليل الشرعي
تُستعمل الأشعة فوق البنفسجية للكشف عن "السوائل المقذوفة"، وذلك بغض النظر عن بنية السطح أو لونِه.[29] أما رؤوس الحيوانات المنوية، مثلًا في المسحات المهبلية، يُكشف عنها عن طريق الفحص المجهري باستخدام طريقة صبغة شجرة عيد الميلاد (الاسم العلمي: Christmas Tree Stain)، والتي تُسمى أيضًا صبغة كيرنشتروت بيكروينديجوكارمين (اختصارًا KPIC).[30][31]
في النباتات
تُنتج الحيوانات المنوية في الطحالب والعديد من النابتات العرسية في معرساتٍ [الإنجليزية] (معفرات) عبر الانقسام المتساوِ. أما في النباتات المزهرة، فإنها تُنتج داخل حبوب اللقاح.[32]
حيوانات منوية متحركة

تتحرك الحيوانات المنوية المُتحركة عادةً عبر الأسواط، ولكنها تحتاج لوسطٍ مائي لتسبح فيه نحو البويضة لإخصابها. تُستمد معظم الطاقة اللازمة لحركة الحيوانات المنوية في البشر والحيوانات من أيض الفركتوز الموجود في السائل المنوي. يحدث هذا في الميتوكوندريا الموجودة في الجزء الأوسط من الحيوانات المنوية (عند قاعدة رأس الحيوان المنوي). لا تستطيع هذه الخلايا السباحة للخلف بسبب طبيعة دفعها. يُشار إلى خلايا الحيوانات المنوية وحيدة السوط في الحيوانات باسم الحيوانات المنوية المتحركة (الاسم العلمي: spermatozoa)، وتختلف في الحجم.[بحاجة لمصدر]
تُنتج الحيوانات المنوية المتحركة أيضًا في العديد من الطلائعيات والنابتات العرسية من الطحلبيات والسراخس وبعض عاريات البذور مثل النخل السرخسي والجنكة. تُعد خلايا الحيوانات المنوية الخلايا الوحيدة التي تمتلك أسواطًا في دورة حياة هذه النباتات. تكون هذه الخلايا متعددة الأسواط في العديد من السراخس والنباتات الذئبية والنخل السرخسي والجنكة.[33]
تتحرك خلايا الحيوانات المنوية في الديدان الأسطوانية عبر الحركة الأميبية، حيث تزحف باتجاه خلية البويضة بدلًا من السباحة نحوها.[34]
حيوانات منوية غير متحركة
تُسمى الحيوانات المنوية غير المتحركة بالأبواغ الذكرية (الاسم العلمي: spermatia)، وهي لا تمتلكُ أسواطًا، وبالتالي غير قادرةٍ على السباحة. تُنتج هذه الحيوانات المنوية في المعرس [الإنجليزية].[33]
نظرًا لأنَّ الأبواغ الذكرية لا تستطيع السباحة، فإنها تُعتمد على بيئتها لنقلها نحو خلية البويضة. تُنتج بعض الطحالب الحمراء، مثل الطحالب الحمر، حيواناتٍ منويةٍ غيرُ متحركةٍ تنتشر عبر التيارات المائية بعد إطلاقها.[33] تكون الأبواغ الذكرية في الشقرانيات مغطاةً بمادةٍ لزجةٍ، حيث تُنتج في هياكل تُشبه القارورة تحتوي على رحيق، والتي تجذب الذباب الذي ينقل الأبواغ الذكرية إلى خيوطٍ فطريةٍ قريبة للإخصاب، ويكون هذا في آليةٍ مشابهةٍ لتلقيح الحشرات في النباتات المزهرة.[35]
قد يُخلط بين الأبواغ الذكرية الفطرية مع الغبيرات، وهي أبواغٌ تنبتُ بشكلٍ مستقل عن الإخصاب، في حين أنَّ الأبواغ الذكرية هي جاميتاتٌ مطلوبةٌ للإخصاب. تتطابق الأبواغ الذكرية في بعض الفطريات، مثل العصيباء المبوغة السميكة، مع الغبيرات، حيث يمكنها أداء وظيفتي الإخصاب وكذلك إنتاج كائناتٍ حيةٍ جديدة بدون إخصاب.[36]
النواة
في جميع النباتات الجنينية تقريبًا، بما في ذلك مُعظم عاريات البذور وجميع كاسيات البذور، فإنَّ النابتات العرسية الذكرية (حبوب اللقاح) تُعد الشكل الأساسي للانتشار الحيوي، على سبيل المثال عن طريق التأبير بالرياح أو الحشرات، مما يُلغي الحاجة إلى الماء لسد الفجوة بين الذكر والأنثى. تحتوي كل حبة لقاح على خلية منوية (مُولدة). بمجرد هبوط حبوب اللقاح على ميسم الزهرة المستقبلة، فإنها تُنبت وتبدأ في إنماء أنبوب اللقاح عبر المتاع، وقبل أن يصل الأنبوب إلى البويضة النباتية، تنقسم نواة الخلية المُنتجة في حبوب اللقاح وتنتج نواتين من الحيوانات المنوية، ثم تُفرغ من خلال الأنبوب إلى البويضة للإخصاب.[33]
في بعض الطلائعيات، يتضمن الإخصاب أيضًا هجرة نوى الحيوانات المنوية، بدلًا من الخلايا، نحو خلية البويضة من خلال أنبوب الإخصاب. تُشكل الطلائعيات البيضية نوى الحيوانات المنوية في معفرٍ ملتحمٍ خلويٍ يُحيط بخلايا البويضة. تصل نوى الحيوانات المنوية إلى البويضات عبر أنابيب الإخصاب، وذلك على غرار آلية أنبوب اللقاح في النباتات.[33]
المريكزات
تحتوي معظم خلايا الحيوانات المنوية على مريكزاتٍ في عنقها.[37] تحتوي الحيوانات المنوية للعديد من الحيوانات على مريكزان نموذجيان يعرفان باسم المريكز الدانٍ والمريكز القاصِ. يمتلك الإنسان وبعض الحيوانات مثل والأبقار مريكزًا نموذجيًا واحدًا، يُعرف باسم المريكز الدانِ، ومريكز ثانٍ له بنيةٌ غير نمطية. ليس لدى الفئران والجرذان مريكزاتٍ يمكن تحديدها في الحيوانات المنوية. تمتلك ذبابة الفاكهة الشائعة (الاسم العلمي: Drosophila melanogaster) مريكزًا واحدًا ومريكزًا غيرُ نمطيٍ يُسمى المُريكز شبيه الدانِ.[38]
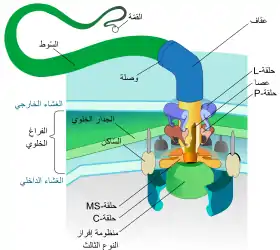
تكون الذيل
يُعد ذيل الحيوانات المنوية نوعًا مُتخصصًا من الهَدَبُ (المعروف أيضًا باسم السوط). يتكون الذيل في العديد من الحيوانات بطريقةٍ فريدة، والتي تسمى تكون الأهداب العصاري الخلوي [الإنجليزية]، حيث يتشكلُ كل أو جزء من الخيط المحوري من ذيل الحيوانات المنوية في السيتوبلازم أو تتعرض له.[39]
الهوامش
انظر أيضًا
المراجع
باللغة الإنجليزية
- المعجم الموحد لمصطلحات علم الأحياء، قائمة إصدارات سلسلة المعاجم الموحدة (8) (بالعربية والإنجليزية والفرنسية)، تونس العاصمة: مكتب تنسيق التعريب، 1993، ص. 319، OCLC:929544775، QID:Q114972534
- "Spermatium definition and meaning | Collins English Dictionary". www.collinsdictionary.com (بالإنجليزية). Archived from the original on 2021-05-01. Retrieved 2020-02-20.
- Kumar, Anil (2006). Botany for Degree Gymnosperm (بالإنجليزية) (Multicolor ed.). S. Chand Publishing. p. 261. ISBN:978-81-219-2618-8. Archived from the original on 31 كانون الثاني 2022. Retrieved 31 كانون الثاني 2022.
{{استشهاد بكتاب}}: تحقق من التاريخ في:|تاريخ الوصول=and|تاريخ أرشيف=(help) - "Animal reproductive system - Male systems". Encyclopedia Britannica (بالإنجليزية). Archived from the original on 31 كانون الثاني 2022. Retrieved 2020-02-20.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ أرشيف=(help) - Pitnick, Scott S.; Hosken, Dave J.; Birkhead, Tim R. (21 Nov 2008). Sperm Biology: An Evolutionary Perspective (بالإنجليزية). Academic Press. pp. 43–44. ISBN:978-0-08-091987-4. Archived from the original on 2022-02-01. Retrieved 2022-02-01.
- Fitzpatrick، John L.؛ Bridge، C. Daisy؛ Snook، Rhonda R. (12 أغسطس 2020). "Repeated evidence that the accelerated evolution of sperm is associated with their fertilization function". Proceedings of the Royal Society B: Biological Sciences. ج. 287 ع. 1932: 20201286. DOI:10.1098/rspb.2020.1286. PMC:7575512. PMID:32752988.
- Boitrelle، F؛ Guthauser، B؛ Alter، L؛ Bailly، M؛ Wainer، R؛ Vialard، F؛ Albert، M؛ Selva، J (2013). "The nature of human sperm head vacuoles: a systematic literature review". Basic Clin Androl. ج. 23: 3. DOI:10.1186/2051-4190-23-3. PMC:4346294. PMID:25780567.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: دوي مجاني غير معلم (link) - Fawcett, D. W. (1981) Sperm Flagellum. In: The Cell. D. W. Fawcett. Philadelphia, W. B. Saunders Company. 14: pp. 604-640.
- Lehti, M. S. and A. Sironen (2017). "Formation and function of sperm tail structures in association with sperm motility defects." Bi
- Ishijima، Sumio؛ Oshio، Shigeru؛ Mohri، Hideo (1986). "Flagellar movement of human spermatozoa". Gamete Research. ج. 13 ع. 3: 185–197. DOI:10.1002/mrd.1120130302.
- Fishman، Emily L؛ Jo، Kyoung؛ Nguyen، Quynh P. H؛ Kong، Dong؛ Royfman، Rachel؛ Cekic، Anthony R؛ Khanal، Sushil؛ Miller، Ann L؛ Simerly، Calvin؛ Schatten، Gerald؛ Loncarek، Jadranka؛ Mennella، Vito؛ Avidor-Reiss، Tomer (2018). "A novel atypical sperm centriole is functional during human fertilization". Nature Communications. ج. 9 ع. 1: 2210. Bibcode:2018NatCo...9.2210F. DOI:10.1038/s41467-018-04678-8. PMC:5992222. PMID:29880810.
- Blachon، S؛ Cai، X؛ Roberts، K. A؛ Yang، K؛ Polyanovsky، A؛ Church، A؛ Avidor-Reiss، T (2009). "A Proximal Centriole-Like Structure is Present in Drosophila Spermatids and Can Serve as a Model to Study Centriole Duplication". Genetics. ج. 182 ع. 1: 133–44. DOI:10.1534/genetics.109.101709. PMC:2674812. PMID:19293139.
- Hewitson, Laura & Schatten, Gerald P. (2003). "The biology of fertilization in humans". في Patrizio, Pasquale؛ وآخرون (المحررون). A color atlas for human assisted reproduction: laboratory and clinical insights. Lippincott Williams & Wilkins. ص. 3. ISBN:978-0-7817-3769-2. مؤرشف من الأصل في 2022-02-03. اطلع عليه بتاريخ 2013-11-09.
- "Semen and sperm quality". مؤرشف من الأصل في 10 تشرين الثاني 2000. اطلع عليه بتاريخ 24 كانون الأول 2017.
{{استشهاد ويب}}: تحقق من التاريخ في:|تاريخ الوصول=و|تاريخ أرشيف=(مساعدة) - Gould، JE؛ Overstreet، JW؛ Hanson، FW (1984). "Assessment of human sperm function after recovery from the female reproductive tract". Biology of Reproduction. ج. 31 ع. 5: 888–894. DOI:10.1095/biolreprod31.5.888. PMID:6518230.
- Cyranoski، David (2016). "Researchers claim to have made artificial mouse sperm in a dish". Nature. DOI:10.1038/nature.2016.19453. S2CID:87014225.
- Gurevich، Rachel (10 يونيو 2008). "Does Age Affect Male Fertility?". About.com. مؤرشف من الأصل في 2015-09-28. اطلع عليه بتاريخ 2010-02-14.
- Gavriliouk D، Aitken RJ (2015). "Damage to Sperm DNA Mediated by Reactive Oxygen Species: Its Impact on Human Reproduction and the Health Trajectory of Offspring". The Male Role in Pregnancy Loss and Embryo Implantation Failure. Advances in Experimental Medicine and Biology. ج. 868. ص. 23–47. DOI:10.1007/978-3-319-18881-2_2. ISBN:978-3-319-18880-5. PMID:26178844.
- Marchetti F، Wyrobek AJ (2008). "DNA repair decline during mouse spermiogenesis results in the accumulation of heritable DNA damage". DNA Repair. ج. 7 ع. 4: 572–81. DOI:10.1016/j.dnarep.2007.12.011. PMID:18282746. مؤرشف من الأصل في 30 كانون الثاني 2022. اطلع عليه بتاريخ 6 شباط 2022.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ أرشيف=(مساعدة) - Marchetti F، Essers J، Kanaar R، Wyrobek AJ (2007). "Disruption of maternal DNA repair increases sperm-derived chromosomal aberrations". Proceedings of the National Academy of Sciences of the United States of America. ج. 104 ع. 45: 17725–9. Bibcode:2007PNAS..10417725M. DOI:10.1073/pnas.0705257104. PMC:2077046. PMID:17978187.
- Marchetti F، Bishop J، Gingerich J، Wyrobek AJ (2015). "Meiotic interstrand DNA damage escapes paternal repair and causes chromosomal aberrations in the zygote by maternal misrepair". Scientific Reports. ج. 5: 7689. Bibcode:2015NatSR...5E7689M. DOI:10.1038/srep07689. PMC:4286742. PMID:25567288.
- Lüpold، Stefan؛ Manier، Mollie K؛ Puniamoorthy، Nalini؛ Schoff، Christopher؛ Starmer، William T؛ Luepold، Shannon H. Buckley؛ Belote، John M؛ Pitnick، Scott (2016). "How sexual selection can drive the evolution of costly sperm ornamentation". Nature. ج. 533 ع. 7604: 535–8. Bibcode:2016Natur.533..535L. DOI:10.1038/nature18005. PMID:27225128. S2CID:4407752. مؤرشف من الأصل في 2020-08-07. اطلع عليه بتاريخ 2022-02-02.
- Gardiner، Jennifer R (2016). "The bigger, the better". Nature. ج. 533 ع. 7604: 476. DOI:10.1038/533476a. PMID:27225117.
- Sarfraz Manzoor (2 نوفمبر 2012). "Come inside: the world's biggest sperm bank". The Guardian. مؤرشف من الأصل في 2019-05-01. اطلع عليه بتاريخ 2013-08-04.
- Assisted Reproduction in the Nordic Countries نسخة محفوظة 11 تشرين الثاني 2013 على موقع واي باك مشين. ncbio.org
- FDA Rules Block Import of Prized Danish Sperm نسخة محفوظة 7 شباط 2022 على موقع واي باك مشين. Posted Aug 13, 08 7:37 AM CDT in World, Science & Health
- Steven Kotler (26 September 2007). "The God of Sperm". مؤرشف من الأصل في 26 حزيران 2018. اطلع عليه بتاريخ 26 نيسـان 2018.
{{استشهاد بخبر}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - "Timeline: Assisted reproduction and birth control". CBC News. مؤرشف من الأصل في 28 نيسـان 2016. اطلع عليه بتاريخ 2006-04-06.
{{استشهاد بخبر}}: تحقق من التاريخ في:|تاريخ أرشيف=(مساعدة) - Fiedler، Anja؛ Rehdorf، Jessica؛ Hilbers، Florian؛ Johrdan، Lena؛ Stribl، Carola؛ Benecke، Mark (2008). "Detection of Semen (Human and Boar) and Saliva on Fabrics by a Very High Powered UV-/VIS-Light Source". The Open Forensic Science Journal. ج. 1: 12–15. DOI:10.2174/1874402800801010012.
- Allery، J. P؛ Telmon، N؛ Mieusset، R؛ Blanc، A؛ Rougé، D (2001). "Cytological detection of spermatozoa: Comparison of three staining methods". Journal of Forensic Sciences. ج. 46 ع. 2: 349–51. DOI:10.1520/JFS14970J. PMID:11305439.
- Illinois State Police/President's DNA Initiative. "The Presidents's DNA Initiative: Semen Stain Identification: Kernechtrot" (PDF). مؤرشف من الأصل (PDF) في 2016-12-26. اطلع عليه بتاريخ 2009-12-10.
- Phatlane William Mokwala؛ Phetole Mangena (6 يونيو 2018). Pollination in Plants. BoD – Books on Demand. ص. 8. ISBN:978-1-78923-236-3. مؤرشف من الأصل في 2022-02-10. اطلع عليه بتاريخ 2022-02-10.
- Raven، Peter H.؛ Ray F. Evert؛ Susan E. Eichhorn (2005). Biology of Plants, 7th Edition. New York: W.H. Freeman and Company Publishers. ISBN:0-7167-1007-2.
- Bottino D, Mogilner A, Roberts T, Stewart M, Oster G (2002). "How nematode sperm crawl". Journal of Cell Science. ج. 115 ع. Pt 2: 367–84. DOI:10.1242/jcs.115.2.367. PMID:11839788.
{{استشهاد بدورية محكمة}}: صيانة الاستشهاد: أسماء متعددة: قائمة المؤلفين (link) - Sumbali، Geeta (2005). The Fungi. Alpha Science Int'l Ltd. ISBN:1-84265-153-6.
- Maheshwari R (1999). "Microconidia of Neurospora crassa". Fungal Genetics and Biology. ج. 26 ع. 1: 1–18. DOI:10.1006/fgbi.1998.1103. PMID:10072316.
- Avidor-Reiss، T؛ Khire، A؛ Fishman، EL؛ Jo، KH (2015). "Atypical centrioles during sexual reproduction". Front Cell Dev Biol. ج. 3: 21. DOI:10.3389/fcell.2015.00021. PMC:4381714. PMID:25883936.
- Blachon، S.؛ Cai، X.؛ Roberts، K. A.؛ Yang، K.؛ Polyanovsky، A.؛ Church، A.؛ Avidor-Reiss، T. (مايو 2009). "A Proximal Centriole-Like Structure Is Present in Drosophila Spermatids and Can Serve as a Model to Study Centriole Duplication". Genetics. ج. 182 ع. 1: 133–44. DOI:10.1534/genetics.109.101709. PMC:2674812. PMID:19293139.
- Avidor-Reiss، Tomer؛ Leroux، Michel R (2015). "Shared and Distinct Mechanisms of Compartmentalized and Cytosolic Ciliogenesis". Current Biology. ج. 25 ع. 23: R1143–50. DOI:10.1016/j.cub.2015.11.001. PMC:5857621. PMID:26654377.
باللغة العربيَّة
- ألباني، عبد الرحمن؛ المالكي، عبد الله أبو عشي؛ إبراهيم، عبد اللطيف الشيخ (1995). معجم المصطلحات الدينية: عربي-إنجليزي. العبيكان للنشر. ص. 135. ISBN:9789960201528. مؤرشف من الأصل في 2022-02-10. اطلع عليه بتاريخ 2022-02-10.
- حسب المصادر التالية:
- ناصر الدين، ناصر فضل الله (2007). المعجم الطبي الإنكليزي. دار ومؤسسة رسلان. ج. الثاني. ص. 265. ISBN:9796500084121. مؤرشف من الأصل في 2022-02-10. اطلع عليه بتاريخ 2022-02-10.
- معجم مصطلحات التقانة الحيوية في الغذاء والزراعة. منظمة الأغذية والزراعة. 2021. ص. 315. ISBN:9789251342626. مؤرشف من الأصل في 2022-02-10. اطلع عليه بتاريخ 2022-02-10.
- حسب المصادر التالية:
- الحسيني، أيمن (1996). قاموس ابن سينا الطبي. مكتبة ابن سينا للنشر والتوزيع والتصدير. ص. 321. ISBN:9772712024. مؤرشف من الأصل في 2020-09-04.
- سارة، قاسم (2013). معجم أكاديميا الطبي الجديد (ط. الأولى). أكاديميا إنترناشيونال. ص. 629. ISBN:9789953370927.
- الخياط، محمد هيثم (2006). المعجم الطبي الموحد (ط. الرابعة). منظمة الصحة العالمية. ص. 1945. ISBN:9953337268. مؤرشف من الأصل في 2020-09-04.
- حسب المصادر التالية:
- العبيدي، خالد فائق صديق (2009). الوراثة والاستنساخ. دار الكتب العلمية. ص. 9. ISBN:9782745146236. مؤرشف من الأصل في 2022-02-10. اطلع عليه بتاريخ 2022-02-10.
- مؤتمر كلية الحقوق (2010). الحماية القانونية للأسرة بين الواقع والطموح. جامعة عمان الأهلية. ص. 219. ISBN:9796500022574. مؤرشف من الأصل في 2022-02-10. اطلع عليه بتاريخ 2022-02-10.
- طه، علي (2000). الاستنساخ الجيني بين العلم والدين. دار الندى. ص. 23. مؤرشف من الأصل في 2022-02-10. اطلع عليه بتاريخ 2022-02-10.
- حسب المصادر التالية:
- النجار، زغلول (2018). قصة الخلق. مؤسسة بداية للنشر والتوزيع. ص. 21. ISBN:9789777381543. مؤرشف من الأصل في 2022-02-10. اطلع عليه بتاريخ 2022-02-10.
- فضل الله، محمد حسين (1997). الندوة: سلسلة ندوات الحوار الأسبوعية بدمشق. دار الملاك. ص. 516. ISBN:9789953600604. مؤرشف من الأصل في 2022-02-10. اطلع عليه بتاريخ 2022-02-10.
- بوابة تشريح
- بوابة طب
- بوابة علم الأحياء الخلوي والجزيئي