التهاب دماغ مضاد مستقبل نمدا
التهاب دماغ بأضداد المستقبلات نمدا NMDA أو التهاب دماغ بأضداد المستقبل ن-مثيل-د-أسبارتات (بالإنجليزية: Anti-NMDA receptor encephalitis) هو من أنواع التهاب الدماغ بسبب الأجسام المضادة.[2] تُعتبر الحمى من الأعراض المُبكرة للمرض، بالإضافة إلى الصداع والشعور بالتعب،[1][4] وتُتْبَع عادةً بذهان والذي يظهر على شكل أوهام (رؤية أو سماع أشياء لا يراها أو يسمعها الآخرون) وهلوسة،[1] وغالبًا ما يكون المصابون لديهم هياج أو تشويش،[1] ومع مرور الوقت تظهر نوبات صرع ونقص التهوية وخلل الوظائف المستقلة (اضطراب في ضغط الدم ومعدل ضربات القلب).[1]
| التهاب دماغ بأضداد المستقبلات نمدا NMDA | |
|---|---|
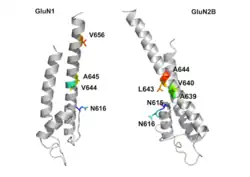 رسم تخطيطي لمستقبل ن-مثيل-د-أسبارتات رسم تخطيطي لمستقبل ن-مثيل-د-أسبارتات | |
| معلومات عامة | |
| الاختصاص | طب الجهاز العصبي، طب نفسي |
| من أنواع | التهاب الدماغ |
| الأسباب | |
| عوامل الخطر | ورم مسخي، غير معروف[1][2] |
| المظهر السريري | |
| البداية المعتادة | على مدى أيام إلى أسابيع[3] |
| الأعراض | مبكرًا: حمى، وجع رأس، شعور بالتعب، ذهان،هيجان[1][4] لاحقًا: نوبة، نقص التهوية، خلل الوظائف المستقلة[1] |
| المضاعفات | مشاكل عقلية أو سلوكية طويلة الأمد[4] |
| الإدارة | |
| التشخيص | أجسام مضادة خاصة في السائل الدماغي الشوكي[1] |
| العلاج | دواء كبت مناعة، جراحة[1] |
| أدوية | |
| المآل | عادةً جيدة (مع العلاج)[1] |
| حالات مشابهة | التهاب الدماغ الفيروسي، ذهان، متلازمة مضادات الذهان الخبيثة[4] |
| الوبائيات | |
| انتشار المرض | شائع نسبيًا[4] |
| الوفيات | ~4% خطر الوفاة[4] |
حوالي نصف الحالات ترتبط مع أورام، غالباً ورم مسخي في المبايض، بينما سبب الحالات الأخرى غير واضح.[1][2] الآلية المرضية الكامنة هي مناعية ذاتية مع هدف أساسي هو تحت الوحدة GluN1 subunit في مستقبلات NMDAR (مستقبل N-مثيل-D-أسبارتات) في الدماغ.[5][6] يعتمد التشخيص عادة على وجود أضداد نوعية في السائل الدماغي الشوكي.[1] الرنين المغناطيسي للدماغ MRI غالباً طبيعي.[4] التشخيص الخاطئ شائع الحدوث.[6]
يتم العلاج عادة بالأدوية الكابحة للمناعة، وفي حال وجود الورم، يجب أن يتم استئصاله بالجراحة.[1] عند العلاج حوالي 80% من الناس لديهم نتائج جيدة.[1] تكون النتائج أفضل عند بدء العلاج باكراً.[4] قد تبقى مشاكل عقلية وسلوكية على الأمد الطويل.[4] حوالي 4% من هؤلاء المرضى يتوفون.[4] تكرار الإصابة يحدث عند حوالي 10% من الناس.[1]
هذه الحالة شائعة نسبيًا،[4] وحوالي 80% من الحالات تكون في النساء.[4] يحدث عادةً في البالغين الأقل عمرهم من 45 عامًا، ولكن قد يحدث في أي سن.[2][6] يُعتبر جوزيف دالماو أول من وصف المرض عام 2007.[1][7]
العلامات والأعراض
قبل أن تتطور الأعراض النوعية لالتهاب الدماغ بأضداد المستقبلات NMDA، قد يعاني المصابين بأعراض بادرية، تتضمن صداع، أعراض شبيهة بالإنفلونزا، أو أعراض شبيهة بعدوى تنفسية علوية. هذه الأعراض قد تكون موجودة قبل أسابيع أو أشهر من بدء المرض.[8] بعد الأعراض البادرية، يتطور المرض بمعدلات متفاوتة، ويمكن أن يشتكي المرضى من أعراض عصبية متنوعة. خلال المرحلة البدئية للمرض، تختلف الأعراض قليلاً بين الأطفال والبالغين. على كل حال، تعتبر تغيرات السلوك هي أول الأعراض شيوعاً في كلا المجموعتين. تتضمن هذه التغيرات عادة الهياج، ذهان كبريائي، ذهان، وسلوك عدواني. تتضمن المظاهر الأخرى الأولى الشائعة نوبات صرعية، حركات غريبة، غالباً للشفاه والفم، ولكن تتضمن أيضاً حركات في الساقين واليدين تشبه العزف على البيانو. بعض الأعراض الأخرى النموذجية في بداية المرض تتضمن ضعف الإدراك، مشاكل في الذاكرة والكلام (تتضمن عدم القدرة على الكلام -الحبسة- (بالإنجليزية: aphasia)، المواظبة على الكلام (بالإنجليزية: preservation)، أو الخرس (بالإنجليزية: mutism)).[9][10] تظهر عادة الأعراض على شكل أعراض نفسية، مما يؤدي إلى ارتباك عند وضع التشاخيص التفريقية. في العديد من الحالات، يؤدي هذا إلى عدم تشخيص المرض.[11] بتطور المرض، تصبح الأعراض خطيرة وتتضمن غالباً فشل الجهاز العصبي الذاتي، نقص التهوية، رَنَح مخيخي، خزل شقي،[12] فقدان الوعي، الجمود (بالإنجليزية: catatonia). خلال المرحلة الحادة، يتطلب معظم المرضى علاج في وحدة العناية المشددة ICU) Intensive Care Unit) للحفاظ على استقرار التنفس، معدل ضربات القلب، وضغط الدم. من السمات المميزة لالتهاب الدماغ بأضداد المستقبلات NMDA هو الوجود المتزامن للعديد من الأعراض التي ذُكرت سابقاً. يحدث عند غالبية المرضى أربعة أعراض على الأقل، ويحدث لدى العديد من المرضى ستة أو سبعة أعراض خلال فترة مرضهم.[9][10]
الفيزيولوجيا المرضية
تحدث الحالة بسبب الأضداد الذاتية التي تستهدف مستقبلات NMDA في الدماغ. هذه يمكن أن تُنتج بسبب التشابه مع مستقبلات NMDA الموجودة في الورم المسخي، والذي يحوي أنواع عديدة من الخلايا، منها الخلايا الدماغية، ولهذا يمكن أن تحدث ثغرة في التحمل المناعي. الآليات المناعية الذاتية الأخرى يُشك بها في المرضى الذين ليس لديهم أورام. في حين أن الآلية الإمراضية للمرض ما تزال موضع نقاش، التقييم التجريبي لمنشأ الأجسام المضادة للـ NMDA في المصل والسائل الدماغي الشوكي يوجه لآليتين محتملتين. تستخدم هذه الآليات بعض الملاحظات البسيطة. أضداد مستقبلات NMDA المصلية توجد بتراكيز أعلى من الأضداد الموجودة في السائل الدماغي الشوكي، بمعدل أعلى بعشر مرات.[13][14] هذا يقترح بشكل قوي أن إنتاج الأضداد جهازي أكثر من كونه دماغي أو من السائل الدماغي الشوكي. عندما تكون التراكيز الكلية لـلغلوبيولين مناعي ج IgG طبيعية فإنه يجب التحقق من التركيب داخل القراب. وهذا يعني أن هناك أضداد لمستقبلات NMDA في السائل الدماغي الشوكي أكثر مما هو متوقع بالنظر إلى الكميات المتوقعة من IgG الكلي.
- النقل المنفعل يؤدي لانتشار الأضداد من الدم إلى الدماغ عبر الحاجز الدموي الدماغي المصاب (BBB).[15] هذا المرشح الخلوي، يفصل الجهاز العصبي المركزي عن الدوران الجهازي، في الحالة الطبيعية يمنع الجزيئات الكبيرة من المرور للدماغ. وقد اُقترح العديد من الأسباب لفقدان سلامة الحاجز، وكان الجواب الأكثر احتمالاً هو الآثار المترتبة من الالتهاب الحاد في الجهاز العصبي. وبالمثل وُجِدَ أن تأثير الهرمون المحرر لحاثات قشر الكظر (بالإنجليزية: corticotropin releasing hormone (CRH)) على الخلايا البدينة (بالإنجليزية: mast cells) في حالات الشدة الحادة يسهل من اختراق الحاجز الدماغي الدموي.[16] على كل حال، إن اضطراب وظيفة الجهاز العصبي الذاتي التي ظهرت في العديد من المرضى في المراحل المتأخرة من المرض قد تساعد في عبور الأضداد. على سبيل المثال، ارتفاع الضغط يؤدي إلى إجبار البروتينات الكبيرة الحجم، مثل الأضداد، للتسرب إلى السائل الدماغي الشوكي.
- الإنتاج داخل القراب (إنتاج الأضداد في الحيز داخل القراب intrathecal space) هو آلية محتملة أيضاً. دالمو Dalmau وآخرون أثبتوا أن 53 من أصل 58 مريض قد حافظوا على الأقل جزئياً على وظيفة الحاجز الدموي الدماغي، بينما كان لديهم تركيز عالي من الأضداد في السائل الدماغي الشوكي. علاوة على ذلك، سيكلوفوسفاميد (بالإنجليزية: cyclophosphamide) وريتوكسيماب (بالإنجليزية: rituximab)،[17] الأدوية التي تستخدم لكبح المناعة، قد أظهرت نجاحاً كخط ثاني في العلاج عند فشل الخط الأول من المعالجة المناعية.[18] تخرب هذه الأدوية الخلايا المنتجة للأضداد في الحويصلة الغمدية (بالإنجليزية: thecal sac)، وبالتالي التخفيف من الأعراض.
تحليلات أكثر تعقيداً لتفسير وجود الأضداد في السائل الدماغي الشوكي تشير إلى تداخل الآليتين مع بعضها لإحداث المرض.
الأضداد
بمجرد دخول الأضداد للسائل الدماغي الشوكي، ترتبط الأضداد بتحت الوحدة NR1 الخاصة بالمستقبل NMDA. هنالك ثلاث طرق محتملة لإحداث الضرر العصبي.
- نقص في كثافة المستقبلات NMDA في العقدة بعد المشبك، بسبب ارتباط الأضداد بالمستقبلات. هذا يعتمد على النهايات التشابكية للأضداد.[19]
- عمل أضداد مستقبلات NMDA شبيه بعمل الأدوية الحاصرة للمستقبلات (بالإنجليزية: antagonism)، مثل فينسيكليدين (بالإنجليزية: phencyclidine) وكيتامين (بالإنجليزية: ketamine).
- تفعيل شلال المتممة عبر الطريق الكلاسيكي (تفاعل ضد-مستضد). معقد الهجوم الغشائي (بالإنجليزية: Membrane attack complex)هو واحد من المنتجات النهائية لشلال المتممة[20] والذي يمكن أن يدخل إلى العصبونات كجزيء برميلي، يسمح بدخول الماء. بعد ذلك تنحل الخلية. ومن الجدير بالذكر أن هذه الآلية غير محتملة لأنها تسبب موت الخلية، وهو أمر لا يتفق مع الأدلة الحالية.
التشخيص
أولاً وقبل أي شيء يجب وجود درجة عالية من الشك السريري خاصة عند اليافعين الذين يظهرون سلوكاً غير طبيعي وكذلك عدم استقرار ذاتي. قد يكون لدى المصاب تبدل في الإحساسات ونوبات صرعية في المراحل المبكرة للمرض. قد يكشف الفحص السريري عن وجود أوهام وهلاوس.
العلاج
إذا وُجِدَ لدى المريض ورم، يكون المآل بشكل عام على المدى الطويل أفضل والنكس أقل بكثير. لأن الورم يمكن استئصاله جراحياً، وبالتالي القضاء على مصدر الأضداد الذاتية. بشكل عام، يُعتقد أن التشخيص المبكر والعلاج المكثف يحسنان من حالة المريض، ولكن يبقى من المستحيل معرفة ذلك من دون بيانات التجارب.[9] لأن غالبية المرضى يلجؤون في البداية لأطباء نفسيين، فمن الهام لكل الأطباء (خاصة أطباء علم النفس) أن يأخذوا بعين الاعتبار التهاب الدماغ بأضداد مستقبلات NMDA كسبب محتمل للذهان الحاد عند المرضى الشباب الذين ليس لديهم تاريخ طبي نفسي عصبي.
- إذا تم اكتشاف الورم، يجب أن تتم إزالته بالتزامن مع إعطاء أدوية الخط الأول المناعية. يجب أن تتضمن الستيروئيدات لكبح المناعة، الغلوبيولين المناعي وريدياً، وفصادة البلازما (بالإنجليزية: plasmapheresis) للتخلص من الأضداد الذاتية. وأظهرت دراسة أجريت على 577 مريض أنه على مدى أربعة أسابيع، تحسن نصف المرضى تقريباً بعد تلقي الخط الأول من العلاج المناعي.[9]
- يتضمن الخط الثاني للأدوية المناعية ريتوكسيماب (بالإنجليزية: rituximab)، وهي عبارة عن أضداد وحيدة النسيلة تستهدف مستقبل CD20 الموجود على سطح الخلايا البائية (بالإنجليزية: B cells)، وبالتالي تدمير رد الفعل المناعي الذاتي للخلايا البائية. سيكلوفوسفاميد (بالإنجليزية: Cyclophosphamide)، وهو عامل مؤلكِل يرتبط مع الحمض النووي DNA ويستخدم لعلاج كل من السرطان وأمراض المناعة الذاتية، وأثبت فعاليته أحياناً عند فشل العلاجات الأخرى.
- الأدوية الأخرى، مثل أليمتوزوماب (بالإنجليزية: alemtuzumab)، تبقى تجريبية.[21]
المآل
الشفاء من التهاب الدماغ بأضداد مستقبلات NMDA يمكن أن يأخذ عدة أشهر. تعود الأعراض لتظهر بترتيب عكسي: يمكن أن يعاني المريض من الذهان مجدداً، مما يدفع العديد من الأشخاص للاعتقاد بشكل خاطئ أن المريض لا يتعافى. مع استمرار عملية الشفاء، يتلاشى الذهان. وأخيراً، يبدأ السلوك الاجتماعي والوظائف التنفيذية للشخص بالتحسن.[8]
الوبائيات
إن عدد الحالات المرضية الجديدة خلال السنة غير معروف.[22] حسب مشروع كاليفورنيا لالتهاب الدماغ (بالإنجليزية: California Encephalitis Project)، معدل حدوث المرض أعلى من نظيره «التهاب الدماغ الفيروسي الفردي» في الأعمار الأقل من 30 عاماً.[23] أكبر سلسلة حالات حتى الآن سجلت 577 مريضاً مصابين بالتهاب الدماغ بأضداد مستقبلات NMDA. البيانات الوبائية كانت محدودة، لكن هذه الدراسة توفر أفضل معلومات عن انتشار المرض. وُجد أن الإناث أكثر عرضةً للإصابة، حيث كانت 81% من الحالات المسجلة عند الإناث. يميل ظهور المرض عند الأطفال، مع متوسط عمر التشخيص 21 سنة. أكثر من ثلث الحالات ظهرت عند الأطفال، بينما 5% من الحالات شُخصت عند الأشخاص فوق 45 سنة. نفس الدراسة أظهرت أن 394 من أصل 501 مريض (79%) تحسنت حالتهم الصحية خلال 24 شهر.[9] 30 مريض (6%) ماتوا، والباقي حدث لديهم عجز متوسط لشديد. أكدت الدراسة أيضاً أن المرض أكثر حدوثاً عند الأشخاص ذوي الأصل الآسيوي أو الإفريقي.
اجتماعياً وثقافياً
- يشتبه بكونها السبب الخفي للاعتقادات التاريخية بالمس الشيطاني.[24][25][26][27]
- كتبت مراسلة نيويورك بوست New York Post سوزانا كاهالان Susannah Cahalan كتاباً بعنوان دماغ يشتعل: شهري من الجنون (بالإنجليزية: Brain on Fire: My Month of Madness) عن تجربتها مع المرض.[28] وقد تحول هذا لاحقاً إلى فيلم يحمل نفس الاسم.[29]
- قضى أموبي أوكوي (بالإنجليزية: Amobi Okoye) لاعب في خط الدفاع في فريق دالاس كاوبويز (بالإنجليزية: Dallas Cowboys) 17 شهراً يتصارع مع التهاب الدماغ بأضداد مستقبلات NMDA. بالإضافة لذلك قضى 3 أشهر بغيبوبة محدثة طبياً، حدث لديه فجوة في الذاكرة لمدة 145 يوم وخسر 78 باوند (حوالي ~35.3 كيلوغرام) من وزنه. عاد للتدريب في 23 تشرين الأول 2014.[30]
- كنوت (بالإنجليزية: Knut)، دب قطبي في حديقة الحيوان في برلين Berlin Zoological Garden توفي في 19 آذار2011، شُخص بالتهاب الدماغ بأضداد مستقبلات NMDA في آب 2015. كانت هذه أول حالة اكتشفت خارج الإنسان.[31][32][33]
انظر أيضًا
المراجع
- Kayser، MS؛ Dalmau، J (سبتمبر 2016). "Anti-NMDA receptor encephalitis, autoimmunity, and psychosis". Schizophrenia Research. ج. 176 ع. 1: 36–40. DOI:10.1016/j.schres.2014.10.007. PMC:4409922. PMID:25458857.
- Venkatesan، A؛ Adatia، K (20 ديسمبر 2017). "Anti-NMDA-Receptor Encephalitis: From Bench to Clinic". ACS Chemical Neuroscience. ج. 8 ع. 12: 2586–2595. DOI:10.1021/acschemneuro.7b00319. PMID:29077387.
- Niederhuber, John E.; Armitage, James O.; Doroshow, James H.; Kastan, Michael B.; Tepper, Joel E. (2013). Abeloff's Clinical Oncology E-Book (بالإنجليزية). Elsevier Health Sciences. p. 600. ISBN:9781455728817. Archived from the original on 2019-12-16.
- Kayser، MS؛ Dalmau، J (2011). "Anti-NMDA Receptor Encephalitis in Psychiatry". Current Psychiatry Reviews. ج. 7 ع. 3: 189–193. DOI:10.2174/157340011797183184. PMC:3983958. PMID:24729779.
- Kayser، MS؛ Dalmau، J (سبتمبر 2016). "Anti-NMDA receptor encephalitis, autoimmunity, and psychosis". Schizophrenia Research. ج. 176 ع. 1: 36–40. DOI:10.1016/j.schres.2014.10.007. PMC:4409922. PMID:25458857.
- Minagar, Alireza; Alexander, J. Steven (2017). Inflammatory Disorders of the Nervous System: Pathogenesis, Immunology, and Clinical Management (بالإنجليزية). Humana Press. p. 177. ISBN:9783319512204. Archived from the original on 2019-04-04. Retrieved 2018-07-14.
- Dalmau، Josep؛ Tüzün، Erdem؛ Wu، Hai-yan؛ Masjuan، Jaime؛ Rossi، Jeffrey E.؛ Voloschin، Alfredo؛ Baehring، Joachim M.؛ Shimazaki، Haruo؛ Koide، Reiji؛ King، Dale؛ Mason، Warren؛ Sansing، Lauren H.؛ Dichter، Marc A.؛ Rosenfeld، Myrna R.؛ Lynch، David R. (2007). "Paraneoplastic anti-N-methyl-D-aspartate receptor encephalitis associated with ovarian teratoma". Annals of Neurology. ج. 61 ع. 1: 25–36. DOI:10.1002/ana.21050. PMC:2430743. PMID:17262855.
- Dalmau، Josep؛ Gleichman، Amy J؛ Hughes، Ethan G؛ Rossi، Jeffrey E؛ Peng، Xiaoyu؛ Lai، Meizan؛ Dessain، Scott K؛ Rosenfeld، Myrna R؛ Balice-Gordon، Rita؛ Lynch، David R (2008). "Anti-NMDA-receptor encephalitis: Case series and analysis of the effects of antibodies". The Lancet Neurology. ج. 7 ع. 12: 1091–8. DOI:10.1016/S1474-4422(08)70224-2. PMC:2607118. PMID:18851928.
- Titulaer، Maarten J؛ McCracken، Lindsey؛ Gabilondo، Iñigo؛ Armangué، Thaís؛ Glaser، Carol؛ Iizuka، Takahiro؛ Honig، Lawrence S؛ Benseler، Susanne M؛ Kawachi، Izumi؛ Martinez-Hernandez، Eugenia؛ Aguilar، Esther؛ Gresa-Arribas، Núria؛ Ryan-Florance، Nicole؛ Torrents، Abiguei؛ Saiz، Albert؛ Rosenfeld، Myrna R؛ Balice-Gordon، Rita؛ Graus، Francesc؛ Dalmau، Josep (2013). "Treatment and prognostic factors for long-term outcome in patients with anti-NMDA receptor encephalitis: An observational cohort study". The Lancet Neurology. ج. 12 ع. 2: 157–65. DOI:10.1016/S1474-4422(12)70310-1. PMC:3563251. PMID:23290630.
- Dalmau، J؛ Lancaster، E؛ Martinez-Hernandez، E؛ Rosenfeld، MR؛ Balice-Gordon، R (يناير 2011). "Clinical experience and laboratory investigations in patients with anti-NMDAR encephalitis". The Lancet. Neurology. ج. 10 ع. 1: 63–74. DOI:10.1016/s1474-4422(10)70253-2. PMC:3158385. PMID:21163445.
- Greiner، Hansel؛ Leach، James L.؛ Lee، Ki-Hyeong؛ Krueger، Darcy A. (أبريل 2011). "Anti-NMDA receptor encephalitis presenting with imaging findings and clinical features mimicking Rasmussen syndrome". Seizure. ج. 20 ع. 3: 266–270. DOI:10.1016/j.seizure.2010.11.013. PMID:21146427. مؤرشف من الأصل في 2015-09-24.
- Cahalan, Susannah. Brain on Fire-My Month of Madness, New York: Simon & Schuster, 2013.
- Irani SR، Bera K، Waters P، Zuliani L، Maxwell S، Zandi MS، Friese MA، Galea I، Kullmann DM، Beeson D، Lang B، Bien CG، Vincent A (يونيو 2010). "N-methyl-D-aspartate antibody encephalitis: temporal progression of clinical and paraclinical observations in a predominantly non-paraneoplastic disorder of both sexes". Brain. ج. 133 ع. 6: 1655–67. DOI:10.1093/brain/awq113. PMC:2877907. PMID:20511282.
- Suh-Lailam BB، Haven TR، Copple SS، Knapp D، Jaskowski TD، Tebo AE (يونيو 2013). "Anti-NMDA-receptor antibody encephalitis: performance evaluation and laboratory experience with the anti-NMDA-receptor IgG assay". Clin Chim Acta. ج. 421: 1–6. DOI:10.1016/j.cca.2013.02.010. PMID:23454475.
- Moscato، Emilia H.؛ Jain، Ankit؛ Peng، Xiaoyu؛ Hughes، Ethan G (2010). "Mechanisms underlying autoimmune synaptic encephalitis leading to disorders of memory, behavior and cognition: Insights from molecular, cellular and synaptic studies". European Journal of Neuroscience. ج. 32 ع. 2: 298–309. DOI:10.1111/j.1460-9568.2010.07349.x. PMC:2955837. PMID:20646055.
- Rabchevsky، Alexander G.؛ Degos، Jean-Denis؛ Dreyfus، Patrick A. (1999). "Peripheral injections of Freund's adjuvant in mice provoke leakage of serum proteins through the blood–brain barrier without inducing reactive gliosis". Brain Research. ج. 832 ع. 1–2: 84–96. DOI:10.1016/S0006-8993(99)01479-1. PMID:10375654.
- BritishNational Formulary. 2012. http://www.bnf.org/bnf/index.htm%5Bتحقق+من+المصدر%5D نسخة محفوظة 18 مايو 2020 على موقع واي باك مشين.
- Florance، Nicole R.؛ Davis، Rebecca L.؛ Lam، Christopher؛ Szperka، Christina؛ Zhou، Lei؛ Ahmad، Saba؛ Campen، Cynthia J.؛ Moss، Heather؛ Peter، Nadja؛ Gleichman، Amy J.؛ Glaser، Carol A.؛ Lynch، David R.؛ Rosenfeld، Myrna R.؛ Dalmau، Josep (2009). "Anti-N-methyl-D-aspartate receptor (NMDAR) encephalitis in children and adolescents". Annals of Neurology. ج. 66 ع. 1: 11–8. DOI:10.1002/ana.21756. PMC:2826225. PMID:19670433.
- Hughes، E. G.؛ Peng، X.؛ Gleichman، A. J.؛ Lai، M.؛ Zhou، L.؛ Tsou، R.؛ Parsons، T. D.؛ Lynch، D. R.؛ Dalmau، J.؛ Balice-Gordon، R. J. (2010). "Cellular and Synaptic Mechanisms of Anti-NMDA Receptor Encephalitis". Journal of Neuroscience. ج. 30 ع. 17: 5866–75. DOI:10.1523/JNEUROSCI.0167-10.2010. PMC:2868315. PMID:20427647.
- Abbas، Abul K.؛ Lichtman، Andrew H. H.؛ Pillai، Shiv (2011). Cellular and Molecular Immunology (ط. 7th). Elsevier Health Sciences. ISBN:978-1-4377-3573-4. مؤرشف من الأصل في 2019-12-16.
- Liba، Zuzana؛ Sebronova، Vera؛ Komarek، Vladimir؛ Sediva، Anna؛ Sedlacek، Petr (2013). "Prevalence and treatment of anti-NMDA receptor encephalitis". The Lancet Neurology. ج. 12 ع. 5: 424–425. DOI:10.1016/S1474-4422(13)70070-X. PMID:23602156.
- Pruss، H.؛ Dalmau، J.؛ Harms، L.؛ Höltje، M.؛ Ahnert-Hilger، G.؛ Borowski، K.؛ Stoecker، W.؛ Wandinger، K. P. (2010). "Retrospective analysis of NMDA receptor antibodies in encephalitis of unknown origin". Neurology. ج. 75 ع. 19: 1735–9. DOI:10.1212/WNL.0b013e3181fc2a06. PMID:21060097.
- Gable، M. S.؛ Sheriff، H.؛ Dalmau، J.؛ Tilley، D. H.؛ Glaser، C. A. (2012). "The Frequency of Autoimmune N-Methyl-D-Aspartate Receptor Encephalitis Surpasses That of Individual Viral Etiologies in Young Individuals Enrolled in the California Encephalitis Project". Clinical Infectious Diseases. ج. 54 ع. 7: 899–904. DOI:10.1093/cid/cir1038. PMC:3297648. PMID:22281844.
- Daniela J. Lamas, "When the brain is under attack", بوسطن غلوب, 27 May 2013. نسخة محفوظة 26 مارس 2018 على موقع واي باك مشين.
- "A Young Reporter Chronicles Her 'Brain On Fire'", الإذاعة الوطنية العامة, 14 November 2012. نسخة محفوظة 18 يونيو 2018 على موقع واي باك مشين.
- Tam, Johnny; Zandi, Michael S. (19 Jun 2017). "The witchcraft of encephalitis in Salem". Journal of Neurology (بالإنجليزية). 264 (7): 1529–1531. DOI:10.1007/s00415-017-8546-4. ISSN:0340-5354. Archived from the original on 2019-03-30.
- Sébire, Guillaume (23 Feb 2010). "In search of lost time from "Demonic Possession" to anti-N-methyl-D-aspartate receptor encephalitis". Annals of Neurology (بالإنجليزية). 67 (1): 141–142. DOI:10.1002/ana.21928. ISSN:0364-5134. Archived from the original on 2019-12-16.
- "A YoungReporter Chronicles Her 'Brain On Fire'". Fresh Air. WHYY; NPR. 14 نوفمبر 2012. مؤرشف من الأصل في 2019-12-10. اطلع عليه بتاريخ 2013-09-20.
- "What to watch with your kids: 'Ant-Man and the Wasp,' 'Leave No Trace' and more". Washington Post (بالإنجليزية). Archived from the original on 2018-07-15. Retrieved 2018-07-14.
- Whitmire، Keith. "Cowboys' Okoye returns to practice after battling rare brain disease". www.foxsports.com. FOX Sports Southwest. مؤرشف من الأصل في 2019-04-22. اطلع عليه بتاريخ 2014-10-24.
- Nuwer، Rachel (27 أغسطس 2015). "Knut the Polar Bear's Mysterious Death Finally Solved". Smithsonian. مؤرشف من الأصل في 2018-10-06.
- Armitage، Hanae (27 أغسطس 2015). "Death of beloved polar bear, Knut, solved". Science. DOI:10.1126/science.aad1675. مؤرشف من الأصل في 2015-11-04.
- Prüss، H.؛ Leubner، J.؛ Wenke، N.K.؛ وآخرون (27 أغسطس 2015). "Anti-NMDA Receptor Encephalitis in the Polar Bear (Ursus maritimus) Knut". Scientific Reports. ج. 5 ع. 12805: 12805. DOI:10.1038/srep12805. PMC:4551079. PMID:26313569. مؤرشف من الأصل في 2017-02-22.
مصادر إضافية
- Cahalan، Susannah (4 أكتوبر 2009). "My mysterious lost month of madness". نيويورك بوست. مؤرشف من الأصل في 2012-11-16. — about her experience with the disease
- Conova، Susan (1 سبتمبر 2010). "Quick Diagnosis of Rare Disease Leads to Remarkable Recovery". Columbia University Medical Center. مؤرشف من الأصل في 2017-12-27.
- بوابة طب