إيثر تاجي
الإيثر التاجي هو مركب كيميائي حلقي يتكون من عدة مجموعات إيثر متصلة مع بعضها البعض. أشهر الإيثرات التاجية هي مركبات قليلة الوحدات من أكسيد الإيثيلين تكون فيها وحدة التكرار من أوكسي الإيثيلين CH2CH2O–. قد يكون التكرار رباعياً (تترامير n = 4)، أو خماسياً (بنتامير n = 5) أو سداسياً (هكسامير n = 6).
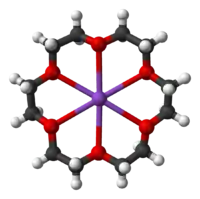
أتت تسمية الإيثر التاجي من مشابهة بنية الإيثر التاجي عند تناسقه مع كاتيون لشكل التاج على الرأس. يسمى المركب عادة باستخدام رقمين تتوسط بينهما كلمة تاج، حيث يشير الرقم الأول إلى عدد الذرات الكلي في الحلقة، أما الرقم الثاني فيشير إلى عدد ذرات الأكسجين.
التاريخ
اكتشفت مركبات الإيثرات التاجية من قبل الكيميائي تشارلز بيدرسن أثناء عمله في شركة دو بونت،[1] وحاز لاكتشافه هذا على جائزة نوبل في الكيمياء سنة 1987 بالمشاركة مع جان ماري لين ودونالد كرام.
الميزات
ترتبط الإيثرات التاجية بشكل قوي مع كاتيونات محددة مشكّلةً معقدات تناسقية، تحتل فيها ذرات الأكسجين مواقع مناسبة للتناسق مع كاتيون يتوضع داخل الحلقة، ويشكل فيها الهيكل الكربوني الكاره للماء (الدافع للماء) الإطار الخارجي للمعقد. تكون الكاتيونات عادة ذات قدرة جيدة على الانحلال في المذيبات في اللاقطبية، ولذلك فإن مركبات الإيثرات التاجية ذات أهمية في حفازات انتقال الطور.
يعتمد نوع الكاتيون المرتبط بالإيثر التاجي على حجم الحلقة، إذ غالباً ما يكون هناك تناسب بين حجم التجويف داخل الحلقة وقطر الكاتيون. فعلى سبيل المثال، فلمركب إيثر 18-تاج-6 ألفة عالية تجاه كاتيونات البوتاسيوم، أما إيثر 15-تاج-5 فله ألفة لكاتيونات الصوديوم، في حين أن إيثر 12-تاج-4 ألفة لكاتيونات الليثيوم.
.png.webp) بنى مختلفة من إيثرات تاجية شائعة: من اليمين إلى اليسار: ثنائي آزا-18-تاج-6، ثنائي بنزو-18-تاج-6، إيثر 18-تاج-6، إيثر 15-تاج-5، إيثر 12-تاج-4.
بنى مختلفة من إيثرات تاجية شائعة: من اليمين إلى اليسار: ثنائي آزا-18-تاج-6، ثنائي بنزو-18-تاج-6، إيثر 18-تاج-6، إيثر 15-تاج-5، إيثر 12-تاج-4.
المراجع
- Pedersen، C. J. (1967). "Cyclic polyethers and their complexes with metal salts". Journal of the American Chemical Society. ج. 89 ع. 26: 7017–7036. DOI:10.1021/ja01002a035.
- بوابة الكيمياء