Seewater
Seewater is water van 'n see of oseaan. Dit bedek amper 70% van die oppervlakte van die aarde. Dit is die tuiste van baie lewende organismes en is baie in beweging.
Korrosie
Dit is 'n baie korrosiewe medium wat die konstruksie van platforms, pyplyne, skepe, duikbote, fabrieke wat dit as koelmiddel gebruik, seewaterakwariums, ontsoutingsaanlegte ensomeer bemoeilik. Dit stel hoë eise aan konstruksiemateriale.[1] By petroleumontginning waar dikwele koolstofdioksied vrygestel word, is die vorming van ysterkarbonaat en verwante verbindings dikwels 'n probleem.[2] Daar is egter legerings met 'n goeie weerstand teen korrosie, soos monel.
Ontsouting
- Die hoofartikel vir hierdie afdeling is: Soutwater#Ontsouting.
Varswater is skaars, veral in droë streke, terwyl seewater volop is, maar seewater kan gewoonlik nie pleks van varswater aangewend word nie. Dit bevat 3,5% opgeloste soute veral natriumchloried. Die soute kan vandag vir meer as 99,3% met omgekeerde osmose verwyder word en daar is kuste waar dit reeds aangewend word. Die outsouting gebruik 'n membraan en lê 'n druk van 23 bar op die seewater aan. Ongelukkig vir die drinkwatervoorsiening is dit nie goedkoop nie. 'n Tipiese outsoutingsfabriek lewer in 2015 varswater vir ongeveer $0,75-$1 (VSA) per kubieke meter.[3]
Die soute
Die samestelling van seewater is nie oral dieselfde nie. Seë soos die Middellandse See en Rooisee waar veel verdamping maar weinig reënval is, het hoër konsentrasies as die gemiddelde.[4]
| Parameter | Wêreldgemiddelde [mg/L] | Middellandse See [mg/L] | Wonthaggi, Australië [mg/L] |
|---|---|---|---|
| Chloried, Cl− | 18.980 | 21.000–23.000 | 20.200 |
| Natrium, Na+ | 10.556 | 10.945–12.000 | 11.430 |
| Sulfaat, SO2−4 | 2649 | 2400–2985 | 2910 |
| Magnesium, Mg2+ | 1272 | 1371–1550 | 1400 |
| Kalsium, Ca2+ | 400 | 440–670 | 420 |
| Kalium, K+ | 380 | 410–620 | 490 |
| Waterstofkarbonaat, HCO−3 | 140 | 120–161 | |
| Bromied, Br− | 65 | 45–69 | 62 |
| Boraat, H2BO−3 | 26 | ||
| Stronsium, Sr2+ | 13 | 5–8 | 8 |
| Fluoried, F− | 1,0 | 1,2–1,6 | 0,9 |
| Tot. Opgeloste stowwe | 34.482 | 38.000–40.000 |
Seewater is oorversadig met betrekking tot die vorming van dolomiet, maar dit word vandag selde as neerslag gevorm, hoewel in die geologiese geskiedenis dit die volopste karbonaatneerslag was. Hierdie teenstrydigheid word die dolomietprobleem genoem.[5]
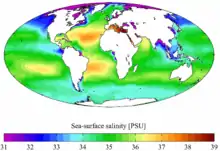
Die saliniteit
Die soutgehalte word dikwels uitgedruk in PSU (Practical Salinity Units) oftwel 1 PSU= 1 [g/kg].
In die verlede is die saliniteit dikwels bepaal deur titrasie van die chloorione wat teenwoordig is, maar dit het tot verskille tussen laboratoriums gelei. Dit word vandag bepaal deur die geleibaarheid van 'n seewatermonster te vergelyk met 'n standaardoplossing van kaliumchloried met 'n massafraksie van 32,4356 x 10-3. Die meting word verrig by T=15 °C and P=1 Atm. Die gemiddelde saliniteit van die oseane is 35,5 PSU.[6] In die Botniese Golf wissel dit egter van net 2,5 tot 4 PSU.[7] Die saliniteit is effens anders as die metings hierbo omdat elke ioon sy eie massa en sy eie beweeglikheid besit.
Die drievoudpunt

Die ewewigsdampdruk van water en die drievoudpunt van water verander afhanklik van die saliniteit.
Geleibaarheid
Seewater het 'n hoë elektriese geleibaarheid. Vergelyk:[8]
| Soort | geleibaarheid in μS/cm |
|---|---|
| suiwer water (sonder ione) | 0,055 |
| gedistilleerde water | 0,5 |
| reënwater | 5-30 |
| drinkwater | 500-1000 |
| grondwater | 30-2000 |
| seewater | 54 000 |
| gekonsentreerde sure en basisse | tot 1 000 000 |
Digtheid
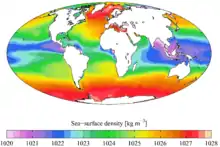
Die digtheid van seewater word gewoonlik in kg/m3 uitgedruk en dit word deur drie faktore bepaal:
- die saliniteit S, gewoonlik in kg sout per 1000 kg seewater, uitgedruk in promille ‰
- die temperatuur t, gewoonlik in °C
- die hoeveelheid gesuspendeerde materiaal (slib)
Die laaste faktor kan groot verskille in digtheid veroorsaak, maar is gewoonlik net dig by die kus naby riviermondings belangrik.
| S in ‰ | t= 0°C | t= 10°C | t=20 °C |
|---|---|---|---|
| 0 | 999,8 | 999,7 | 998,2 |
| 20 | 1016,1 | 1015,3 | 1013,4 |
| 40 | 1032,0 | 1030,7 | 1028,5 |
Die digtheid kan tussen 0<S<40‰ en 0<t<20°C benader word met die formule:[9]
Water se digtheid het 'n anomalie. Dit bereik 'n maksimum by:
- °C
Omdat saliniteit 'n groter invloed het dan temperatuur kan seewater se digtheid in onderskeidbare lae verskillend wees. Die gelaagdheid kan stabiel wees maar daar is ook seisoensinvloede vanweë die anomalie. As in die najaar die bolaag kouer word as die water daaronder kan die bolaag begin om te sink en water van verskillende dieptes kan begin om te meng.[9] Maar as die bolaag onder die temperatuur tρ-maks sak, word die bolaag ligter as die lae daaronder, hou menging op en kan dryfys gevorm word.
Afstandswaarneming
Daar is ook metodes om saliniteit vanuit 'n satelliet te bepaal. Vooruitgang in die radiometrie van die L-band van die mikrogolfgedeelte van die elektromagnetiese spektrum (1,4 GHz) het dit moontlik gemaak om met satelliete soos ESA se SMOS en NASA se Aquarius en SMAP die saliniteit van die boonste sentimeter van die oseaanwater deur afstandswaarneming vanuit die ruimte te bepaal. Hierdie gegewens is 'n aanvulling op die Argo-stelsel s'n wat dit in die oop oseaan doen. Dit is egter onmoontlik om die hele oppervlak van die oseane met hierdie metings dop te hou, maar hulle lewer 'n goeie vergelyking met die afstandwaarnemings.[10]
Hidrografie
- Die hoofartikel vir hierdie afdeling is: Hidrografie.
Die studie van wat onder die oppervlakte lê word hier op aarde gedoen en is die fokus van die hidrografie.
Verwysings
- B. Phull (2010). 2.18 - Marine Corrosion, in:Shreir's Corrosion. Elsevier. pp. 1107–1148. doi:10.1016/B978-044452787-5.00046-9. ISBN 9780444527875.
{{cite book}}: Onbekende parameter|editors=geïgnoreer (hulp)AS1-onderhoud: gebruik authors-parameter (link) - Abdullah Hussein (2023). Chapter 5 - Mineral Scales in Oil and Gas Fields, in: Essentials of Flow Assurance Solids in Oil and Gas Operations. Gulf Professional Publishing. pp. 199–296. doi:10.1016/B978-0-323-99118-6.00004-6. ISBN 9780323991186.
{{cite book}}: AS1-onderhoud: gebruik authors-parameter (link) - R.W. Baker, B.T. Low (2015). Membrane Separation, in:Reference Module in Chemistry, Molecular Sciences and Chemical Engineering. Elsevier. doi:10.1016/B978-0-12-409547-2.11674-9. ISBN 9780124095472.
{{cite book}}: AS1-onderhoud: gebruik authors-parameter (link) - Sanghyun Jeong, Gayathri Naidu, TorOve Leiknes, Saravanamuthu Vigneswaran (2017). 4.3 Membrane Biofouling: Biofouling Assessment and Reduction Strategies in Seawater Reverse Osmosis Desalination, in:Comprehensive Membrane Science and Engineering (Second Edition). Elsevier. pp. 48–71. doi:10.1016/B978-0-12-409547-2.12261-9. ISBN 9780444637963.
{{cite book}}: Onbekende parameter|editors=geïgnoreer (hulp)AS1-onderhoud: gebruik authors-parameter (link) - Fang Y, Zhang F, Farfan GA, Xu H (2021). "Low-Temperature Synthesis of Disordered Dolomite and High-Magnesium Calcite in Ethanol-Water Solutions: The Solvation Effect and Implications". ACS Omega. 7 (1): 281–292. doi:10.1021/acsomega.1c04624.
{{cite journal}}: AS1-onderhoud: gebruik authors-parameter (link) - "Sea Surface Salinity; definition and units". Salinity and remote sensing. Geargiveer vanaf die oorspronklike op 10 Augustus 2023. Besoek op 9 Augustus 2023.
- "Metabase explorer Bothinain Bay Region". NOAA.
- "Electrical Conductivity (EC)". Aqion.
- Kranenburg C. (1998). Dichtheidsstromen. TU Delft.
{{cite book}}: AS1-onderhoud: gebruik authors-parameter (link) - Nadya Vinogradova, Tong Lee, Jacqueline Boutin, Kyla Drushka, Severine Fournier, Roberto Sabia, Detlef Stammer, Eric Bayler, Nicolas Reul, Arnold Gordon, Oleg Melnichenko, Laifang Li, Eric Hackert, Matthew Martin, Nicolas Kolodziejczyk, Audrey Hasson, Shannon Brown, Sidharth Misra, Eric Lindstrom (2019). "Satellite Salinity Observing System: Recent Discoveries and the Way Forward". Front. Mar. Sci. Sec. Ocean Observation. 6. doi:10.3389/fmars.2019.00243.
{{cite journal}}: AS1-onderhoud: gebruik authors-parameter (link)