Saampersbaarheidsfaktor
Die saampersbaarheidsfaktor (Z) word gebruik om afwykings van die ideale gaswet te bestudeer. Dit beskryf die verhouding van die molekulêre volume van 'n gas tot die molekulêre volume van 'n ideale gas by dieselfde temperatuur en druk.
Vir 'n ideale gas geld:
Dat wil sê dat vir 'n ideale gas:
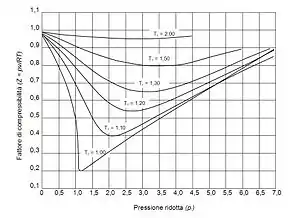
Vir 'n nie-ideale gas kan egter Z afwyk van die ideale waarde van een. Daar is twee effekte. Vir gasse soos helium is daar net 'n positiewe afwyking wat by hogere drukke lineêr toeneem. Dit is die gevolg van die feit dat heliumatome 'n eindige volume besit wat die beskikbare volume vir andere atome verlaag. Vir gasse soos CO2 is daar nog een andere, negatiewe, effek. Dit is die gevolg is van die intermolekulêre aantrekking wat die druk verlaag. Die afwykings van Z=1 word veral duidelik by lae temperature (sien grafiek).[1]
Die saamperbaarheidsfaktor kan verder beskryf word met 'n viriaalvergelyking of met die vanderwaalsvergelyking.
Kyk ook
Verwysings
- Peter Atkins, Julio de Paula Physical Chemistry 10th ed., 2014, ISBN 978-1-4292-9019-7, bls 46